1 . 部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是
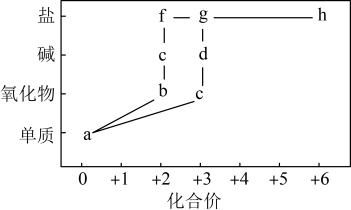
A. 在一定条件下分别与氧气或水蒸气反应均可生成相同的化合物 在一定条件下分别与氧气或水蒸气反应均可生成相同的化合物 |
B. 溶于氢碘酸的离子方程式为 溶于氢碘酸的离子方程式为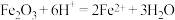 |
C. 与 与 的相互转化均可通过化合反应来实现 的相互转化均可通过化合反应来实现 |
D. 既可被氧化,也可被还原 既可被氧化,也可被还原 |
您最近一年使用:0次
名校
解题方法
2 . 下列说法或有关反应的离子方程式不正确 的是
A.与Al反应能放出H2的溶液中:NO 、Na+、Fe3+、SO 、Na+、Fe3+、SO 一定不能大量共存 一定不能大量共存 |
B.铅酸蓄电池充电时的阳极反应: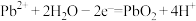 |
C.乙酰甲胺在稀盐酸中水解: |
D.向含溶质a mol的FeBr2溶液中通入b mol Cl2,充分反应,当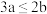 时,反应的离子方程式为: 时,反应的离子方程式为: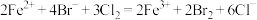 |
您最近一年使用:0次
名校
3 . 常温下,下列各组粒子在指定溶液中能大量共存的是
A. 碳酸钠溶液 碳酸钠溶液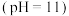 中: 中: 、 、 、 、 |
B.加入苯酚显紫色的溶液中能大量共存的离子: 、 、 、 、 、 、 |
C. 酸性 酸性 溶液中: 溶液中: 、 、 、 、 、 、 |
D.常温下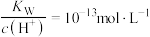 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
4 . 便携式消毒除菌卡主要活性成分为亚氯酸钠(NaClO2);一种制备NaClO2粗产品的工艺流程如图。已知纯ClO2易分解爆炸,一般用空气稀释到10%以下。
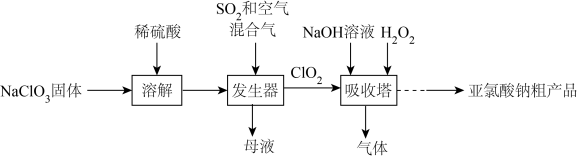
| A.溶解过程中可以用盐酸代替稀硫酸 |
| B.流程中H2O2做氧化剂 |
| C.发生器中鼓入空气的主要目的是提供氧化剂 |
| D.吸收塔中温度不宜过高,否则会导致NaClO2产率下降 |
您最近一年使用:0次
5 . 某反应体系只有六种粒子: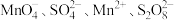 (无色)、
(无色)、 和
和 。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是
。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是
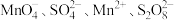 (无色)、
(无色)、 和
和 。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是
。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是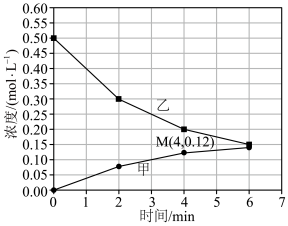
A.图中乙代表 ,甲代表 ,甲代表 |
| B.若溶液由无色变为紫红色,则反应已发生 |
C.每消耗 乙时转移 乙时转移 电子 电子 |
D.该反应为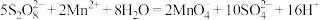 |
您最近一年使用:0次
6 . 中国古代四大发明之一的黑火药,其爆炸过程中发生反应的化学方程式为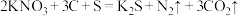 。下列说法正确的是
。下列说法正确的是
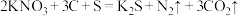 。下列说法正确的是
。下列说法正确的是| A.消耗1 mol KNO3转移电子数为6.02×1023 |
| B.S和KNO3均为还原剂 |
| C.反应过程中氮元素被还原 |
| D.CO2为还原产物 |
您最近一年使用:0次
名校
7 . 标准电极电位指离子有效浓度为1mol/L时相对标准氢电极的电极电位差值,电对的标准电极电势 越高,其电对中氧化剂的氧化性越强。酸性介质中,以下电对的标准电极电势为:①
越高,其电对中氧化剂的氧化性越强。酸性介质中,以下电对的标准电极电势为:①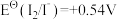 ;②
;②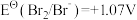 ;③
;③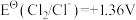 ;④
;④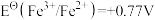 ;⑤
;⑤ ;⑥
;⑥ 。下列有关说法正确的是
。下列有关说法正确的是
 越高,其电对中氧化剂的氧化性越强。酸性介质中,以下电对的标准电极电势为:①
越高,其电对中氧化剂的氧化性越强。酸性介质中,以下电对的标准电极电势为:①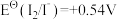 ;②
;②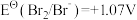 ;③
;③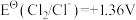 ;④
;④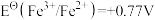 ;⑤
;⑤ ;⑥
;⑥ 。下列有关说法正确的是
。下列有关说法正确的是A.向1mol/L的HBr溶液中滴加 溶液,无明显现象发生 溶液,无明显现象发生 |
B.2mol/L的 与2mol/L的稀盐酸等体积混合有大量 与2mol/L的稀盐酸等体积混合有大量 产生 产生 |
C.在含 、 、 、 、 的混合溶液中若仅氧化 的混合溶液中若仅氧化 ,最佳的氧化剂是 ,最佳的氧化剂是 |
D.浓度相等时,还原性: |
您最近一年使用:0次
名校
8 . 电解能处理酸性工业废水中的乙醛,过程中电极反应存在如下物质间的转化:
①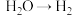 ;②
;②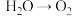 ;③
;③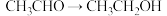 ;④
;④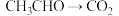 ;⑤
;⑤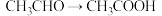 。
。
下列说法错误的是
①
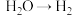 ;②
;②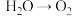 ;③
;③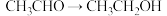 ;④
;④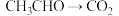 ;⑤
;⑤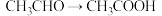 。
。下列说法错误的是
| A.发生反应②⑤的电极电势较另一电极更高 |
| B.乙醛既体现氧化性又体现还原性 |
C.当生成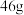 乙醇时,电路中转移 乙醇时,电路中转移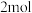 电子 电子 |
D.电解过程中,电极附近溶液的 :阴极 :阴极 阳极 阳极 |
您最近一年使用:0次
2024·浙江·模拟预测
解题方法
9 . 根据物质的组成和结构可推测其性质,下列推测不合理 的是
| 物质 | 性质描述 | 推测 | |
| A | 三甲基铝Al(CH3)3 | 暴露空气中瞬间着火,与水反应剧烈 | 水反应可得到CH4和Al(OH)3 |
| B | 三氟化氯 ClF3 | 极强助燃剂,能发生自耦电离: 2ClF3  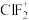 + + | BrF3比ClF3更易发生自耦电离 |
| C | 亚铁氰化钾K4[Fe(CN)6] | 食盐的抗结剂,3K4[Fe(CN)6] 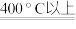 12KCN+Fe3C+5C+3N2↑ 12KCN+Fe3C+5C+3N2↑ | 在空气中灼烧,生成K2CO3、FeO、CO2和N2 |
| D | 魔酸SbF5∙HSO3F | 五氟化锑和氟磺酸的混合物,是一种酸性比普通无机酸强106~1010倍的超强酸 | SbF5∙HF是超强酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
10 . 化学需氧量(COD)是指用强氧化剂将1 L废水中的还原性物质氧化为二氧化碳和水所消耗的氧化剂的量,并换算成以O2为氧化剂时所消耗O2的质量。水体COD值常作为水体中有机污染物相对含量的综合指标之一,Fenton(Fe2+/H2O2)法能产生Fe3+和具有强氧化性的羟基自由基(·OH)引发一系列链式反应,被广泛应用于有机废水的治理。
(1)羟基自由基(·OH)的电子式为___________ 。
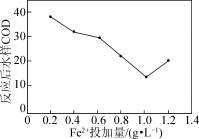
(2)分别取初始pH=4、COD=80的废水200 mL,加入200 mL H2O2,改变起始投加FeSO4·7H2O的量,反应相同时间。测得反应后水样COD随Fe2+投加量的关系如图所示。当Fe2+投加量超过1 g·L-1时,反应后水样COD不降反升的原因可能是___________ 。 )的氧化技术引起关注。研究发现,一种Mn3O4石墨烯纳米复合材料对催化活化S2O
)的氧化技术引起关注。研究发现,一种Mn3O4石墨烯纳米复合材料对催化活化S2O 产生SO
产生SO 具有很好的效果。S2O
具有很好的效果。S2O 结构如图所示。
结构如图所示。 的使用范围更广。SO
的使用范围更广。SO 在强碱性条件下反应生成·OH,写出该反应的离子方程式:
在强碱性条件下反应生成·OH,写出该反应的离子方程式:___________ 。
② 一种制取Mn3O4—石墨烯纳米复合材料的物种转化关系可表示如下(GO表示石墨烯):___________ mol。
③利用该复合材料催化活化S2O 并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为
并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为___________ 。
(1)羟基自由基(·OH)的电子式为
(2)分别取初始pH=4、COD=80的废水200 mL,加入200 mL H2O2,改变起始投加FeSO4·7H2O的量,反应相同时间。测得反应后水样COD随Fe2+投加量的关系如图所示。当Fe2+投加量超过1 g·L-1时,反应后水样COD不降反升的原因可能是
 )的氧化技术引起关注。研究发现,一种Mn3O4石墨烯纳米复合材料对催化活化S2O
)的氧化技术引起关注。研究发现,一种Mn3O4石墨烯纳米复合材料对催化活化S2O 产生SO
产生SO 具有很好的效果。S2O
具有很好的效果。S2O 结构如图所示。
结构如图所示。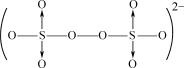
 的使用范围更广。SO
的使用范围更广。SO 在强碱性条件下反应生成·OH,写出该反应的离子方程式:
在强碱性条件下反应生成·OH,写出该反应的离子方程式:② 一种制取Mn3O4—石墨烯纳米复合材料的物种转化关系可表示如下(GO表示石墨烯):
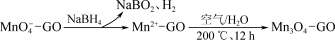
③利用该复合材料催化活化S2O
 并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为
并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为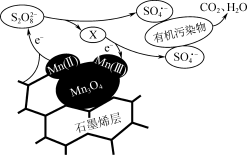
您最近一年使用:0次



