2023高三·全国·专题练习
解题方法
1 . 某危险品仓库中存放有化工原料氰化钠(NaCN),该物质有剧毒,一旦进入城市排水系统,后果不堪设想,当仓库发生火灾爆炸事故时,工作人员一方面封堵氰化钠泄漏渠道,另一方面对已经泄漏的少量氰化钠做无害化处理。根据NaCN的化合价,推测它可能有的性质是
| A.NaCN中N元素的化合价为+3价既能升高又能降低,因此该物质既有氧化性又有还原性 |
| B.NaCN中N元素的化合价为—3价只能升高,因此该物质具有还原性;C元素的化合价为+2价既能升高又能降低,因此该物质既有氧化性又有还原性 |
| C.NaCN中C元素的化合价为+4价既能升高又能降低,因此该物质既有氧化性又有还原性 |
| D.NaCN中CN—的化合价为-1价既能升高又能降低,因此该物质既有氧化性又有还原性 |
您最近一年使用:0次
2 . 某小组以4H++4I-+O2=2I2+2H2O为研究对象,探究影响氧化还原反应因素。
(1)实验Ⅳ的作用是______________ 。用CCl4萃取Ⅰ、Ⅱ、Ⅲ、Ⅳ的溶液,萃取后下层CCl4的颜色均无明显变化。
(2)取萃取后上层溶液,用淀粉检验:Ⅰ、Ⅲ的溶液变蓝;Ⅱ、Ⅳ的溶液未变蓝。溶液变蓝说明Ⅰ、Ⅲ中生成了______________ 。
(3)查阅资料:I2易溶于KI溶液。下列实验证实了该结论并解释Ⅰ、Ⅲ的萃取现象。
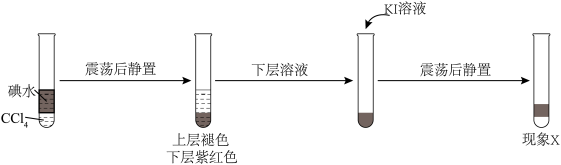
现象x是______________ 。
(4)针对Ⅱ中溶液未检出I2的原因,提出三种假设:
假设1:溶液中c(H+)较小。小组同学认为此假设不成立,依据是______________ 。
假设2:O2只氧化了SO2,化学方程式是______________ 。
假设3:I2不能在此溶液中存在。
(5)设计下列实验,验证了假设3,并继续探究影响氧化还原反应的因素。
i.取Ⅱ中亮黄色溶液,滴入品红,红色褪去。
ii.取Ⅱ中亮黄色溶液,加热,黄色褪去,经品红检验无SO2。加入酸化的AgNO3溶液,产生大量AgI沉淀,长时间静置,沉淀无明显变化。
iii.取Ⅱ中亮黄色溶液,控制一定电压和时间进行电解,结果如下。
结合化学反应,解释上表中的现象:______________ 。
(6)综合实验证据说明影响I-被氧化的因素及对应关系______________ 。
| 实验 | 气体a | 编号及现象 |
 | HCl | Ⅰ.溶液迅速呈黄色 |
| SO2 | Ⅱ.溶液较快呈亮黄色 | |
| CO2 | Ⅲ.长时间后,溶液呈很浅的黄色 | |
| 空气 | Ⅳ.长时间后,溶液无明显变化 |
(2)取萃取后上层溶液,用淀粉检验:Ⅰ、Ⅲ的溶液变蓝;Ⅱ、Ⅳ的溶液未变蓝。溶液变蓝说明Ⅰ、Ⅲ中生成了
(3)查阅资料:I2易溶于KI溶液。下列实验证实了该结论并解释Ⅰ、Ⅲ的萃取现象。

现象x是
(4)针对Ⅱ中溶液未检出I2的原因,提出三种假设:
假设1:溶液中c(H+)较小。小组同学认为此假设不成立,依据是
假设2:O2只氧化了SO2,化学方程式是
假设3:I2不能在此溶液中存在。
(5)设计下列实验,验证了假设3,并继续探究影响氧化还原反应的因素。
i.取Ⅱ中亮黄色溶液,滴入品红,红色褪去。
ii.取Ⅱ中亮黄色溶液,加热,黄色褪去,经品红检验无SO2。加入酸化的AgNO3溶液,产生大量AgI沉淀,长时间静置,沉淀无明显变化。
iii.取Ⅱ中亮黄色溶液,控制一定电压和时间进行电解,结果如下。
| 电解时间/min | 溶液 | 阳极 | 阴极 |
| t1 | 黄色变浅、有少量SO42- | 检出I2,振荡后消失 | H2 |
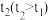 | 溶液无色、有大量SO42- | 检出I2,振荡后消失 | H2 |
(6)综合实验证据说明影响I-被氧化的因素及对应关系
您最近一年使用:0次
2019-12-21更新
|
337次组卷
|
2卷引用:2020届高考化学二轮复习大题精准训练——反应原理(历程)的探究式实验
2023高三·全国·专题练习
3 . 科学家最近研制出有望成为高效火箭推进剂的N(NO2)3(如图所示)。已知该分子中N−N−N键角都是108.1°,下列有关N(NO2)3的说法正确的是
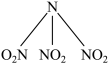

| A.分子中N、O原子间形成的共价键是非极性键 | B.分子中四个氮原子共平面 |
| C.该物质既有氧化性又有还原性 | D.分子中四个氮原子围成一个空间正四面体 |
您最近一年使用:0次
4 . 某小组探究 溶液与KI溶液的反应及其速率,实验过程和现象如表。
溶液与KI溶液的反应及其速率,实验过程和现象如表。
已知:ⅰ. 具有强氧化性,能完全电离,
具有强氧化性,能完全电离, 易被还原为
易被还原为 ;
;
ⅱ.淀粉检测 的灵敏度很高,遇低浓度的
的灵敏度很高,遇低浓度的 即可快速变蓝;
即可快速变蓝;
ⅲ. 可与
可与 发生反应:
发生反应: 。
。
(1)实验1-1的目的是________________________ 。
(2) 与KI反应的离子方程式为
与KI反应的离子方程式为________________________ 。
为了研究 与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。
与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。
(3)实验2-1不能用于测定 与KI反应的速率,原因有无
与KI反应的速率,原因有无 时反应生成少量
时反应生成少量 后淀粉立即变蓝,无法确定
后淀粉立即变蓝,无法确定 与
与 反应的浓度变化外,还有
反应的浓度变化外,还有____________ 。
(4)加入 溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。
溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。
猜想1: 先与
先与 反应,使
反应,使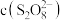 降低;
降低;
猜想2: 先与KI反应,
先与KI反应, ,
,
①甲同学提出猜想1的依据:由信息ⅲ推测, 的还原性
的还原性______ (填“强于”或“弱于”)KI的。
②乙同学根据现有数据证明猜想1不成立,理由是__________________ 。
③补全猜想2:________________________________________________ 。
(5)查阅文献表明猜想2成立。根据实验2-2的数据,计算30s内的平均反应速率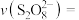
____________  (写出计算式)。
(写出计算式)。
(6)实验2-2中,30s内未检测到 与
与 反应,可能原因是
反应,可能原因是______ 。(写出2条)。
 溶液与KI溶液的反应及其速率,实验过程和现象如表。
溶液与KI溶液的反应及其速率,实验过程和现象如表。已知:ⅰ.
 具有强氧化性,能完全电离,
具有强氧化性,能完全电离, 易被还原为
易被还原为 ;
;ⅱ.淀粉检测
 的灵敏度很高,遇低浓度的
的灵敏度很高,遇低浓度的 即可快速变蓝;
即可快速变蓝;ⅲ.
 可与
可与 发生反应:
发生反应: 。
。编号 | 1-1 | 1-2 |
实验操作 |
|
|
现象 | 无明显现象 | 溶液立即变蓝 |
(2)
 与KI反应的离子方程式为
与KI反应的离子方程式为为了研究
 与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。
与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。编号 |
|
| 蒸馏水/mL | 0.4%的淀粉溶液/滴 |
| 变色时间/s |
2-1 | 2 | 0 | 2.8 | 2 | 0.2 | 立即 |
2-2 | 2 | 0.8 | 0.2 | 2 | 2 | 30 |
 与KI反应的速率,原因有无
与KI反应的速率,原因有无 时反应生成少量
时反应生成少量 后淀粉立即变蓝,无法确定
后淀粉立即变蓝,无法确定 与
与 反应的浓度变化外,还有
反应的浓度变化外,还有(4)加入
 溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。
溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。猜想1:
 先与
先与 反应,使
反应,使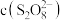 降低;
降低;猜想2:
 先与KI反应,
先与KI反应, ,
,①甲同学提出猜想1的依据:由信息ⅲ推测,
 的还原性
的还原性②乙同学根据现有数据证明猜想1不成立,理由是
③补全猜想2:
(5)查阅文献表明猜想2成立。根据实验2-2的数据,计算30s内的平均反应速率
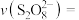
 (写出计算式)。
(写出计算式)。(6)实验2-2中,30s内未检测到
 与
与 反应,可能原因是
反应,可能原因是
您最近一年使用:0次
5 . “价—类”二维图是认识和预测元素化合物及其转化关系的重要认知模型。下列有关说法不正确的是


| A.X的浓溶液需保存在棕色试剂瓶中 | B.NO既有氧化性又有还原性 |
| C.NH3能直接转化为NO | D.反应①属于氧化还原反应 |
您最近一年使用:0次
6 . 草酸是一种常用的还原剂,某校高三化学小组探究草酸被氧化的速率问题。
(1)H2C2O4是二元弱酸,写出H2C2O4溶于水的电离方程式:_____________ 。
(2)实验I试管a中KMnO4最终被还原为Mn2+,该反应的离子方程式为:________ 。
(3)瑛瑛和超超查阅资料,实验I试管c中H2C2O4与K2Cr2O7溶液反应需数月时间才能完成,但加入MnO2可促进H2C2O4与K2Cr2O7的反应。依据此资料,吉吉和昊昊设计如下实验证实了这一点。
实验IV的目的是:_______________________ 。
(4)睿睿和萌萌对实验II继续进行探究,发现溶液中Cr2O72- 浓度变化如图:

臧臧和蔡蔡认为此变化是通过两个过程实现的。
过程i.MnO2与H2C2O4反应生成了Mn2+。
过程ii.__________________________________ 。
①查阅资料:溶液中Mn2+能被PbO2氧化为MnO4-。针对过程i,可采用如下方法证实:将0.0001molMnO2加入到6mL____________ 中,固体完全溶解;从中取出少量溶液,加入过量PbO2固体,充分反应后静置,观察到_______________ 。
②波波和姝姝设计实验方案证实了过程ii成立,她们的实验方案是________ 。
(5)综合以上实验可知,草酸发生氧化反应的速率与__________________ 有关。
| 实验Ⅰ | 试剂 | 混合后 溶液pH | 现象 (1h后溶液) | ||
| 试管 | 滴管 | ||||
 | a | 4mL0.01mol·L−1 KMnO4溶液,几滴浓H2SO4 | 2mL0.3mol·L−1H2C2O4 溶液 | 2 | 褪为无色 |
| b | 4mL0.01mol·L−1KMnO4溶液,几滴浓NaOH | 7 | 无明显变化 | ||
| c | 4mL0.01mol·L−1 K2Cr2O7溶液,几滴浓H2SO4 | 2 | 无明显变化 | ||
| d | 4mL0.01mol·L−1 K2Cr2O7溶液,几滴浓NaOH | 7 | 无明显变化 | ||
(2)实验I试管a中KMnO4最终被还原为Mn2+,该反应的离子方程式为:
(3)瑛瑛和超超查阅资料,实验I试管c中H2C2O4与K2Cr2O7溶液反应需数月时间才能完成,但加入MnO2可促进H2C2O4与K2Cr2O7的反应。依据此资料,吉吉和昊昊设计如下实验证实了这一点。
| 实验II | 实验III | 实验IV | |
| 实验操作 | 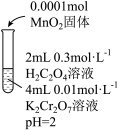 |  | 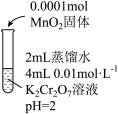 |
| 实验现象 | 6 min后固体完全溶解,溶液橙色变浅,温度不变 | 6 min后固体未溶解,溶液颜色无明显变化 | 6 min后固体未溶解,溶液颜色无明显变化 |
(4)睿睿和萌萌对实验II继续进行探究,发现溶液中Cr2O72- 浓度变化如图:

臧臧和蔡蔡认为此变化是通过两个过程实现的。
过程i.MnO2与H2C2O4反应生成了Mn2+。
过程ii.
①查阅资料:溶液中Mn2+能被PbO2氧化为MnO4-。针对过程i,可采用如下方法证实:将0.0001molMnO2加入到6mL
②波波和姝姝设计实验方案证实了过程ii成立,她们的实验方案是
(5)综合以上实验可知,草酸发生氧化反应的速率与
您最近一年使用:0次
2019-06-11更新
|
950次组卷
|
4卷引用:专题5.2 化学实验的设计与评价(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升
解题方法
7 . 下列方案设计、现象和结论不正确的是
| 实验方案 | 现象 | 结论 | |
| A | 试管中依次加入3mL乙醇2mL浓硫酸、2mL乙酸及沸石后连接好装置并加热 | 饱和碳酸钠液面上出现有香味的无色油状液体 | 有酯类物质生成 |
| B | 将 液体和 液体和 固体分别暴露在潮湿空气中 固体分别暴露在潮湿空气中 | 只有前者会冒“白烟” | 相同条件下水解程度: |
| C | 室温下,将 溶液和稀 溶液和稀 混合 混合 | 溶液变浑浊且有刺激性气味的气体生成 |  既体现还原性又体现氧化性 既体现还原性又体现氧化性 |
| D | 向 溶液中加入5滴 溶液中加入5滴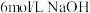 溶液 溶液 | 溶液由橙色变黄色 |  减小,平衡向 减小,平衡向 减小的方向移动 减小的方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 周期表中VIA族元素及其化合物应用广泛。 是常见的氧化剂和助燃剂。
是常见的氧化剂和助燃剂。 催化氧化是工业制硫酸的重要反应之一(中和热为
催化氧化是工业制硫酸的重要反应之一(中和热为 )。
)。 (硒)是重要的工业原材料与动物体必须营养素。提取
(硒)是重要的工业原材料与动物体必须营养素。提取 的主要原材料为电解铜产生的阳极泥。可通过阳极泥硫酸化焙烧提取
的主要原材料为电解铜产生的阳极泥。可通过阳极泥硫酸化焙烧提取 ,硫酸化焙烧提取
,硫酸化焙烧提取 的步骤主要分为两步:第一步焙烧,硫酸将单质
的步骤主要分为两步:第一步焙烧,硫酸将单质 氧化为
氧化为 。第二步还原吸收,在水中
。第二步还原吸收,在水中 将
将 转化为单质
转化为单质 。下列物质性质与用途具有对应关系的是
。下列物质性质与用途具有对应关系的是
 是常见的氧化剂和助燃剂。
是常见的氧化剂和助燃剂。 催化氧化是工业制硫酸的重要反应之一(中和热为
催化氧化是工业制硫酸的重要反应之一(中和热为 )。
)。 (硒)是重要的工业原材料与动物体必须营养素。提取
(硒)是重要的工业原材料与动物体必须营养素。提取 的主要原材料为电解铜产生的阳极泥。可通过阳极泥硫酸化焙烧提取
的主要原材料为电解铜产生的阳极泥。可通过阳极泥硫酸化焙烧提取 ,硫酸化焙烧提取
,硫酸化焙烧提取 的步骤主要分为两步:第一步焙烧,硫酸将单质
的步骤主要分为两步:第一步焙烧,硫酸将单质 氧化为
氧化为 。第二步还原吸收,在水中
。第二步还原吸收,在水中 将
将 转化为单质
转化为单质 。下列物质性质与用途具有对应关系的是
。下列物质性质与用途具有对应关系的是| A.二氧化硫具有还原性,可用作漂白剂 |
| B.硒在光照下导电性显著提高,可用作光敏材料 |
| C.臭氧能溶于水,可用作杀菌剂 |
| D.硫酸具有强氧化性,可用作干燥剂 |
您最近一年使用:0次
13-14高三上·北京海淀·期中
名校
9 . 已知下列实验事实:
① 固体既能溶于KOH溶液得到
固体既能溶于KOH溶液得到 溶液,又能溶于硫酸得到
溶液,又能溶于硫酸得到 溶液;
溶液;
②向 溶液中滴加
溶液中滴加 溶液,再酸化,可得
溶液,再酸化,可得 溶液;
溶液;
③将 溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。
溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。
下列判断不正确的是
①
 固体既能溶于KOH溶液得到
固体既能溶于KOH溶液得到 溶液,又能溶于硫酸得到
溶液,又能溶于硫酸得到 溶液;
溶液;②向
 溶液中滴加
溶液中滴加 溶液,再酸化,可得
溶液,再酸化,可得 溶液;
溶液;③将
 溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。
溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。下列判断不正确的是
A.化合物 中Cr元素为+3价 中Cr元素为+3价 |
B.实验①证明 是两性氧化物 是两性氧化物 |
C.实验②证明 既有氧化性又有还原性 既有氧化性又有还原性 |
D.实验③证明氧化性: |
您最近一年使用:0次
2022-11-29更新
|
324次组卷
|
37卷引用:苏教版2017届高三单元精练检测二化学试题
苏教版2017届高三单元精练检测二化学试题(已下线)第4讲 氧化还原反应的基本概念与规律(已下线)2014届北京市海淀区高三上学期期中考试化学试卷(已下线)2015届福建省厦门双十中学高三上学期期中化学试卷(已下线)2015届江西省新余一中高三上学期第三次模拟化学试卷2015届河北省冀州中学高三上学期期中化学A试卷2015届四川省高三“联测促改”活动第二轮测试理综化学试卷2016届河南省西华县第一高级中学高三上学期10月联考化学试卷2016届福建省大田县第一中学高三上学期期中考试化学试卷2015-2016学年江苏省镇江中学高一上学期期中考试化学试卷2016届河南省洛阳市高三上学期12月统考化学试卷2015-2016学年河北石家庄一中高一下学情反馈一化学卷2017届福建省南安一中高三暑假阶段性考试化学试卷2017届山东省淄博市淄川一中高三上学期第一次月考化学试卷2017届河北省定州中学高三上学期第二次月考化学试卷2016-2017学年河北省武邑中学高二上学期第二次月考化学试卷2017届山东省莱州一中高三上第一次质检化学试卷黑龙江省牡丹江市第一高级中学2016-2017学年高二6月月考化学试题黑龙江省牡丹江市第一高级中学2016-2017学年高二下学期期末考试化学试题北京市清华大学附属中学2016-2017学年高一下学期期中考试化学试题江西省抚州市临川区第一中学2018届高三上学期期中考试化学试题黑龙江省哈尔滨市第六中学2017-2018学年高一12月月考化学试题黑龙江省哈尔滨六中2017-2018学年高一12月月考化学试卷(已下线)北京四中2018届上学期高三年级期中考试化学试卷天津市滨海新区大港油田一中2019届高三上学期期中考试化学试题【全国百强校】北京市北京四中2019届高三上学期期中考试化学试题河北省沧州市泊头市第一中学2020届高三上学期第二次月考化学试题云南省曲靖二中2020届高三第一次月考理综化学试题(已下线)【南昌新东方】江西省九江市第一中学2015-2016学年高一上学期第二次(12月)月考化学试题(已下线)【南昌新东方】江西省九江一中2015-2016学年高一上学期第二次月考化学试卷北京师范大学附属实验中学 2019-2020 学年高一下学期 AR 层线上测试化学试题广东省珠海市第二中学2021届高三10月月考化学试题江西省兴国三中2021届高三上学期第一次月考化学试题安徽省泗县第一中学2022届高三上学期开学考试化学试题江西省樟树航天中学高三年级2021-2022学年高三上学期10月调研考试化学试题重庆南开中学2022-2023学年高一上学期期中考试化学试题广东省惠州市惠阳区中山中学2021-2022学年高一上学期第三次月考质量检测化学试题
解题方法
10 .  的还原性较强,而浓硫酸具有很强的氧化性,所以浓硫酸不能干燥
的还原性较强,而浓硫酸具有很强的氧化性,所以浓硫酸不能干燥 气体。(______)
气体。(______)
 的还原性较强,而浓硫酸具有很强的氧化性,所以浓硫酸不能干燥
的还原性较强,而浓硫酸具有很强的氧化性,所以浓硫酸不能干燥 气体。(______)
气体。(______)
您最近一年使用:0次

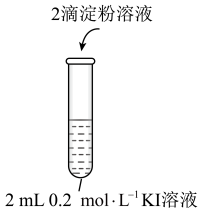
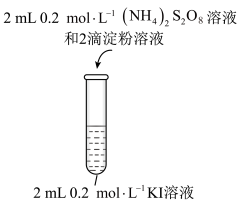
 KI溶液/mL
KI溶液/mL


