1 . 某反应中反应物与生成物有:AsH3,H2SO4,KBrO3,K2SO4,H3AsO4,H2O和一种未知物质X。
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是___________ 。
(2)已知2个BrO 在反应中得到10个电子生成1个X分子,则X的化学式为
在反应中得到10个电子生成1个X分子,则X的化学式为___________ 。
(3)根据上述反应可推知___________。
(4)写出该反应的化学方程式:___________ 。
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是
(2)已知2个BrO
 在反应中得到10个电子生成1个X分子,则X的化学式为
在反应中得到10个电子生成1个X分子,则X的化学式为(3)根据上述反应可推知___________。
| A.氧化性:KBrO3>H3AsO4 | B.氧化性:H3AsO4>KBrO3 |
| C.还原性:AsH3>X | D.还原性:X>AsH3 |
您最近一年使用:0次
名校
解题方法
2 . 亚氯酸钠 是一种高效漂白剂和强氧化剂。某兴趣小组制取
是一种高效漂白剂和强氧化剂。某兴趣小组制取 的装置如下图(
的装置如下图( 中制得
中制得 气体,
气体, 中制得
中制得 )。
)。

已知: 饱和溶液在低于38℃时析出
饱和溶液在低于38℃时析出 ,高于38℃时析出无水
,高于38℃时析出无水 ,高于60℃时
,高于60℃时 分解成
分解成 和
和 。
。
(1)实验时 中
中 稍微过量,否则会生成
稍微过量,否则会生成 。写出
。写出 中产生
中产生 的化学方程式:
的化学方程式:___________ 。
(2)装置C的作用是___________ 。
(3)为使 气体能被均匀、充分吸收,操作时应注意
气体能被均匀、充分吸收,操作时应注意___________ ;D中反应的离子方程式为___________ ;如果撤去D中的冷水浴,可能导致产品中混有的杂质是___________ 。
(4)A、E中 的作用是吸收
的作用是吸收 尾气,若反应中生成了物质的量之比为
尾气,若反应中生成了物质的量之比为 的两种阴离子,一种为
的两种阴离子,一种为 ,则另一种离子为
,则另一种离子为___________ 。
(5)反应后,经以下步骤可从装置 的溶液中获得无水
的溶液中获得无水 晶体。将实验操作补充完整。
晶体。将实验操作补充完整。
Ⅰ.55℃蒸发结晶;Ⅱ.___________ ;Ⅲ.___________ ;Ⅳ.低于60℃干燥,得到成品。
 是一种高效漂白剂和强氧化剂。某兴趣小组制取
是一种高效漂白剂和强氧化剂。某兴趣小组制取 的装置如下图(
的装置如下图( 中制得
中制得 气体,
气体, 中制得
中制得 )。
)。
已知:
 饱和溶液在低于38℃时析出
饱和溶液在低于38℃时析出 ,高于38℃时析出无水
,高于38℃时析出无水 ,高于60℃时
,高于60℃时 分解成
分解成 和
和 。
。(1)实验时
 中
中 稍微过量,否则会生成
稍微过量,否则会生成 。写出
。写出 中产生
中产生 的化学方程式:
的化学方程式:(2)装置C的作用是
(3)为使
 气体能被均匀、充分吸收,操作时应注意
气体能被均匀、充分吸收,操作时应注意(4)A、E中
 的作用是吸收
的作用是吸收 尾气,若反应中生成了物质的量之比为
尾气,若反应中生成了物质的量之比为 的两种阴离子,一种为
的两种阴离子,一种为 ,则另一种离子为
,则另一种离子为(5)反应后,经以下步骤可从装置
 的溶液中获得无水
的溶液中获得无水 晶体。将实验操作补充完整。
晶体。将实验操作补充完整。Ⅰ.55℃蒸发结晶;Ⅱ.
您最近一年使用:0次
名校
3 . 探究卤族元素单质及其化合物的性质,下列实验方案能达到探究目的的是
| 实验方案 | 探究目的 | |
| A | 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液,观察溶液颜色变化 | 氧化性:Cl2>Br2>I2 |
| B | 往碘的CCl4溶液中加入等体积浓KI溶液,振荡分层,下层由紫红色变成浅粉红色,上层呈棕黄色 | 碘在浓KI溶液的溶解能力大于在CCl4中的溶解能力 |
| C | 常温下,向盛有NaCl、NaI的混合溶液中加入2滴0.1mol·L-1AgNO3溶液,观察沉淀颜色 | Ksp(AgCl)>Ksp(AgI) |
| D | 取两份新制氯水,分别滴加AgNO3溶液和淀粉KI溶液,观察实验现象 | 氯气与水的反应是否存在限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 下列A~D四组反应中,其中Ⅰ和Ⅱ可用同一个离子方程式表示的是
| 选项 | Ⅰ | Ⅱ |
| A | 把金属铁放入稀硫酸中 | 把金属铁放入稀硝酸中 |
| B |  溶液中加入足量的 溶液中加入足量的 溶液 溶液 |  溶液中加入足量的 溶液中加入足量的 溶液 溶液 |
| C | 将 通入 通入 的溶液中 的溶液中 | 将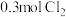 通入 通入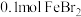 的溶液中 的溶液中 |
| D |  溶液与 溶液与 溶液反应恰好呈中性 溶液反应恰好呈中性 |  溶液与 溶液与 溶液反应使 溶液反应使 恰好沉淀 恰好沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 在处理NO废气的过程中,催化剂 会逐渐失活变为
会逐渐失活变为 。某小组为解决这一问题,实验研究
。某小组为解决这一问题,实验研究 和
和 之间的相互转化。
之间的相互转化。
资料:Ⅰ.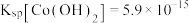

Ⅱ.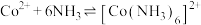
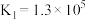
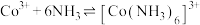
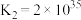
Ⅲ. 和
和 在酸性条件下均能生成
在酸性条件下均能生成
(1)探究 的还原性
的还原性
实验Ⅰ 粉红色的 溶液或
溶液或 溶液在空气中久置,无明显变化。
溶液在空气中久置,无明显变化。
实验Ⅱ 向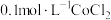 溶液中滴入2滴酸性
溶液中滴入2滴酸性 溶液,无明显变化。
溶液,无明显变化。
实验Ⅲ 按如图装置进行实验,观察到电压表指针偏转。
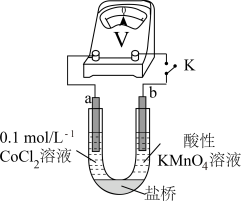
①甲同学根据实验Ⅲ得出结论: 能被酸性
能被酸性 溶液氧化。乙同学补充实验Ⅳ,
溶液氧化。乙同学补充实验Ⅳ,_______ (补全实验操作及现象),否定了该观点 。
②探究碱性条件下Co(Ⅱ)的还原性,进行实验。
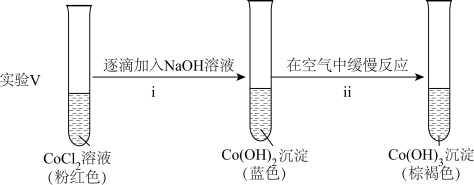
ⅱ中反应的化学方程式是_______ 。
③根据氧化还原反应规律解释还原性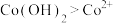 :
: 在碱性条件下,
在碱性条件下, 与
与 、
、 反应,使
反应,使 和
和 均降低,但
均降低,但_______ 降低的程度更大,还原剂的还原性增强。
(2)探究 的氧化性
的氧化性
①根据实验Ⅲ和Ⅳ推测氧化性: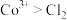 ,设计实验证明:向Ⅴ中得到的棕褐色沉淀中,
,设计实验证明:向Ⅴ中得到的棕褐色沉淀中,_______ (补全实验操作及现象),反应的离子方程式是_______ 。
②向Ⅴ中得到的棕褐色沉淀中,滴加 溶液,加入催化剂,产生无色气泡,该气体是
溶液,加入催化剂,产生无色气泡,该气体是_______ 。
 会逐渐失活变为
会逐渐失活变为 。某小组为解决这一问题,实验研究
。某小组为解决这一问题,实验研究 和
和 之间的相互转化。
之间的相互转化。资料:Ⅰ.
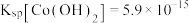

Ⅱ.
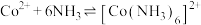
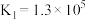
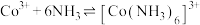
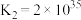
Ⅲ.
 和
和 在酸性条件下均能生成
在酸性条件下均能生成
(1)探究
 的还原性
的还原性实验Ⅰ 粉红色的
 溶液或
溶液或 溶液在空气中久置,无明显变化。
溶液在空气中久置,无明显变化。实验Ⅱ 向
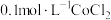 溶液中滴入2滴酸性
溶液中滴入2滴酸性 溶液,无明显变化。
溶液,无明显变化。实验Ⅲ 按如图装置进行实验,观察到电压表指针偏转。

①甲同学根据实验Ⅲ得出结论:
 能被酸性
能被酸性 溶液氧化。乙同学补充实验Ⅳ,
溶液氧化。乙同学补充实验Ⅳ,②探究碱性条件下Co(Ⅱ)的还原性,进行实验。

ⅱ中反应的化学方程式是
③根据氧化还原反应规律解释还原性
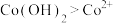 :
: 在碱性条件下,
在碱性条件下, 与
与 、
、 反应,使
反应,使 和
和 均降低,但
均降低,但(2)探究
 的氧化性
的氧化性①根据实验Ⅲ和Ⅳ推测氧化性:
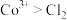 ,设计实验证明:向Ⅴ中得到的棕褐色沉淀中,
,设计实验证明:向Ⅴ中得到的棕褐色沉淀中,②向Ⅴ中得到的棕褐色沉淀中,滴加
 溶液,加入催化剂,产生无色气泡,该气体是
溶液,加入催化剂,产生无色气泡,该气体是
您最近一年使用:0次
6 . 室温下,探究 溶液的性质,下列实验方案能达到探究目的的是
溶液的性质,下列实验方案能达到探究目的的是
 溶液的性质,下列实验方案能达到探究目的的是
溶液的性质,下列实验方案能达到探究目的的是| 选项 | 探究目的 | 实验方案 |
| A |  是否变质 是否变质 | 向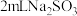 溶液中加入盐酸酸化的 溶液中加入盐酸酸化的 溶液,观察是否有沉淀生成 溶液,观察是否有沉淀生成 |
| B |  是否有还原性 是否有还原性 | 向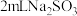 溶液中滴加几滴酸性 溶液中滴加几滴酸性 溶液,观察颜色变化 溶液,观察颜色变化 |
| C |  是否有漂白性 是否有漂白性 | 向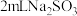 溶液中滴加溴水,观察颜色变化 溶液中滴加溴水,观察颜色变化 |
| D |  是否水解 是否水解 | 向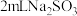 溶液中滴加 溶液中滴加 滴酚酞试液,观察溶液颜色变化 滴酚酞试液,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 .  和
和 都是重要的锂的化合物。
都是重要的锂的化合物。
I. 电极材料是动力型锂离子电池的理想正极材料。它可以通过
电极材料是动力型锂离子电池的理想正极材料。它可以通过 、
、 和
和 溶液发生共沉淀反应、将所得沉淀干燥、高温成型而制得。实验室制备
溶液发生共沉淀反应、将所得沉淀干燥、高温成型而制得。实验室制备 的方法如下:
的方法如下:
步骤1:将 置于题图所示实验装置的三颈烧瓶中,加入煮沸过的蒸馏水,搅拌使其溶解。从分液漏斗中滴加
置于题图所示实验装置的三颈烧瓶中,加入煮沸过的蒸馏水,搅拌使其溶解。从分液漏斗中滴加 溶液,并持续通入氮气。
溶液,并持续通入氮气。

步骤2:将 固体溶于蒸馏水中,迅速倒入三颈烧瓶中,快速搅拌,充分反应后,过滤、洗涤滤渣得
固体溶于蒸馏水中,迅速倒入三颈烧瓶中,快速搅拌,充分反应后,过滤、洗涤滤渣得 固体。
固体。
(1)共沉淀反应投料时,不将 和
和 溶液直接混合的原因是
溶液直接混合的原因是_______ 。
(2)工业制取 在高温成型前,常向
在高温成型前,常向 中加入少量活性炭黑,其作用除了可以改善成型后
中加入少量活性炭黑,其作用除了可以改善成型后 的导电性能外,还能
的导电性能外,还能_______ 。
Ⅱ.磷酸锂渣(主要成分为 )和废旧电极材料(含铝、炭、
)和废旧电极材料(含铝、炭、 和
和 )均可用于制取
)均可用于制取 。
。
(3)实验室以磷酸锂渣为原料制备高纯 的部分实验流程如下:
的部分实验流程如下:

“低酸转化”使 转化为
转化为 。写出“磷锂分离”的化学方程式:
。写出“磷锂分离”的化学方程式:_______ 。
(4)已知: 微溶于水;
微溶于水; 难溶于水和碱,可溶于盐酸生成
难溶于水和碱,可溶于盐酸生成 和
和 ;
; 时,
时, 沉淀完全。完善由某废旧电极材料制取
沉淀完全。完善由某废旧电极材料制取 的实验方案:边搅拌边向废旧电极材料中加入
的实验方案:边搅拌边向废旧电极材料中加入 溶液至不再产生气泡,过滤,
溶液至不再产生气泡,过滤,_______ ,过滤、洗涤,低温干燥得 固体。(实验中须使用的试剂有:双氧水、盐酸、
固体。(实验中须使用的试剂有:双氧水、盐酸、 溶液、
溶液、 溶液)
溶液)
 和
和 都是重要的锂的化合物。
都是重要的锂的化合物。I.
 电极材料是动力型锂离子电池的理想正极材料。它可以通过
电极材料是动力型锂离子电池的理想正极材料。它可以通过 、
、 和
和 溶液发生共沉淀反应、将所得沉淀干燥、高温成型而制得。实验室制备
溶液发生共沉淀反应、将所得沉淀干燥、高温成型而制得。实验室制备 的方法如下:
的方法如下:步骤1:将
 置于题图所示实验装置的三颈烧瓶中,加入煮沸过的蒸馏水,搅拌使其溶解。从分液漏斗中滴加
置于题图所示实验装置的三颈烧瓶中,加入煮沸过的蒸馏水,搅拌使其溶解。从分液漏斗中滴加 溶液,并持续通入氮气。
溶液,并持续通入氮气。
步骤2:将
 固体溶于蒸馏水中,迅速倒入三颈烧瓶中,快速搅拌,充分反应后,过滤、洗涤滤渣得
固体溶于蒸馏水中,迅速倒入三颈烧瓶中,快速搅拌,充分反应后,过滤、洗涤滤渣得 固体。
固体。(1)共沉淀反应投料时,不将
 和
和 溶液直接混合的原因是
溶液直接混合的原因是(2)工业制取
 在高温成型前,常向
在高温成型前,常向 中加入少量活性炭黑,其作用除了可以改善成型后
中加入少量活性炭黑,其作用除了可以改善成型后 的导电性能外,还能
的导电性能外,还能Ⅱ.磷酸锂渣(主要成分为
 )和废旧电极材料(含铝、炭、
)和废旧电极材料(含铝、炭、 和
和 )均可用于制取
)均可用于制取 。
。(3)实验室以磷酸锂渣为原料制备高纯
 的部分实验流程如下:
的部分实验流程如下:
“低酸转化”使
 转化为
转化为 。写出“磷锂分离”的化学方程式:
。写出“磷锂分离”的化学方程式:(4)已知:
 微溶于水;
微溶于水; 难溶于水和碱,可溶于盐酸生成
难溶于水和碱,可溶于盐酸生成 和
和 ;
; 时,
时, 沉淀完全。完善由某废旧电极材料制取
沉淀完全。完善由某废旧电极材料制取 的实验方案:边搅拌边向废旧电极材料中加入
的实验方案:边搅拌边向废旧电极材料中加入 溶液至不再产生气泡,过滤,
溶液至不再产生气泡,过滤, 固体。(实验中须使用的试剂有:双氧水、盐酸、
固体。(实验中须使用的试剂有:双氧水、盐酸、 溶液、
溶液、 溶液)
溶液)
您最近一年使用:0次
名校
解题方法
8 . 高铁酸钾( )是一种暗紫色固体,低温碱性条件下比较稳定。工业上湿法制备
)是一种暗紫色固体,低温碱性条件下比较稳定。工业上湿法制备 的流程如下:
的流程如下:

下列说法正确的是
 )是一种暗紫色固体,低温碱性条件下比较稳定。工业上湿法制备
)是一种暗紫色固体,低温碱性条件下比较稳定。工业上湿法制备 的流程如下:
的流程如下:
下列说法正确的是
A. 中铁元素的化合价是+3 中铁元素的化合价是+3 |
B.“反应”步骤的离子方程式: |
C.“过滤”所得滤液中大量存在的离子有: 、 、 、 、 、 、 、 、 |
D.“反应”步骤中 发生氧化反应 发生氧化反应 |
您最近一年使用:0次
2023-07-28更新
|
188次组卷
|
2卷引用:江苏省宿迁市2022-2023学年高一下学期2月开学考试化学试题
解题方法
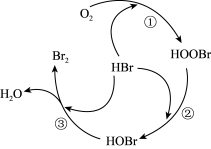
9 . 据文献报道,我国学者提出 氧化HBr生成Br2的反应历程如图所示。下列有关该历程的说法
氧化HBr生成Br2的反应历程如图所示。下列有关该历程的说法不正确 的是
 氧化HBr生成Br2的反应历程如图所示。下列有关该历程的说法
氧化HBr生成Br2的反应历程如图所示。下列有关该历程的说法
A. 氧化HBr生成 氧化HBr生成 的总反应为 的总反应为 |
| B.中间体HOOBr和HOBr中Br的化合价相同 |
C.步骤③中,每生成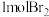 转移2mol电子 转移2mol电子 |
| D.步骤①②③均为氧化还原反应 |
您最近一年使用:0次
10 . 某经预处理的含砷废水中砷元素主要以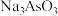 和
和 形式存在。以其为原料制备粗
形式存在。以其为原料制备粗 的部分流程如下:
的部分流程如下:
②“酸化”时发生反应:
下列说法正确的是
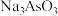 和
和 形式存在。以其为原料制备粗
形式存在。以其为原料制备粗 的部分流程如下:
的部分流程如下:

②“酸化”时发生反应:

下列说法正确的是
A.“氧化”时每 被氧化,会消耗 被氧化,会消耗 |
| B.“沉砷”和“酸化”可提高溶液中砷元素浓度,实现砷元素的富集 |
C.“酸化”时可用 溶液代替 溶液代替 溶液 溶液 |
D.“还原”过程溶液的 不断增大 不断增大 |
您最近一年使用:0次
2023-07-17更新
|
233次组卷
|
2卷引用:江苏省扬州市2022-2023学年高三下学期开学考试化学试题



