名校
1 . 回答下列问题:
(1)①写出NH3的电子式_______ ;
②甘氨酸的结构简式为_______ 。
(2)写出碳和浓硫酸加热时发生反应的化学方程式_______ ;
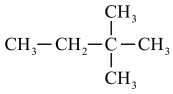
(3)图的系统命名法的名称_______ ,其二氯代物有_______ 种。
(1)①写出NH3的电子式
②甘氨酸的结构简式为
(2)写出碳和浓硫酸加热时发生反应的化学方程式
(3)图的系统命名法的名称
您最近一年使用:0次
解题方法
2 . 下表为长式元素周期表的主要部分。①~⑬代表13种元素,⑭表示元素周期表中某一区域。
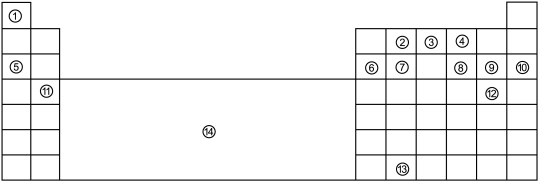
请回答:
(1)①、②、④的原子半径从大到小排列的顺序是______ 。(填化学式)
(2)①与③组成的含10个电子的阳离子的化学式是______ 。
(3)有些族的元素有特别的名称,⑨所在主族的元素叫做______ 元素。
(4)⑩的元素符号是______ 。
(5)⑪的元素名称是______ 。
(6)⑫的原子结构示意图是______ 。
(7)⑬在元素周期表中的位置是______ 。
(8)下列说法不正确 的是______ 。
A. ②的原子所含原子数即
②的原子所含原子数即 任何粒子的粒子数
任何粒子的粒子数
B.⑥、⑦的氧化物均能与⑤的最高价氧化物对应水化物反应
C.⑧的某种氧化物进入大气会形成酸雨
D.⑨的某种氧化物可用于自来水消毒
E.⑭所示区域内的元素常见于农药中
(9)⑥的单质与 溶液反应的化学方程式是
溶液反应的化学方程式是______ 。

请回答:
(1)①、②、④的原子半径从大到小排列的顺序是
(2)①与③组成的含10个电子的阳离子的化学式是
(3)有些族的元素有特别的名称,⑨所在主族的元素叫做
(4)⑩的元素符号是
(5)⑪的元素名称是
(6)⑫的原子结构示意图是
(7)⑬在元素周期表中的位置是
(8)下列说法
A.
 ②的原子所含原子数即
②的原子所含原子数即 任何粒子的粒子数
任何粒子的粒子数B.⑥、⑦的氧化物均能与⑤的最高价氧化物对应水化物反应
C.⑧的某种氧化物进入大气会形成酸雨
D.⑨的某种氧化物可用于自来水消毒
E.⑭所示区域内的元素常见于农药中
(9)⑥的单质与
 溶液反应的化学方程式是
溶液反应的化学方程式是
您最近一年使用:0次
3 . “金声玉振”学习小组设计如图实验装置(部分夹持装置已略去)检验炭与浓硫酸反应的产物。已知: 。
。

请回答:
(1)装置①中的玻璃仪器有酒精灯、玻璃弯管、______ 和______ 。
(2)设计装置②、③的目的分别是______ 。
(3)装置④中反应的离子方程式是______ 。
(4)能证明炭与浓硫酸反应的产物中有 的现象是
的现象是______ 。
(5)装置⑦的作用是______ ,优点是______ 。
 。
。
请回答:
(1)装置①中的玻璃仪器有酒精灯、玻璃弯管、
(2)设计装置②、③的目的分别是
(3)装置④中反应的离子方程式是
(4)能证明炭与浓硫酸反应的产物中有
 的现象是
的现象是(5)装置⑦的作用是
您最近一年使用:0次
解题方法
4 . 将足量 通入
通入 溶液,无明显现象,当加入某试剂(或气体)X后,有沉淀生成。X
溶液,无明显现象,当加入某试剂(或气体)X后,有沉淀生成。X不可能 是:① 、②
、② 、③
、③ 、④
、④ 溶液、⑤
溶液、⑤ 溶液、⑥
溶液、⑥ 溶液中的
溶液中的
 通入
通入 溶液,无明显现象,当加入某试剂(或气体)X后,有沉淀生成。X
溶液,无明显现象,当加入某试剂(或气体)X后,有沉淀生成。X 、②
、② 、③
、③ 、④
、④ 溶液、⑤
溶液、⑤ 溶液、⑥
溶液、⑥ 溶液中的
溶液中的| A.②⑥ | B.①② | C.③⑤⑥ | D.①②④ |
您最近一年使用:0次
解题方法
5 . 下列物质制备方法可用于大规模工业生产的是
| A.铝与氧化铁发生置换反应制铁 |
| B.加热分解氯化钠制金属钠和氯气 |
| C.硫黄与空气中的氧气反应制二氧化硫 |
| D.金属钾与熔融氯化钠反应制金属钠 |
您最近一年使用:0次
解题方法
6 . 下列说法不正确的是
A. 俗称铁红,可用作油漆、涂料的红色颜料 俗称铁红,可用作油漆、涂料的红色颜料 |
| B.还原铁粉具有强还原性,可用作食品脱氧剂 |
| C.碳酸钠溶液显碱性,可用作食用碱或工业用碱 |
D. 有毒,且有刺激性气味,不可用于食品加工 有毒,且有刺激性气味,不可用于食品加工 |
您最近一年使用:0次
解题方法
7 . 在探究 水溶液成分和性质的实验中,下列实验现象或实验结论
水溶液成分和性质的实验中,下列实验现象或实验结论不正确 的是
 水溶液成分和性质的实验中,下列实验现象或实验结论
水溶液成分和性质的实验中,下列实验现象或实验结论| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 向 水溶液中加入 水溶液中加入 粉末 粉末 | 有气泡产生 |  水溶液呈酸性 水溶液呈酸性 |
| B | 向 水溶液中滴加2滴石蕊溶液,振荡 水溶液中滴加2滴石蕊溶液,振荡 | 溶液先变红后褪色 |  有漂白作用 有漂白作用 |
| C | 向 水溶液中加入 水溶液中加入 溶液 溶液 | 有淡黄色沉淀产生 |  具有氧化性 具有氧化性 |
| D | 向 溶液中加入足量 溶液中加入足量 水溶液 水溶液 | 溶液紫色褪去 |  具有还原性 具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-14更新
|
132次组卷
|
2卷引用:浙江省宁波市鄞州高级中学2023-2024学年高二上学期12月月考化学试题
名校
8 . 下列离子方程式书写正确的是
A.大理石与稀硝酸反应: |
B.碳酸氢钠溶液和过量的澄清石灰水混合: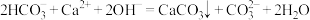 |
C.少量 通入 通入 溶液中: 溶液中: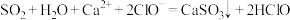 |
D.过量铁粉投入稀硝酸中: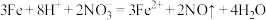 |
您最近一年使用:0次
2024-03-08更新
|
290次组卷
|
2卷引用:浙江省宁波市九校2023-2024学年高一上学期1月期末化学试题
9 . 下列说法不正确的是
| A.储氢合金要求储氢量大,金属氢化物既容易形成,受热又不容易分解 |
| B.二氧化硫可用于杀菌消毒,还是一种食品添加剂 |
| C.中国华为集团自主研发的“麒麟”芯片生产时需要用到硅 |
| D.硬铝是一种铝合金,是制造飞机和宇宙飞船的理想材料 |
您最近一年使用:0次
2024-03-08更新
|
137次组卷
|
3卷引用:浙江省宁波市九校2023-2024学年高一上学期1月期末化学试题
名校
解题方法
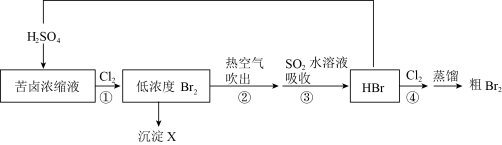
10 . 海水是资源宝库,可利用海水提溴:
资料:常用提溴原料
(1)选用苦卤浓缩液而不是天然海水作为提溴原料的原因是___________ 。
(2)海水中溴元素的存在形式是Br—,从原子结构角度解释反应①能发生的原因:___________ 。
(3)步骤③反应的化学方程式是___________ 。
(4)在海水提溴生产工艺中,通常通过蒸馏法实现溴和水的分离(蒸馏是利用物质的沸点不同而实现分离的办法)。在蒸馏的过程中,温度应控制在80~90℃,温度过高或过低都不利于生产,请解释其原因___________ 。
(5)若步骤④中通入960g SO2,实际产出Br2的质量为1920g,则实际产量Br2的产率为___________ 。(产率=实际产量/理论产量×100%)

资料:常用提溴原料
| 提溴原料 | 天然海水 | 苦卤浓缩液(浓缩海水) |
| 溴含量(g·L-1) | 0.045 | 7.270 |
(1)选用苦卤浓缩液而不是天然海水作为提溴原料的原因是
(2)海水中溴元素的存在形式是Br—,从原子结构角度解释反应①能发生的原因:
(3)步骤③反应的化学方程式是
(4)在海水提溴生产工艺中,通常通过蒸馏法实现溴和水的分离(蒸馏是利用物质的沸点不同而实现分离的办法)。在蒸馏的过程中,温度应控制在80~90℃,温度过高或过低都不利于生产,请解释其原因
(5)若步骤④中通入960g SO2,实际产出Br2的质量为1920g,则实际产量Br2的产率为
您最近一年使用:0次



