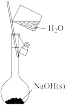1 . 某小组同学用 与浓盐酸反应制备
与浓盐酸反应制备 的过程中(装置如下图所示),观察到氯气不再逸出时,固液混合物
的过程中(装置如下图所示),观察到氯气不再逸出时,固液混合物 中仍存在盐酸和
中仍存在盐酸和 .
.

(1)发生装置中制取
 的
的(2)除杂装置①中的试剂是______(填序号)。
| A.浓硫酸 | B.饱和 溶液 溶液 |
C.饱和 溶液 溶液 | D. 溶液 溶液 |
(3)将虚线框中的收集装置补充完整
(4)尾气处理装置中发生反应的
(5)分析
 中仍存在盐酸和
中仍存在盐酸和 的可能原因。
的可能原因。ⅰ.随 降低或
降低或 浓度升高,
浓度升高, 氧化性减弱。
氧化性减弱。
ⅱ.随 降低,
降低,
设计补充实验证实上述分析。
实验操作 | 试剂 | 产物 | |
Ⅰ |
| 较浓 | 有氯气 |
Ⅱ |
| 有氯气 | |
Ⅲ |
| 无氯气 |
则 是
是 是
是
您最近一年使用:0次
2 . 磺酰氯 是重要的有机合成试剂,实验室可利用
是重要的有机合成试剂,实验室可利用 与
与 在活性炭作用下反应制取少量
在活性炭作用下反应制取少量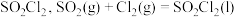 ,该反应放热,装置如图所示(部分夹持装置省略)。已知
,该反应放热,装置如图所示(部分夹持装置省略)。已知 的熔点为
的熔点为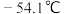 ,沸点为
,沸点为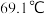 ,遇水能发生剧烈的水解反应,并产生白雾。
,遇水能发生剧烈的水解反应,并产生白雾。
回答下列问题。 ,则下列试剂组合中合适的是___________。
,则下列试剂组合中合适的是___________。
(2)导管a的作用是___________ ;仪器b中的试剂是___________ 。
(3)实验结束时,关闭分液漏斗活塞和止水夹k,此时装置戊的作用是___________ 。
(4) 遇水发生反应生成两种酸,该反应的化学方程式为
遇水发生反应生成两种酸,该反应的化学方程式为___________ 。
(5)若反应中消耗的氯气体积为 (标准状况下),最后经过分离提纯得到
(标准状况下),最后经过分离提纯得到 纯净的磺酰氯,则磺酰氯的产率为
纯净的磺酰氯,则磺酰氯的产率为___________ (产率:实际产量/理论产量 )。
)。
(6)已知酸性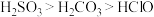 ,借助该酸性排序,使用以下装置设计实验证明
,借助该酸性排序,使用以下装置设计实验证明 的酸性强于
的酸性强于 ,其连接顺序应为
,其连接顺序应为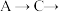
___________ 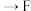 ;能证明
;能证明 的酸性强于
的酸性强于 的实验现象为
的实验现象为___________ 。
 是重要的有机合成试剂,实验室可利用
是重要的有机合成试剂,实验室可利用 与
与 在活性炭作用下反应制取少量
在活性炭作用下反应制取少量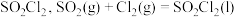 ,该反应放热,装置如图所示(部分夹持装置省略)。已知
,该反应放热,装置如图所示(部分夹持装置省略)。已知 的熔点为
的熔点为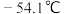 ,沸点为
,沸点为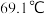 ,遇水能发生剧烈的水解反应,并产生白雾。
,遇水能发生剧烈的水解反应,并产生白雾。回答下列问题。

 ,则下列试剂组合中合适的是___________。
,则下列试剂组合中合适的是___________。A. 的硫酸和 的硫酸和 | B. 的硝酸和 的硝酸和 固体 固体 |
C. 的硫酸和 的硫酸和 固体 固体 | D. 的硫酸和 的硫酸和 固体 固体 |
(2)导管a的作用是
(3)实验结束时,关闭分液漏斗活塞和止水夹k,此时装置戊的作用是
(4)
 遇水发生反应生成两种酸,该反应的化学方程式为
遇水发生反应生成两种酸,该反应的化学方程式为(5)若反应中消耗的氯气体积为
 (标准状况下),最后经过分离提纯得到
(标准状况下),最后经过分离提纯得到 纯净的磺酰氯,则磺酰氯的产率为
纯净的磺酰氯,则磺酰氯的产率为 )。
)。(6)已知酸性
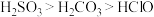 ,借助该酸性排序,使用以下装置设计实验证明
,借助该酸性排序,使用以下装置设计实验证明 的酸性强于
的酸性强于 ,其连接顺序应为
,其连接顺序应为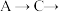
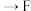 ;能证明
;能证明 的酸性强于
的酸性强于 的实验现象为
的实验现象为
您最近一年使用:0次
2024-02-23更新
|
154次组卷
|
2卷引用:广东省深圳实验学校高中部2023-2024学年高一上学期第三阶段考试化学试题
名校
解题方法
3 . 下列实验操作或装置设计合理的是
|
|
|
|
A.配制 的 的 溶液 溶液 | B.闻气体气味 | C.验证碳酸氢钠受热易分解 | D.尾气 最好用水吸收 最好用水吸收 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-03更新
|
73次组卷
|
3卷引用:广东省阳江市江城区部分学校2023-2024学年高一上学期期末联考化学试题
名校
解题方法
4 . ClO2作为一种广谱型的消毒剂,将逐渐用来取代Cl2,成为自来水的消毒剂。已知ClO2是一种易溶于水的气体,实验室制备ClO2的原理是用亚氯酸钠固体与氯气反应:2NaClO2+Cl2=2C1O2+2NaCl,下图是实验室用于制备和收集一定量纯净的ClO2的装置(某些夹持装置和垫持用品已省略),其中E用于除去ClO2中的未反应的Cl2。___________ 。
(2)写出装置A中烧瓶内发生反应的离子方程式:___________ 。
(3)B装置中所盛试剂是___________ 。
(4)F为ClO2收集装置,应选用的装置是___________ (填序号),其中与E装置导管相连的导管口是___________ (填接口字母)。
①请写出该反应的化学方程式:___________ ,每消耗319.5gNaClO3,生成___________ L氯气(标况下)。(M(NaClO3)=106.5)。
②浓盐酸在该反应中表现出来的性质是___________ (填序号)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
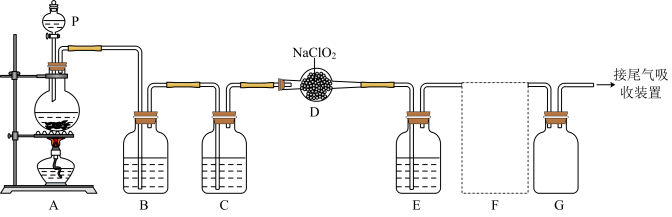
(2)写出装置A中烧瓶内发生反应的离子方程式:
(3)B装置中所盛试剂是
(4)F为ClO2收集装置,应选用的装置是

①请写出该反应的化学方程式:
②浓盐酸在该反应中表现出来的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
您最近一年使用:0次
2024-02-02更新
|
141次组卷
|
3卷引用:广东省深圳市南头中学2023-2024学年高一上学期期末调研考试(模拟)化学试题
解题方法
5 . 实验室用如图所示装置制备干燥的Cl2并探究其性质。其中,a为湿润的淀粉-KI试纸,b为湿润的红纸条。下列说法正确的是
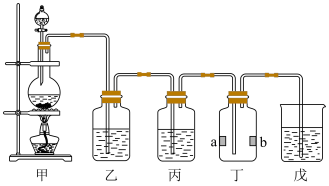
| A.上述装置用浓盐酸和MnO2反应制备Cl2,用向下排空气法收集 Cl2 |
| B.装置乙中为浓硫酸,装置丙中为NaOH溶液 |
| C.一段时间后,装置丁中a变蓝,反应的离子方程式为Cl2+2I-=I2+2Cl- |
| D.装置丁中b褪色,说明Cl2具有漂白性 |
您最近一年使用:0次
2024-01-27更新
|
86次组卷
|
2卷引用:广东省汕尾市2023-2024学年高一上学期期末教学质量监测化学试卷
名校
解题方法
6 . 部分含氯物质的分类与相应氯元素的化合价关系如图所示。下列说法不正确的是


| A.b→a一定需要加还原剂才能进行 | B.c可作为一种新型自来水消毒剂 |
| C.f→d可以通过加稀硫酸实现转化 | D.一定条件下a和f可能发生反应得到b |
您最近一年使用:0次
2024-01-25更新
|
106次组卷
|
2卷引用:广东省惠州市2023-2024学年高一上学期期末质量检测化学试题
22-23高一上·广东深圳·期末
名校
7 . 类推思维是化学学习中常用的一种方法,下列有关方程式的类推正确的是
A.Zn加入 溶液置换出Cu,Na加入 溶液置换出Cu,Na加入 溶液也置换出Cu 溶液也置换出Cu |
B.Fe与 点燃生成 点燃生成 ,则Fe与 ,则Fe与 点燃生成 点燃生成 |
C. 受热易分解, 受热易分解, 受热也易分解 受热也易分解 |
D. 通入 通入 产生白色沉淀, 产生白色沉淀, 通入 通入 也产生白色沉淀 也产生白色沉淀 |
您最近一年使用:0次
2024-01-25更新
|
109次组卷
|
7卷引用:广东省深圳中学2022-2023学年高一上学期期末考试化学试题
(已下线)广东省深圳中学2022-2023学年高一上学期期末考试化学试题(已下线)专项05 常见物质的性质、用途与转化-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)四川省绵阳市绵阳中学2023-2024学年高一上学期期末模拟测试化学试题云南省宣威市第六中学2023-2024学年高一上学期12月月考化学试题吉林省长春外国语学校2023-2024学年高一下学期开学化学试题吉林省通化市梅河口市第五中学2023-2024学年高一下学期开学化学试题江西省丰城市第九中学2023-2024学年高一下学期开学考试化学试题
名校
8 . “84消毒液”被广泛应用于物体表面杀菌消毒,化学兴趣小组设计了如图的实验装置制氯气探究氯气的性质并制备少量84消毒液:
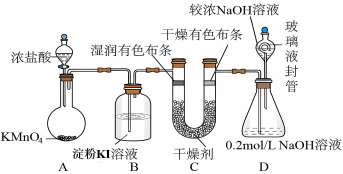
(1)盛放浓盐酸的仪器名称___________ ,酸性高锰酸钾作为强氧化剂其还原产物一般为Mn2+,装置A中反应的离子方程式是:___________ 。
(2)下列物质均可用于干燥气体,为了验证氯气是否具有漂白性,装置C应选择___________。
(3)装置D中的玻璃液封管中NaOH溶液的作用是___________ 。
(4)B装置可以观察到溶液开始变蓝后褪色,为探究其褪色的原因,取少许B溶液,滴加几滴碘水,溶液恢复蓝色,通过实验结果证明蓝色褪去的原因可能是___________ 。
(5)现在对锥形瓶中制备的消毒液进行定性和定量探究。
i.消毒液漂白性的探究,已知消毒液中起漂白作用的是HClO分子。
上述实验可以得到消毒液的漂白性强弱可能受___________ 影响。
ii.用Na2S2O3溶液和KI定量测定NaClO含量,其原理为: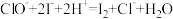 ;
; 。取20mL锥形瓶中的消毒液,加入过量的硫酸酸化的KI溶液,并加入几滴淀粉,再向溶液中逐滴加入0.2mol/L的Na2S2O3,当观察到
。取20mL锥形瓶中的消毒液,加入过量的硫酸酸化的KI溶液,并加入几滴淀粉,再向溶液中逐滴加入0.2mol/L的Na2S2O3,当观察到___________ 现象时,停止加入Na2S2O3。实验结束,测得共消耗20mLNa2S2O3,则计算消毒液中NaClO的浓度为___________ mol/L。

(1)盛放浓盐酸的仪器名称
(2)下列物质均可用于干燥气体,为了验证氯气是否具有漂白性,装置C应选择___________。
| A.浓硫酸 | B.碱石灰 | C.NaOH固体 | D.无水CaCl2 |
(3)装置D中的玻璃液封管中NaOH溶液的作用是
(4)B装置可以观察到溶液开始变蓝后褪色,为探究其褪色的原因,取少许B溶液,滴加几滴碘水,溶液恢复蓝色,通过实验结果证明蓝色褪去的原因可能是
(5)现在对锥形瓶中制备的消毒液进行定性和定量探究。
i.消毒液漂白性的探究,已知消毒液中起漂白作用的是HClO分子。
| 实验组 | 试剂 | 现象 |
| ① | 10mL消毒液+1mL蒸馏水+红色纸条 | 2min后纸条红色褪去 |
| ② | 10mL消毒液+1mL稀硫酸+红色纸条 | 30s后纸条红色褪去 |
| ③ | 10mL消毒液+1mL稀NaOH+红色纸条 | 2min后纸条红色稍变浅 |
ii.用Na2S2O3溶液和KI定量测定NaClO含量,其原理为:
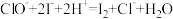 ;
; 。取20mL锥形瓶中的消毒液,加入过量的硫酸酸化的KI溶液,并加入几滴淀粉,再向溶液中逐滴加入0.2mol/L的Na2S2O3,当观察到
。取20mL锥形瓶中的消毒液,加入过量的硫酸酸化的KI溶液,并加入几滴淀粉,再向溶液中逐滴加入0.2mol/L的Na2S2O3,当观察到
您最近一年使用:0次
2024-01-24更新
|
109次组卷
|
2卷引用:广东省广州市三校(广附,铁一,广外)2023-2024学年高一上学期期末联考化学试题
9 . 氯元素是一种重要的“成盐元素”。部分含氯物质的分类与相应化合价关系如图所示。下列说法不正确 的是

| A.存在f→d→b的转化关系 | B.a溶液和f溶液混合可以制得b |
| C.d的稳定性差,其溶液久置即为a溶液 | D.b具有漂白性,能将湿润的有色布条褪色 |
您最近一年使用:0次
2024-01-22更新
|
70次组卷
|
2卷引用:广东省中山市2023-2024学年高一上学期期末考试化学试题
解题方法
10 . 化学与生活密切相关。下列说法不正确的是
A. 代替氯气用于自来水消毒 代替氯气用于自来水消毒 | B.纯碱常用作胃药 |
| C.不锈钢可用于制餐具 | D.放射性同位素可用于诊断和治疗疾病 |
您最近一年使用:0次
2024-01-22更新
|
77次组卷
|
2卷引用:广东省深圳市光明区2023-2024学年高一上学期期末考试化学试题