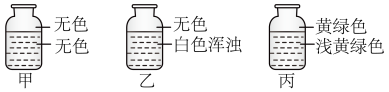
1 . 向盛有Cl2的三个集气瓶甲、乙、丙中各注入下列液体中的一种:
①AgNO3溶液、②NaOH溶液、③水,
经过振荡,现象如图所示,则甲、乙,丙中注入的液体分别是( )
①AgNO3溶液、②NaOH溶液、③水,
经过振荡,现象如图所示,则甲、乙,丙中注入的液体分别是( )

| A.①②③ | B.②①③ | C.③①② | D.①③② |
您最近一年使用:0次
2020-10-09更新
|
248次组卷
|
2卷引用:高一必修第一册(苏教2019)专题3 专题综合检测卷
2 . NaClO是84消毒液的有效成分。请回答下列问题。
(1)NaClO中Cl元素的化合价是______ 。
(2)用氢氧化钠溶液和氯气反应制备84消毒液,反应的离子方程式是_____ 。
(3)若将84消毒液与洁厕灵(通常含盐酸)混合使用,则会产生黄绿色的有毒气体,该反应的离子方程式是_________ 。
(1)NaClO中Cl元素的化合价是
(2)用氢氧化钠溶液和氯气反应制备84消毒液,反应的离子方程式是
(3)若将84消毒液与洁厕灵(通常含盐酸)混合使用,则会产生黄绿色的有毒气体,该反应的离子方程式是
您最近一年使用:0次
2020-09-23更新
|
310次组卷
|
2卷引用:鲁科版(2019)高一必修第一册第二章微项目 科学使用含氯消毒剂
3 . 市场上销售的某消毒液,其商标上有如下说明:①本产品为无色液体,呈弱碱性;②使用时,加水稀释;③可对餐具、衣服进行消毒,也可用于漂白浅色衣物。据此推断,该产品的有效成分可能是
| A.HClO | B.NaCl |
| C.NaClO | D.KMnO4 |
您最近一年使用:0次
2020-09-20更新
|
127次组卷
|
5卷引用:期末模拟卷(一)-2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)
(已下线)期末模拟卷(一)-2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)浙江省东阳中学2020-2021学年高一上学期期中考试化学试题浙江省瓯海中学2022-2023学年高一上学期10月月考化学试题新疆疏勒县第一中学等3校2022-2023学年高一上学期1月期末考试化学试题内蒙古自治区通辽市科尔沁左翼中旗实验高级中学2023-2024学年高一上学期1月期末化学试题
4 .  溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
(1)某同学设计如下实验研究 的性质:
的性质:
①理论上 既有氧化性又有还原性,具有还原性的原因是
既有氧化性又有还原性,具有还原性的原因是___________ 。
②能证明 具有还原性的是实验
具有还原性的是实验_________ (填序号)。
(2)84消毒液的有效成分为 。
。
①将 通入
通入 溶液中可制得84消毒液,化学方程式为
溶液中可制得84消毒液,化学方程式为_________ 。
②84消毒液不能用于钢制器具的消毒,原因是 具有
具有_______ 性。
③84消毒液吸收空气中的 ,其消毒杀菌能力增强,该过程中发生反应的化学方程式为
,其消毒杀菌能力增强,该过程中发生反应的化学方程式为______ 。
 溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:(1)某同学设计如下实验研究
 的性质:
的性质:| 实验 | 操作 | 现象 |
| i | 向5% 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ii | 向5% 溶液中滴加淀粉碘化钾溶液 溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
①理论上
 既有氧化性又有还原性,具有还原性的原因是
既有氧化性又有还原性,具有还原性的原因是②能证明
 具有还原性的是实验
具有还原性的是实验(2)84消毒液的有效成分为
 。
。①将
 通入
通入 溶液中可制得84消毒液,化学方程式为
溶液中可制得84消毒液,化学方程式为②84消毒液不能用于钢制器具的消毒,原因是
 具有
具有③84消毒液吸收空气中的
 ,其消毒杀菌能力增强,该过程中发生反应的化学方程式为
,其消毒杀菌能力增强,该过程中发生反应的化学方程式为
您最近一年使用:0次
名校
解题方法
5 . (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有湿润有色布条的广口瓶,可观察到的现象是___ 。
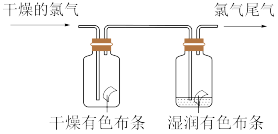
(2)为防止氯气尾气污染空气,实验室通常用____ 溶液吸收多余的氯气,原理是(用化学方程式表示)_______ 。长期露置于空气中的漂白粉,加稀盐酸后产生的气体是_____ (用字母代号填)。
A. O2 B. Cl2 C. CO2 D. HClO

(2)为防止氯气尾气污染空气,实验室通常用
A. O2 B. Cl2 C. CO2 D. HClO
您最近一年使用:0次
6 . 同学们探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验。
步骤1:将5mL市售84消毒液稀释100倍,测得稀释后溶液的 ;
;
步骤2:将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中;
步骤3:用 溶液将a、b、c三个烧杯内溶液的pH分别调至10、7和4。(溶液体积变化忽略不计)
溶液将a、b、c三个烧杯内溶液的pH分别调至10、7和4。(溶液体积变化忽略不计)
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下。
已知溶液中 、HClO、和
、HClO、和 的物质的量分数(α)随溶液pH变化的关系如图所示:
的物质的量分数(α)随溶液pH变化的关系如图所示:
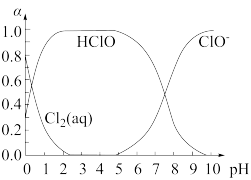
(1)由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色_______ (填“越快”或“越慢”)。
(2)结合图象进行分析,b、c两烧杯中实验现象出现差异的原因是_________ 。
步骤1:将5mL市售84消毒液稀释100倍,测得稀释后溶液的
 ;
;步骤2:将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中;
步骤3:用
 溶液将a、b、c三个烧杯内溶液的pH分别调至10、7和4。(溶液体积变化忽略不计)
溶液将a、b、c三个烧杯内溶液的pH分别调至10、7和4。(溶液体积变化忽略不计)步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下。
| 烧杯 | 溶液的pH | 现象 |
| a | 10 | 10min后,红纸基本不褪色;4h后红纸褪色 |
| b | 7 | 10min后,红纸颜色变浅;4h后红纸褪色 |
| c | 4 | 10min后,红纸颜色比b烧杯中10min后的浅;4h后红纸褪色 |
已知溶液中
 、HClO、和
、HClO、和 的物质的量分数(α)随溶液pH变化的关系如图所示:
的物质的量分数(α)随溶液pH变化的关系如图所示:
(1)由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色
(2)结合图象进行分析,b、c两烧杯中实验现象出现差异的原因是
您最近一年使用:0次
2020-09-14更新
|
136次组卷
|
2卷引用:鲁科版(2019)高一必修第一册第二章微项目 科学使用含氯消毒剂
解题方法
7 . 已知漂白粉溶于水后加入少量的酸能增强漂白效果。某同学据此将少量漂白粉溶于水后,再加入浓盐酸,观察到有黄绿色气体生成。回答下列问题:
(1)写出生成黄绿色气体的化学方程式:_________________________________ 。
(2)家庭生活中常使用“84”消毒液进行消毒。这种消毒液和某品牌洁厕净(主要成分为盐酸)________ (填“能”或“不能”)同时使用,其原因是________ 。
(3)现设计实验由大理石、水、氯气来制取漂白粉:大理石

 漂白粉溶液
漂白粉溶液 漂白粉,请写出在制取漂白粉的实验过程中发生的化学方程式:
漂白粉,请写出在制取漂白粉的实验过程中发生的化学方程式:_______________________ 。
(1)写出生成黄绿色气体的化学方程式:
(2)家庭生活中常使用“84”消毒液进行消毒。这种消毒液和某品牌洁厕净(主要成分为盐酸)
(3)现设计实验由大理石、水、氯气来制取漂白粉:大理石


 漂白粉溶液
漂白粉溶液 漂白粉,请写出在制取漂白粉的实验过程中发生的化学方程式:
漂白粉,请写出在制取漂白粉的实验过程中发生的化学方程式:
您最近一年使用:0次
名校
8 . 抗震救灾中要用大量漂白粉和漂白液杀菌消毒。下列说法正确的是( )
A.漂白粉的有效成分是 |
B.漂白液的有效成分是 |
| C.新制氯水是比漂白粉、漂白液稳定的漂白剂 |
| D.工业上制漂白粉的方法是将氯气通入澄清石灰水中 |
您最近一年使用:0次
2020-09-05更新
|
413次组卷
|
5卷引用:人教版(2019)高一必修第一册第二章 海水中的重要元素 第二节 氯及其化合物 课时1 氯气的性质
名校
解题方法
9 . 肼(N2H4)是氮和氢形成的一种化合物,易溶于水。工业上利用尿素法生产肼,同时得到副产品十水合碳酸钠,其工艺流程如图:
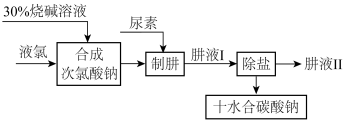
制肼过程的反应为:CO(NH2)2(尿素)+NaClO+2NaOH=N2H4+Na2CO3+NaCl+H2O
(1)实验室若配制30%烧碱溶液,所需的玻璃仪器除玻璃棒外,还有______ (填标号)。
A.漏斗 B.烧杯 C.烧瓶 D.量筒
(2)已知:Cl2+H2O=HCl+HClO,请推测C12与NaOH溶液发生反应的化学方程式:____ 。从后续反应过程来看,若要使原料不浪费,合成次氯酸钠时投入的液氯与烧碱的质量之比为71:_________ 。
(3)实验室中,欲从母液中分离出十水合碳酸钠晶体。可采用的操作依次为________ 。(填标号)
A.蒸馏 B.蒸发 C.灼烧 D.过滤 E.冷却结晶
(4)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧等。请写出肼除氧时发生反应的化学方程式:______________ 。

制肼过程的反应为:CO(NH2)2(尿素)+NaClO+2NaOH=N2H4+Na2CO3+NaCl+H2O
(1)实验室若配制30%烧碱溶液,所需的玻璃仪器除玻璃棒外,还有
A.漏斗 B.烧杯 C.烧瓶 D.量筒
(2)已知:Cl2+H2O=HCl+HClO,请推测C12与NaOH溶液发生反应的化学方程式:
(3)实验室中,欲从母液中分离出十水合碳酸钠晶体。可采用的操作依次为
A.蒸馏 B.蒸发 C.灼烧 D.过滤 E.冷却结晶
(4)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧等。请写出肼除氧时发生反应的化学方程式:
您最近一年使用:0次
2020-08-16更新
|
437次组卷
|
2卷引用:甘肃省庆阳第一中学2018-2019学年高一上学期开学考试化学试题



