解题方法
1 . 氯的含氧酸盐具有较强的氧化性,能够杀菌消毒,在预防新冠疫情中起到重要作用。某化学兴趣小组用氯气和相应的碱溶液反应制取NaClO和 ,制备装置如图所示(部分加持仪器略去),并研究
,制备装置如图所示(部分加持仪器略去),并研究 的氧化性。已知:氯气与碱反应,温度较高时生成
的氧化性。已知:氯气与碱反应,温度较高时生成 ,温度较低时生成
,温度较低时生成 。
。

(1)盛装浓盐酸的仪器名称是_______ 。
(2)装置A烧瓶中反应的化学方程式为_______ 。
(3)装置C中 与试剂a反应的离子方程式为
与试剂a反应的离子方程式为_______ 。
(4)如果缺少装置B,对制取NaClO和 的影响是
的影响是_______ 。
(5)E中可选用试剂有_______ (填标号)。
A.饱和 溶液 B.浓
溶液 B.浓 C.饱和NaCl溶液 D.NaOH溶液
C.饱和NaCl溶液 D.NaOH溶液
(6)该小组在探究 氧化性时,发现
氧化性时,发现 与
与 的反应速率先增大后减小,反应为
的反应速率先增大后减小,反应为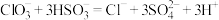 。小组分析认为,反应生成的离子可能对反应速率产生影响。为了探究
。小组分析认为,反应生成的离子可能对反应速率产生影响。为了探究 对化学反应速率的影响,设计如下实验:
对化学反应速率的影响,设计如下实验:
该实验_______ (填“能”或“不能”)达到实验目的,理由是_______ 。
 ,制备装置如图所示(部分加持仪器略去),并研究
,制备装置如图所示(部分加持仪器略去),并研究 的氧化性。已知:氯气与碱反应,温度较高时生成
的氧化性。已知:氯气与碱反应,温度较高时生成 ,温度较低时生成
,温度较低时生成 。
。
(1)盛装浓盐酸的仪器名称是
(2)装置A烧瓶中反应的化学方程式为
(3)装置C中
 与试剂a反应的离子方程式为
与试剂a反应的离子方程式为(4)如果缺少装置B,对制取NaClO和
 的影响是
的影响是(5)E中可选用试剂有
A.饱和
 溶液 B.浓
溶液 B.浓 C.饱和NaCl溶液 D.NaOH溶液
C.饱和NaCl溶液 D.NaOH溶液(6)该小组在探究
 氧化性时,发现
氧化性时,发现 与
与 的反应速率先增大后减小,反应为
的反应速率先增大后减小,反应为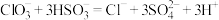 。小组分析认为,反应生成的离子可能对反应速率产生影响。为了探究
。小组分析认为,反应生成的离子可能对反应速率产生影响。为了探究 对化学反应速率的影响,设计如下实验:
对化学反应速率的影响,设计如下实验:| 实验序号 | 温度 |  | 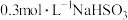 |  盐酸 盐酸 |  |
| ① | 25℃ | 10mL | 10mL | 0mL | 1mL |
| ② | 25℃ | 10mL | 10mL | 1mL | 0mL |
您最近一年使用:0次
2021-06-17更新
|
401次组卷
|
2卷引用:河南省郑州市2020-2021学年高一下学期期末考试化学试题
名校
解题方法
2 . “84消毒液”广泛应用于杀菌消毒,其有效成分是NaClO。实验小组制备消毒液,并利用其性质探索制备碘水的方法。
资料:i.HClO的电离常数为Ka=4.7×10-8;
H2CO3的电离常数为K1=4.3×10-7、K2=5.6×10-11。
ii.碘的化合物主要以I-和IO3-的形式存在,IO3-+5I-+6H+=3I2+3H2O。
iii.碘单质能与I-反应:I2+I- I3-(I3-低浓度时显黄色,高浓度时为棕色)。
I3-(I3-低浓度时显黄色,高浓度时为棕色)。
Ⅰ.制备消毒液(夹持装置略)
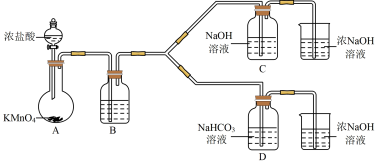
(1)制备NaClO消毒液的装置是__________ (填C或D)。
(2)制备完成后,向C装置的溶液中添加NaOH、Na2SiO3等物质,得到与某品牌成分相同的消毒液,用平衡移动原理解释NaOH的作用___________________ 。
(3)结合资料i,写出D中反应的化学方程式______________________ 。
Ⅱ.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
(4)对比不同方案的实验现象,得出制取碘水的最佳方法要关注的因素是________ 。
(5)针对烧杯3“滴加淀粉溶液不变蓝”的原因,提出两种假设:
假设1:过量的NaClO将反应生成的I2氧化为IO3-。
设计实验证实了假设1成立。NaClO氧化I2生成IO3-的离子方程式是_____________ 。
假设2:生成的I2在碱性溶液中不能存在。
设计实验a证实了假设2成立,实验a的操作及现象是______________________ 。
(6)某小组检验烧杯3所得溶液中含IO3-:取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在IO3-,说明理由______________________ 。
(7)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据________ 。
资料:i.HClO的电离常数为Ka=4.7×10-8;
H2CO3的电离常数为K1=4.3×10-7、K2=5.6×10-11。
ii.碘的化合物主要以I-和IO3-的形式存在,IO3-+5I-+6H+=3I2+3H2O。
iii.碘单质能与I-反应:I2+I-
 I3-(I3-低浓度时显黄色,高浓度时为棕色)。
I3-(I3-低浓度时显黄色,高浓度时为棕色)。Ⅰ.制备消毒液(夹持装置略)

(1)制备NaClO消毒液的装置是
(2)制备完成后,向C装置的溶液中添加NaOH、Na2SiO3等物质,得到与某品牌成分相同的消毒液,用平衡移动原理解释NaOH的作用
(3)结合资料i,写出D中反应的化学方程式
Ⅱ.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
| 方案 | 操作 | 现象 | 反应后加淀粉溶液 |
| 1 | 烧杯1溶液中加入9gKI固体 | 溶液为橙黄色 | …… |
| 2 | 烧杯2溶液中加入9gKI固体再加入1mo/L盐酸10mL | 溶液颜色快速加深,呈紫红色 | 变蓝 |
| 3 | 烧杯3溶液中加入少量KI固体(小于0.5g) | 振荡后溶液保持无色 | 不变蓝 |
(5)针对烧杯3“滴加淀粉溶液不变蓝”的原因,提出两种假设:
假设1:过量的NaClO将反应生成的I2氧化为IO3-。
设计实验证实了假设1成立。NaClO氧化I2生成IO3-的离子方程式是
假设2:生成的I2在碱性溶液中不能存在。
设计实验a证实了假设2成立,实验a的操作及现象是
(6)某小组检验烧杯3所得溶液中含IO3-:取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在IO3-,说明理由
(7)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据
您最近一年使用:0次
2020-05-07更新
|
449次组卷
|
4卷引用:北京市石景山区2020届高三第一次模拟化学试题
北京市石景山区2020届高三第一次模拟化学试题(已下线)北京市2019-2020学年高三各区一模化学考试分类汇编:科学探究北京首都师范大学附属中学2022届高三下学期三模化学试题北京市第八十中学2024届高三上学期10月月考化学试题
解题方法
3 . 含氯消毒剂有多种,二氧化氯可用于自来水消毒,84消毒液用于家庭、宾馆的消毒。
I.实验室可用亚氯酸钠固体与应制备ClO2:2NaClO2+Cl2=2ClO2+2NaCl,装置如图所示:
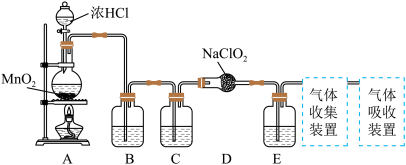
(1)装置A中,盛装浓盐酸的仪器名称为___ ,开始反应后,圆底烧瓶内发生的反应的离子反应方程式为:__ 。
(2)已知常温常压下,ClO2和Cl2是气体,在不同溶剂中溶解性如表所示:B、C、E装置中的试剂依次是___ (填编号)
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.CCl4
(3)使用ClO2在给自来水消毒的过程中会产生有害的副产物亚氯酸根(ClO2-),可用Fe2+将其去除。已知ClO2-与Fe2+在pH=5~7的条件下能快速反应,最终形成红褐色沉淀,而ClO2-则被还原成Cl-。Fe2+消除ClO2-的离子方程式为__ 。
II.某同学在家中自制出与“84消毒液”成分(NaClO和水)相同的消毒液。主要器材有6V变压器、两支木杆铅笔、废纯净水瓶、食盐、卫生纸、绝缘胶布、小刀等。
(4)实验过程:向一个废弃的纯净水瓶中灌入大半瓶自来水,并加入3调味匙食盐,用卫生纸将用铅笔做成的电极包好,并插入纯净水瓶中,使电极恰好卡在瓶口,装置如图,接通电源后,可以看到一侧电极无明显现象,另一侧电极有细小的气泡产生,请写出该电极反应式为:___ ;持续通电约3小时后,发现原先无明显现象的电极附近也开始产生一定量的细小气泡,此电极此时的电极反应式___ 。看到该现象后停止通电。

(5)用该方法制备消毒液的总化学方程式是:___ 。
I.实验室可用亚氯酸钠固体与应制备ClO2:2NaClO2+Cl2=2ClO2+2NaCl,装置如图所示:

(1)装置A中,盛装浓盐酸的仪器名称为
(2)已知常温常压下,ClO2和Cl2是气体,在不同溶剂中溶解性如表所示:B、C、E装置中的试剂依次是
| ClO2 | Cl2 | |
| 水 | 极易溶于水 | 溶 |
| CCl4 | 难溶 | 易溶 |
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.CCl4
(3)使用ClO2在给自来水消毒的过程中会产生有害的副产物亚氯酸根(ClO2-),可用Fe2+将其去除。已知ClO2-与Fe2+在pH=5~7的条件下能快速反应,最终形成红褐色沉淀,而ClO2-则被还原成Cl-。Fe2+消除ClO2-的离子方程式为
II.某同学在家中自制出与“84消毒液”成分(NaClO和水)相同的消毒液。主要器材有6V变压器、两支木杆铅笔、废纯净水瓶、食盐、卫生纸、绝缘胶布、小刀等。
(4)实验过程:向一个废弃的纯净水瓶中灌入大半瓶自来水,并加入3调味匙食盐,用卫生纸将用铅笔做成的电极包好,并插入纯净水瓶中,使电极恰好卡在瓶口,装置如图,接通电源后,可以看到一侧电极无明显现象,另一侧电极有细小的气泡产生,请写出该电极反应式为:

(5)用该方法制备消毒液的总化学方程式是:
您最近一年使用:0次
解题方法
4 . 实验室模拟工业提镁,其相关原理或装置能达到相应实验目的的是
A.制HCl气体 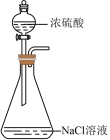 | B.干燥HCl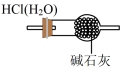 |
C.制无水  | D.电解 尾气处理 尾气处理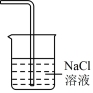 |
您最近一年使用:0次
名校
解题方法
5 . 叠氮化钠( )不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼(
)不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼( )并利用其进一步反应制取
)并利用其进一步反应制取 的流程如下:
的流程如下:
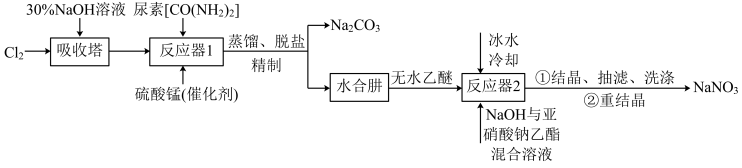
已知:① 易溶于水,具有强还原性,易被氧化成
易溶于水,具有强还原性,易被氧化成 ;
;
②一定条件下,碱性NaClO溶液与尿素溶液反应生成 。
。
回答下列问题:
(1)吸收塔内发生反应的离子方程式为_______ 。
(2)写出反应器1中生成水合肼反应的化学方程式:_______ 。
(3)反应器2中加入无水乙醚的作用是_______ 。
(4)已知亚硝酸乙酯的结构简式为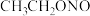 ,反应器2中生成
,反应器2中生成 和
和 。若生成39g
。若生成39g  ,则该反应中转移电子的物质的量为
,则该反应中转移电子的物质的量为_______ 。
(5)反应器1要控制NaClO溶液的用量,其主要目的是_______ 。
(6)某实验室设计了如图所示装置制备 。双极膜是阴、阳复合膜,层间的
。双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。
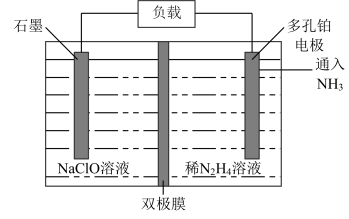
①双极膜中产生的_______ (填“ ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。
②石墨电极反应式为_______ 。
 )不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼(
)不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼( )并利用其进一步反应制取
)并利用其进一步反应制取 的流程如下:
的流程如下:
已知:①
 易溶于水,具有强还原性,易被氧化成
易溶于水,具有强还原性,易被氧化成 ;
;②一定条件下,碱性NaClO溶液与尿素溶液反应生成
 。
。回答下列问题:
(1)吸收塔内发生反应的离子方程式为
(2)写出反应器1中生成水合肼反应的化学方程式:
(3)反应器2中加入无水乙醚的作用是
(4)已知亚硝酸乙酯的结构简式为
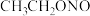 ,反应器2中生成
,反应器2中生成 和
和 。若生成39g
。若生成39g  ,则该反应中转移电子的物质的量为
,则该反应中转移电子的物质的量为(5)反应器1要控制NaClO溶液的用量,其主要目的是
(6)某实验室设计了如图所示装置制备
 。双极膜是阴、阳复合膜,层间的
。双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。
①双极膜中产生的
 ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。②石墨电极反应式为
您最近一年使用:0次
解题方法
6 . 高铁酸盐是优良的多功能水处理剂。 为紫色固体,可溶于水,微溶于KOH浓溶液,难溶于有机物;在
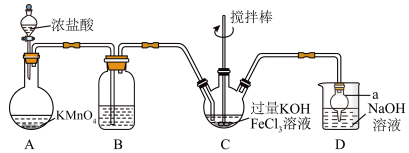
为紫色固体,可溶于水,微溶于KOH浓溶液,难溶于有机物;在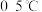 的强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出
的强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出 。某实验小组制备高铁酸钾
。某实验小组制备高铁酸钾 的装置如图所示。
的装置如图所示。
回答下列问题:
(1)仪器a的名称为_______ 。
(2)装置A中发生反应的离子方程式为_______ 。
(3)装置B中盛放的试剂为饱和氯化钠溶液,主要作用是除去挥发出来的氯化氢气体,还有一个作用是_______ 。
(4)装置C中生成 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为_______ 。C中混合物经重结晶、有机物洗涤纯化、真空干燥,得到高铁酸钾晶体。
(5)装置D中尾气处理时,除了生成 、
、 外,还有可能生成
外,还有可能生成_______ (填化学式)。
(6)往装有一定量的 晶体的试管中滴入稀硫酸,振荡。
晶体的试管中滴入稀硫酸,振荡。
①写出其发生反应的离子方程式:_______ 。
②检验生成气体为氧气的方法是_______ 。
 为紫色固体,可溶于水,微溶于KOH浓溶液,难溶于有机物;在
为紫色固体,可溶于水,微溶于KOH浓溶液,难溶于有机物;在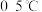 的强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出
的强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出 。某实验小组制备高铁酸钾
。某实验小组制备高铁酸钾 的装置如图所示。
的装置如图所示。
回答下列问题:
(1)仪器a的名称为
(2)装置A中发生反应的离子方程式为
(3)装置B中盛放的试剂为饱和氯化钠溶液,主要作用是除去挥发出来的氯化氢气体,还有一个作用是
(4)装置C中生成
 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为(5)装置D中尾气处理时,除了生成
 、
、 外,还有可能生成
外,还有可能生成(6)往装有一定量的
 晶体的试管中滴入稀硫酸,振荡。
晶体的试管中滴入稀硫酸,振荡。①写出其发生反应的离子方程式:
②检验生成气体为氧气的方法是
您最近一年使用:0次
2022-05-01更新
|
226次组卷
|
3卷引用:云南省名校联盟2021-2022学年高二下学期期中考试化学(B1)试题
名校
解题方法
7 . 二氯异氰尿酸钠(NaC3N3O3Cl2)是一种高效广谱杀菌消毒剂,它常温下为白色固体,难溶于冷水。其制备原理为: 。请选择下列部分装置制备二氯异氰尿酸钠并探究其性质。
。请选择下列部分装置制备二氯异氰尿酸钠并探究其性质。
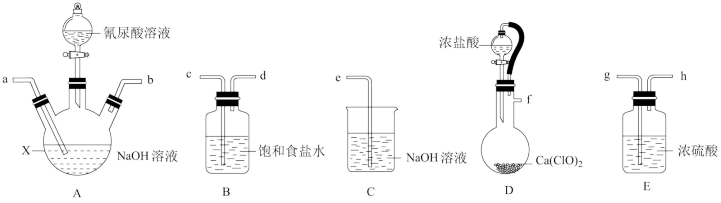
请回答下列问题:
(1)仪器X的名称是___________ 。
(2)装置B的作用是___________ 。
(3)D中发生反应的化学方程式为___________ 。
(4)选择合适装置,按气流从左至右,导管连接顺序为___________ (填字母)。
(5)实验时,先向A中通入氯气,生成高浓度的 溶液后,再加入氰尿酸溶液,并在整个过程中不断通入一定量的氯气,其原因是
溶液后,再加入氰尿酸溶液,并在整个过程中不断通入一定量的氯气,其原因是___________ 。
(6)反应结束后,A中浊液经过滤、___________ 、___________ 得到粗产品mg。
(7)粗产品中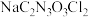 含量测定。将mg粗产品溶于无氧蒸馏水中配制成100mL溶液,取20.00mL所配制溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min。用
含量测定。将mg粗产品溶于无氧蒸馏水中配制成100mL溶液,取20.00mL所配制溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min。用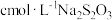 标准溶液进行滴定,加入指示剂,滴定至终点,消耗
标准溶液进行滴定,加入指示剂,滴定至终点,消耗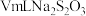 溶液。(假设杂质不与
溶液。(假设杂质不与 反应,涉及的反应为:
反应,涉及的反应为: ,
, )
)
①加入的指示剂是___________ 。
②则 的百分含量为
的百分含量为___________  。(用含m,c,V的代数式表示)
。(用含m,c,V的代数式表示)
 。请选择下列部分装置制备二氯异氰尿酸钠并探究其性质。
。请选择下列部分装置制备二氯异氰尿酸钠并探究其性质。
请回答下列问题:
(1)仪器X的名称是
(2)装置B的作用是
(3)D中发生反应的化学方程式为
(4)选择合适装置,按气流从左至右,导管连接顺序为
(5)实验时,先向A中通入氯气,生成高浓度的
 溶液后,再加入氰尿酸溶液,并在整个过程中不断通入一定量的氯气,其原因是
溶液后,再加入氰尿酸溶液,并在整个过程中不断通入一定量的氯气,其原因是(6)反应结束后,A中浊液经过滤、
(7)粗产品中
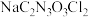 含量测定。将mg粗产品溶于无氧蒸馏水中配制成100mL溶液,取20.00mL所配制溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min。用
含量测定。将mg粗产品溶于无氧蒸馏水中配制成100mL溶液,取20.00mL所配制溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min。用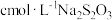 标准溶液进行滴定,加入指示剂,滴定至终点,消耗
标准溶液进行滴定,加入指示剂,滴定至终点,消耗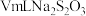 溶液。(假设杂质不与
溶液。(假设杂质不与 反应,涉及的反应为:
反应,涉及的反应为: ,
, )
)①加入的指示剂是
②则
 的百分含量为
的百分含量为 。(用含m,c,V的代数式表示)
。(用含m,c,V的代数式表示)
您最近一年使用:0次
2022-01-23更新
|
1064次组卷
|
4卷引用:重庆市2022届高三第一次联合诊断测试化学试题
重庆市2022届高三第一次联合诊断测试化学试题重庆市天星桥中学2021-2022学年高三下学期学业质量调研抽测化学试题(已下线)专项14 化学实验综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)黑龙江省哈尔滨市第九中学校2022届高考最后押题卷(一)化学试题
8 . 某小组以电石渣[主要成分为 和
和 ]为原料制备
]为原料制备 晶体,流程如下:
晶体,流程如下:
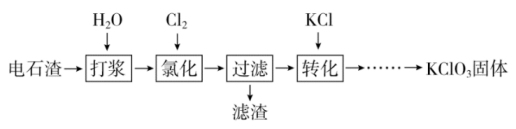
已知:氯化时 与
与 反应生成
反应生成 ,
, 进一步转化生成
进一步转化生成 ,少量
,少量 分解生成
分解生成 和
和 。请回答:
。请回答:
(1)氯化时装置如图所示,B中的试剂是___________ ;若C中导管处堵塞则B中的现象是___________ 。
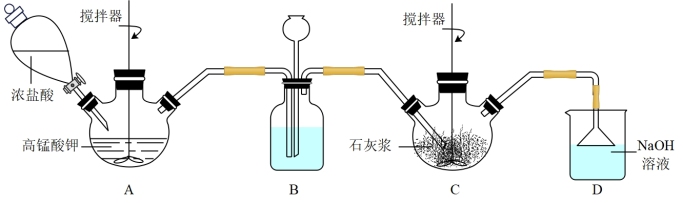
(2)下列说法不正确 的是___________ 。
A.打浆时加水形成石灰浆的目的是使 与
与 充分反应
充分反应
B.氯化时应快速通入氯气以提高氯气的转化率
C.过滤得到的滤渣中含有 、
、
D.过滤后的滤液中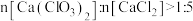
(3)对抽滤后获得的 晶体进行洗涤的方法是
晶体进行洗涤的方法是___________ 。
(4)某小组认为获得的 产品中含有KCl、
产品中含有KCl、 两种物质,为测定
两种物质,为测定 的含量,从下列选项中选出合理的操作(操作可以重复使用)并排序:称取mg样品→用蒸馏水溶解→___________→___________→___________→___________→___________→___________→计算,
的含量,从下列选项中选出合理的操作(操作可以重复使用)并排序:称取mg样品→用蒸馏水溶解→___________→___________→___________→___________→___________→___________→计算,___________
a.往滤液中加入足量的 、
、 溶液b.过滤、洗涤
溶液b.过滤、洗涤
c.干燥、称量d.加入足量的 、
、 溶液
溶液
(5)该小组用上述方法测得 产品中
产品中 的质量分数为72.0%,高于理论值。可能原因是
的质量分数为72.0%,高于理论值。可能原因是___________ 。
 和
和 ]为原料制备
]为原料制备 晶体,流程如下:
晶体,流程如下:
已知:氯化时
 与
与 反应生成
反应生成 ,
, 进一步转化生成
进一步转化生成 ,少量
,少量 分解生成
分解生成 和
和 。请回答:
。请回答:(1)氯化时装置如图所示,B中的试剂是

(2)下列说法
A.打浆时加水形成石灰浆的目的是使
 与
与 充分反应
充分反应B.氯化时应快速通入氯气以提高氯气的转化率
C.过滤得到的滤渣中含有
 、
、
D.过滤后的滤液中
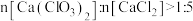
(3)对抽滤后获得的
 晶体进行洗涤的方法是
晶体进行洗涤的方法是(4)某小组认为获得的
 产品中含有KCl、
产品中含有KCl、 两种物质,为测定
两种物质,为测定 的含量,从下列选项中选出合理的操作(操作可以重复使用)并排序:称取mg样品→用蒸馏水溶解→___________→___________→___________→___________→___________→___________→计算,
的含量,从下列选项中选出合理的操作(操作可以重复使用)并排序:称取mg样品→用蒸馏水溶解→___________→___________→___________→___________→___________→___________→计算,a.往滤液中加入足量的
 、
、 溶液b.过滤、洗涤
溶液b.过滤、洗涤c.干燥、称量d.加入足量的
 、
、 溶液
溶液(5)该小组用上述方法测得
 产品中
产品中 的质量分数为72.0%,高于理论值。可能原因是
的质量分数为72.0%,高于理论值。可能原因是
您最近一年使用:0次



