1 . 氮是自然界各种生物体生命活动不可缺少的重要元素,下列物质均含氮元素,回答下列问题:
(1)写出反应①的化学方程式___________ ;
(2)B在催化剂作用下生成C是工业制硝酸的基础,写出反应②的化学方程式___________ ;
(3)工业上用水吸收气体D生产硝酸,写出反应⑤的化学方程式___________ ,若生成标况下的C气体33.6L,转移电子数目为___________ .
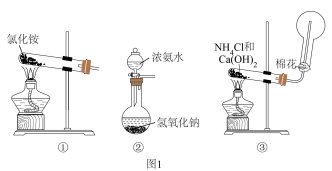
(4)从下图1的装置中选择一个可制备B气体的方法___________ ,并写出对应的化学方程式___________ . ___________ ,硝酸的浓度是___________ 。

(1)写出反应①的化学方程式
(2)B在催化剂作用下生成C是工业制硝酸的基础,写出反应②的化学方程式
(3)工业上用水吸收气体D生产硝酸,写出反应⑤的化学方程式
(4)从下图1的装置中选择一个可制备B气体的方法
您最近一年使用:0次
2024-04-30更新
|
125次组卷
|
2卷引用:四川省成都市安宁河联盟2023-2024学年高一下学期期中联考化学试题
2 . 某化学兴趣小组为了制取氨气并探究其性质,按下列装置(部分夹持装置已略去)进行实验。___________ 。
(2)若氨气的发生装置选择b,则所用的试剂为___________ 和___________ 。
(3)B装置中的干燥剂可选用___________ :实验中观察到C装置中的现象是___________ 。
(4)当实验进行一段时间后,挤压D装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是___________ ,E中倒扣漏斗的作用是___________ 。
(5)氨气(NH3)是一种重要的化工原料,其中约80%用来生产各种氮肥。其中利用NH3生产NH4NO3的主要转化途径如图(转化所需试剂及条件已略去):
NH3→NO→NO2→HNO3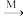 NH4NO3
NH4NO3
①NH3→NO的化学方程为___________ 。
②NO2→HNO3的化学方程式为___________ 。
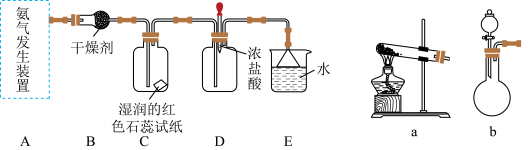
(2)若氨气的发生装置选择b,则所用的试剂为
(3)B装置中的干燥剂可选用
(4)当实验进行一段时间后,挤压D装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(5)氨气(NH3)是一种重要的化工原料,其中约80%用来生产各种氮肥。其中利用NH3生产NH4NO3的主要转化途径如图(转化所需试剂及条件已略去):
NH3→NO→NO2→HNO3
 NH4NO3
NH4NO3①NH3→NO的化学方程为
②NO2→HNO3的化学方程式为
您最近一年使用:0次
2023-07-28更新
|
294次组卷
|
4卷引用:期中测试卷二【测试范围:第五、六章】-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
(已下线)期中测试卷二【测试范围:第五、六章】-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)辽宁省六校协作体2022-2023学年高一下学期期末考试化学试题(已下线)重难点02 常见物质的制取与性质探究-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)(已下线)专题01 硫、氮及其化合物 无机非金属材料-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)
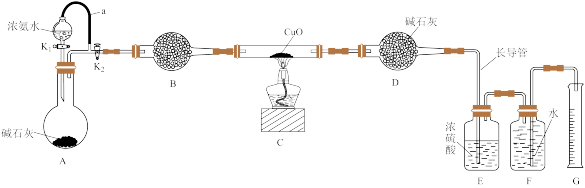
3 . 氨气与灼热氧化铜反应生成铜、氮气和水。实验小组选用如图所示装置测定氨分子的组成(夹持、固定装置均略去)。
(1)实验开始后,应该先___________ (填实验操作),一段时间后再点燃酒精灯,装置C玻璃管中发生反应的化学方程式为___________ 。
(2)装置A中盛装浓氨水的仪器名称为___________ ;橡皮管a的作用是___________ 。
(3)装置E中长导管的作用是___________ 。
(4)实验结束后,G读数折算成标准状况下的气体体积为 ,称得干燥管D增重mg,则氨分子中氮、氢的原子个数比为
,称得干燥管D增重mg,则氨分子中氮、氢的原子个数比为___________ (用含V、m的代数式表示);有同学认为装置E可以省略不用,试分析若不用装置E,测得结果会___________ (“偏大”、“偏小”或“无影响”)。
(1)实验开始后,应该先
(2)装置A中盛装浓氨水的仪器名称为
(3)装置E中长导管的作用是
(4)实验结束后,G读数折算成标准状况下的气体体积为
 ,称得干燥管D增重mg,则氨分子中氮、氢的原子个数比为
,称得干燥管D增重mg,则氨分子中氮、氢的原子个数比为
您最近一年使用:0次
2023-01-14更新
|
558次组卷
|
5卷引用:专题02 氮及其化合物的性质及转化(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)
(已下线)专题02 氮及其化合物的性质及转化(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)(已下线)化学(人教版2019B卷)-学易金卷:2022-2023学年高一下学期期中考前必刷卷(已下线)猜想03 气体的制取、无机实验探究、无机综合应用(考题猜想)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)(已下线)猜想02 氮及其化合物的性质与转化(考题猜想)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)山东省潍坊市安丘市2022-2023学年高一上学期期末考试化学试题
名校
4 . 研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价-物质类别关系图如图
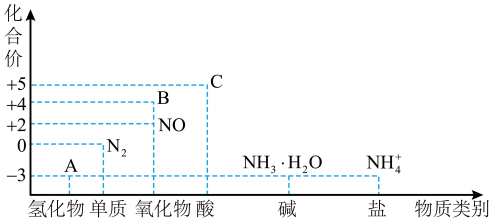
回答下列问题:
(1)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是_______ 。
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:_______ 。
(3)实验室中,检验溶液中含有N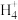 的操作方法是
的操作方法是_______ 。
(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:_______ ,当反应消耗0.15 mol物质B时,转移电子的物质的量为_______ 。

回答下列问题:
(1)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:
(3)实验室中,检验溶液中含有N
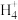 的操作方法是
的操作方法是(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:
您最近一年使用:0次
2021-06-08更新
|
701次组卷
|
12卷引用:专题02 氮及其化合物的性质及转化(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)
(已下线)专题02 氮及其化合物的性质及转化(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)黑龙江省牡丹江市海林市朝鲜族中学2020-2021学年高一5月月考化学试题(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点11 氮及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)3.3.2 氮循环-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)第四章 非金属及其化合物 第23讲 硝酸 含氮化合物的转化关系(已下线)考点11 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第6讲 硝酸 含氮化合物之间的转化湖南省湘楚名校2023-2024学年高一下学期期中考试化学试题(已下线)猜想03 气体的制取、无机实验探究、无机综合应用(考题猜想)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)山东省济宁市微山县第二中学2023-2024学年高一下学期第一次月考化学试题
11-12高一下·山东济宁·阶段练习
名校
解题方法
5 . 某化学实验小组同学利用一下装置制备氨气,并探究氨气的性质(部分仪器已略去)

请回答:
(1)实验室制备氨气的化学方程式为__________________________________________________ ;
干燥氨气常用的干燥剂是_______________ 。
(2)收集氨气时,请你选择氨气的进气口_________ (填“a”或“b”),
理由是________________________________________________________________ 。
(3)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是_______ ;________________________________ 。
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是____________________ (填序号)。

(5)氨气在催化剂并且加热时会被空气氧化,这是工业制硝酸的第一步反应,写出该反应的化学方程式___________________________________________________ 。

请回答:
(1)实验室制备氨气的化学方程式为
干燥氨气常用的干燥剂是
(2)收集氨气时,请你选择氨气的进气口
理由是
(3)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是

(5)氨气在催化剂并且加热时会被空气氧化,这是工业制硝酸的第一步反应,写出该反应的化学方程式
您最近一年使用:0次
2017-07-23更新
|
393次组卷
|
5卷引用:内蒙古杭锦后旗奋斗中学2016-2017学年高一下学期期中考试化学试题
内蒙古杭锦后旗奋斗中学2016-2017学年高一下学期期中考试化学试题(已下线)期中03-2020-2021学年高一化学章末集训必刷卷(人教版2019必修第二册)吉林省长春外国语学校2016-2017学年高一下学期期末考试(理)化学试题广东省揭阳市揭东第一中学2021-2022学年高一下学期期中考试化学试题(已下线)2011-2012学年山东省济宁市微山一中高一3月月考化学试卷
9-10高二下·湖北·期中
6 . 某校化学小组学生利用下图装置进行“氨的催化氧化及其产物验证”实验。(图中夹持装置已略去)

(1)装置B中盛放的试剂是__________ (填名称),用来吸收混合气体中的水汽。
(2)反应开始时,将装置C中铂丝加热到红热,撤去酒精灯,铂丝变暗。此时鼓入空气,铂丝又变红热。写出C中反应的化学方程式______________________ 。
(3)实验过程中,装置D中的导管容易生成无色晶体而堵塞。为了解决该问题,可以在活塞a后增加______ (选填序号)。
①盛有蒸馏水的洗气瓶 ②盛有浓盐酸的洗气瓶 ③盛有碱石灰的U形管
(4)装置E中的含氮化合物有NH3、NO、NO2、________________ (填化学式)。
(5)F中紫色石蕊试液变红,G装置的作用________________ 。
(6)工业上合成氨的反应是:N2(g)+3H2(g)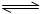 2NH3(g);△H=-92.2kJ·mol-1。
2NH3(g);△H=-92.2kJ·mol-1。
①下列做法能够提高工业合成氨转化率的是_________ (选填字母)
a.增大压强 b.升高温度 c.使用铁触媒 d.将生成的NH3及时从混合气体中分离出去
②工业合成氨时采用500℃左右的温度,主要是因为________________ 。

(1)装置B中盛放的试剂是
(2)反应开始时,将装置C中铂丝加热到红热,撤去酒精灯,铂丝变暗。此时鼓入空气,铂丝又变红热。写出C中反应的化学方程式
(3)实验过程中,装置D中的导管容易生成无色晶体而堵塞。为了解决该问题,可以在活塞a后增加
①盛有蒸馏水的洗气瓶 ②盛有浓盐酸的洗气瓶 ③盛有碱石灰的U形管
(4)装置E中的含氮化合物有NH3、NO、NO2、
(5)F中紫色石蕊试液变红,G装置的作用
(6)工业上合成氨的反应是:N2(g)+3H2(g)
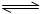 2NH3(g);△H=-92.2kJ·mol-1。
2NH3(g);△H=-92.2kJ·mol-1。①下列做法能够提高工业合成氨转化率的是
a.增大压强 b.升高温度 c.使用铁触媒 d.将生成的NH3及时从混合气体中分离出去
②工业合成氨时采用500℃左右的温度,主要是因为
您最近一年使用:0次



