名校
解题方法
1 .  是一种重要的化工产品,是氮肥工业和制造硝酸、铵盐的重要原料。工业流程如图所示:
是一种重要的化工产品,是氮肥工业和制造硝酸、铵盐的重要原料。工业流程如图所示: 在氮肥工业中发生的是
在氮肥工业中发生的是_______ (填“氧化还原”或“非氧化还原”)反应。
(2)实验室制取氨气通常有两种方法:
Ⅰ.用固体氢氧化钙与氯化铵共热;
Ⅱ.在常温下用固体氢氧化钠与浓氨水混合。
①方法Ⅰ制取氨气的化学方程式为_______ 。
②方法Ⅱ应选用图1的_______ (填“A”或“B”)装置进行。_______ (填“甲”、“乙”或“丙”)进行连接。 与
与 反应的化学方程式为
反应的化学方程式为_______ 。制备硝酸过程中,可循环使用的物质是_______ (填化学式)。
(4)工业上制备的浓硝酸可用铝槽车或铁槽车来运输,原因是_______ ,说明浓硝酸具有_______ 性。
 是一种重要的化工产品,是氮肥工业和制造硝酸、铵盐的重要原料。工业流程如图所示:
是一种重要的化工产品,是氮肥工业和制造硝酸、铵盐的重要原料。工业流程如图所示:
 在氮肥工业中发生的是
在氮肥工业中发生的是(2)实验室制取氨气通常有两种方法:
Ⅰ.用固体氢氧化钙与氯化铵共热;
Ⅱ.在常温下用固体氢氧化钠与浓氨水混合。
①方法Ⅰ制取氨气的化学方程式为
②方法Ⅱ应选用图1的


 与
与 反应的化学方程式为
反应的化学方程式为(4)工业上制备的浓硝酸可用铝槽车或铁槽车来运输,原因是
您最近一年使用:0次
2023-08-04更新
|
135次组卷
|
2卷引用:陕西省西安市阎良区2020-2021学年高一上学期期末考试化学试题
2 . 某化学兴趣小组为了制取并探究氨气性质,按下列装置(夹持装置已略去)进行实验。

【实验探究】
(1)实验室制氨气的化学方程式_______ 利用上述原理,应选用下图中_______ 发生装置进行实验。

(2)F装置中倒置漏斗的作用_______ 。
(3)某同学用排空气法收集一圆底烧瓶氨气做喷泉实验,结果发现液面只上升到圆底烧瓶的一半,该同学认为收集到的氨气不纯,请你求出混合气体的摩尔质量为_______ g/mol,最终所得溶液的浓度为_______ mol/L。

(4)氨气的用途很广,可以作为工业制硝酸的原料,写出氨气催化生成NO的化学方程式_______ 。
(5)硝酸工业尾气中的NO、NO2进入大气后,会形成光化学烟雾、破坏臭氧层等。可用氢氧化钠溶液对含氮氧化物的废气进行处理,反应的化学方程式如下:NO2+NO+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO2+NaNO3+H2O,将一定量NO和NO2的混合气体通入300mL5mol·L-1NaOH溶液中,恰好被完全吸收,则标准状况下NO最多为_______ L。

【实验探究】
(1)实验室制氨气的化学方程式

(2)F装置中倒置漏斗的作用
(3)某同学用排空气法收集一圆底烧瓶氨气做喷泉实验,结果发现液面只上升到圆底烧瓶的一半,该同学认为收集到的氨气不纯,请你求出混合气体的摩尔质量为

(4)氨气的用途很广,可以作为工业制硝酸的原料,写出氨气催化生成NO的化学方程式
(5)硝酸工业尾气中的NO、NO2进入大气后,会形成光化学烟雾、破坏臭氧层等。可用氢氧化钠溶液对含氮氧化物的废气进行处理,反应的化学方程式如下:NO2+NO+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO2+NaNO3+H2O,将一定量NO和NO2的混合气体通入300mL5mol·L-1NaOH溶液中,恰好被完全吸收,则标准状况下NO最多为
您最近一年使用:0次
名校
3 . 硫、氮及其化合物是这一段时间学习的重点。现就硫、氮及其化合物的知识,回答下列问题:
(1)工业上制备硫酸铜是利用废铜屑经灼烧后,在加热情况下跟稀硫酸反应有关的化学方程式是:_______ 。
(2)为实现燃煤脱硫,向煤中加入 ,使燃烧产生的
,使燃烧产生的 转变为稳定的盐类,写出该反应的化学方程式:
转变为稳定的盐类,写出该反应的化学方程式:_______ 。
(3)工业尾气中氮的氧化物常采用碱液吸收法处理。
① 被烧碱溶液吸收时,生成两种钠盐,其物质的量之比1:1,写出该反应的化学方程式:
被烧碱溶液吸收时,生成两种钠盐,其物质的量之比1:1,写出该反应的化学方程式:_______ 。
②NO与 按物质的量之比1:1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐的化学式是
按物质的量之比1:1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐的化学式是_______ 。
(4)浓氨水可以检验输送氯气的管道是否泄漏,如泄漏会冒白烟,写出该反应的化学方程式_______ (氨水用氨气表示)
(5)将一定量的锌与 浓硫酸充分反应后,锌完全溶解,同时生成气体A33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的
浓硫酸充分反应后,锌完全溶解,同时生成气体A33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的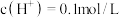 ,则反应过程中转移的电子的物质的量为
,则反应过程中转移的电子的物质的量为_______ 。
(1)工业上制备硫酸铜是利用废铜屑经灼烧后,在加热情况下跟稀硫酸反应有关的化学方程式是:
(2)为实现燃煤脱硫,向煤中加入
 ,使燃烧产生的
,使燃烧产生的 转变为稳定的盐类,写出该反应的化学方程式:
转变为稳定的盐类,写出该反应的化学方程式:(3)工业尾气中氮的氧化物常采用碱液吸收法处理。
①
 被烧碱溶液吸收时,生成两种钠盐,其物质的量之比1:1,写出该反应的化学方程式:
被烧碱溶液吸收时,生成两种钠盐,其物质的量之比1:1,写出该反应的化学方程式:②NO与
 按物质的量之比1:1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐的化学式是
按物质的量之比1:1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐的化学式是(4)浓氨水可以检验输送氯气的管道是否泄漏,如泄漏会冒白烟,写出该反应的化学方程式
(5)将一定量的锌与
 浓硫酸充分反应后,锌完全溶解,同时生成气体A33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的
浓硫酸充分反应后,锌完全溶解,同时生成气体A33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的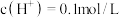 ,则反应过程中转移的电子的物质的量为
,则反应过程中转移的电子的物质的量为
您最近一年使用:0次
名校
4 . 工业上氨气的催化氧化反应的化学方程式_______ 。
您最近一年使用:0次
5 . Ⅰ.硫、氮的氧化物是大气的主要污染物,汽车尾气、工业废气、烟道气等均含有硫或氮元素的氧化物,以 和
和 为主要存在形式。回答下列问题:
为主要存在形式。回答下列问题:
(1)下列关于 和
和 的叙述中正确的是_______(填字母)。
的叙述中正确的是_______(填字母)。
(2)利用氨水可以将SO2和NO2吸收,原理如下图所示:

NO2被吸收的离子方程式是_______ 。
Ⅱ.某化学实验小组同学利用以下实验装置制备氨气,并探究氨气的性质(部分仪器已略去)。请回答:

(3)实验室制备氨气的化学方程式为_______ 。
(4)用装置B收集氨气时,应选择氨气的进气口是_______ (选填“a”或“b”)。
(5)打开装置B中的止水夹c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是_______ 。
Ⅲ.已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用如下示意图中的装置可以实现该反应(夹持装置略)。

(6)反应中氧化剂和还原剂物质的量之比为_______ 。
(7)E中收集的气体为_______ 。
 和
和 为主要存在形式。回答下列问题:
为主要存在形式。回答下列问题:(1)下列关于
 和
和 的叙述中正确的是_______(填字母)。
的叙述中正确的是_______(填字母)。| A.两种气体都无色有毒,且都可用水吸收以消除对空气的污染 |
B.实验室制备 、 、 时,均可用向上排空气的方法收集 时,均可用向上排空气的方法收集 |
| C.两种气体都具有强氧化性,因此都能够使品红溶液褪色 |
D. 与 与 反应转化为 反应转化为 ,属于氮的固定 ,属于氮的固定 |

NO2被吸收的离子方程式是
Ⅱ.某化学实验小组同学利用以下实验装置制备氨气,并探究氨气的性质(部分仪器已略去)。请回答:

(3)实验室制备氨气的化学方程式为
(4)用装置B收集氨气时,应选择氨气的进气口是
(5)打开装置B中的止水夹c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是
Ⅲ.已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用如下示意图中的装置可以实现该反应(夹持装置略)。

(6)反应中氧化剂和还原剂物质的量之比为
(7)E中收集的气体为
您最近一年使用:0次
2022-02-20更新
|
546次组卷
|
4卷引用:山东省青岛莱西市第一中学2021-2022学年高一12月月考(普通班)化学试题
山东省青岛莱西市第一中学2021-2022学年高一12月月考(普通班)化学试题浙江省义乌中学2021-2022学年高一下学期第一次阶段性测试化学试题湖南省娄底市第四中学2021-2022学年高一下学期第一次月考化学试题(已下线)【2023】【高一下】【期中考】【383】【高中化学】
名校
解题方法
6 . 某同学设计实验验证 能还原CuO,装置(部分夹持仪器已省略)如图所示:
能还原CuO,装置(部分夹持仪器已省略)如图所示:
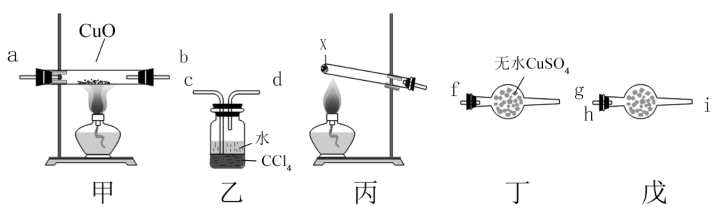
下列说法错误的是
 能还原CuO,装置(部分夹持仪器已省略)如图所示:
能还原CuO,装置(部分夹持仪器已省略)如图所示:
下列说法错误的是
A.试剂X可能是 和 和 的固体混合物 的固体混合物 |
| B.戊盛放的试剂可能是碱石灰,目的是防止空气进入装置 |
| C.装置按合理顺序连接为e→h→i→a→b→f→g→c |
D.证明 能还原CuO的实验现象是甲中黑色粉末变为红色,丁中白色固体变为蓝色 能还原CuO的实验现象是甲中黑色粉末变为红色,丁中白色固体变为蓝色 |
您最近一年使用:0次
2022-02-18更新
|
369次组卷
|
4卷引用:河北省桐柏县第一高级中学2021-2022学年高三上学期10月质量检测化学试题
解题方法
7 . 氮在自然界中的转化是一个复杂的过程,如图所示的氮循环是生态系统物质循环的重要组成部分。
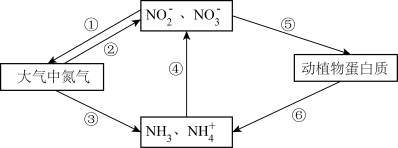
(1)循环图中能够说明含氮有机物可以转化为无机物的是___________ (填转化序号)。
(2)循环图中转化④的反应之一可表示为N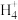 +2O2
+2O2 X+2H++H2O,写出X的化学式:
X+2H++H2O,写出X的化学式:_______ 。
(3)下列有关氮循环说法正确的是___________ 。
a. 图中转化②③④都属于氮的固定
b. 雷雨天气容易发生转化②的过程
c. 动植物蛋白质中一定含有氮元素
(4)氨气与二氧化氮在一定条件下可以发生反应,生成参与大气循环的物质,写出反应的化学方程式:______ 。

(1)循环图中能够说明含氮有机物可以转化为无机物的是
(2)循环图中转化④的反应之一可表示为N
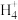 +2O2
+2O2 X+2H++H2O,写出X的化学式:
X+2H++H2O,写出X的化学式:(3)下列有关氮循环说法正确的是
a. 图中转化②③④都属于氮的固定
b. 雷雨天气容易发生转化②的过程
c. 动植物蛋白质中一定含有氮元素
(4)氨气与二氧化氮在一定条件下可以发生反应,生成参与大气循环的物质,写出反应的化学方程式:
您最近一年使用:0次
2022-01-05更新
|
1069次组卷
|
4卷引用:江苏省连云港市2022年普通高中学业水平合格性考试模拟考试化学试题
江苏省连云港市2022年普通高中学业水平合格性考试模拟考试化学试题(已下线)第04讲 氮与氮的氧化物(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)广西桂林市逸仙中学2021-2022学年高一下学期期中考试 化学试题(已下线)专题十三 氮及其化合物
8 .  、
、 和
和 等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1) 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为_____________________ 。
(2) 的氧化吸收。用
的氧化吸收。用 溶液吸收硝酸尾气,可提高尾气中
溶液吸收硝酸尾气,可提高尾气中 的去除率。在酸性溶液中,
的去除率。在酸性溶液中, 氧化
氧化 生成
生成 和
和 ,其离子方程式为
,其离子方程式为___________ 。
(3) 和
和 的处理。工业上用石灰乳吸收已除去
的处理。工业上用石灰乳吸收已除去 的硝酸尾气(含
的硝酸尾气(含 、
、 ),既能净化尾气,又能获得应用广泛的
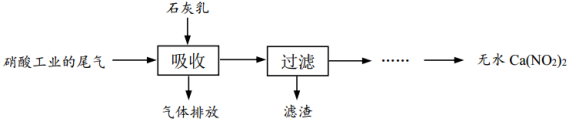
),既能净化尾气,又能获得应用广泛的 ,其部分工艺流程如下:
,其部分工艺流程如下:
注: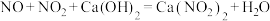 ;
;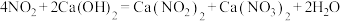
①上述工艺中采用气—液逆流接触吸收(尾气从吸收塔底进入,石灰乳从塔顶喷淋),其目的是__________ ;滤渣可循环使用,其主要成分是__________ (填化学式)。
②该工艺需控制 和
和 物质的量之比接近
物质的量之比接近 。若
。若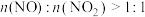 ,则会导致
,则会导致___________ ;若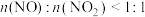 ,则会导致
,则会导致__________ 。
③过滤后的滤液经__________ 、__________ 、过滤、洗涤、干燥,得到无水 。
。
④测定 的纯度。该小组测定产品中
的纯度。该小组测定产品中 纯度的步骤如下:
纯度的步骤如下:
a.称取 产品,溶解、定容至
产品,溶解、定容至 ;
;
b.取 溶液于锥形瓶中,加入过量的
溶液于锥形瓶中,加入过量的 的
的 溶液并酸化;
溶液并酸化;
c.以淀粉为指示剂,用 的
的 溶液滴定,进行三次平行实验,消耗标准溶液体积平均值为
溶液滴定,进行三次平行实验,消耗标准溶液体积平均值为 。(涉及的反应为:
。(涉及的反应为: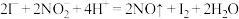 ,
, )
)
该产品中 的质量分数为
的质量分数为__________ 。(写出计算过程)
 、
、 和
和 等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。(1)
 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为(2)
 的氧化吸收。用
的氧化吸收。用 溶液吸收硝酸尾气,可提高尾气中
溶液吸收硝酸尾气,可提高尾气中 的去除率。在酸性溶液中,
的去除率。在酸性溶液中, 氧化
氧化 生成
生成 和
和 ,其离子方程式为
,其离子方程式为(3)
 和
和 的处理。工业上用石灰乳吸收已除去
的处理。工业上用石灰乳吸收已除去 的硝酸尾气(含
的硝酸尾气(含 、
、 ),既能净化尾气,又能获得应用广泛的
),既能净化尾气,又能获得应用广泛的 ,其部分工艺流程如下:
,其部分工艺流程如下:
注:
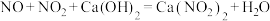 ;
;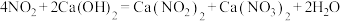
①上述工艺中采用气—液逆流接触吸收(尾气从吸收塔底进入,石灰乳从塔顶喷淋),其目的是
②该工艺需控制
 和
和 物质的量之比接近
物质的量之比接近 。若
。若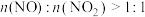 ,则会导致
,则会导致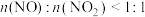 ,则会导致
,则会导致③过滤后的滤液经
 。
。④测定
 的纯度。该小组测定产品中
的纯度。该小组测定产品中 纯度的步骤如下:
纯度的步骤如下:a.称取
 产品,溶解、定容至
产品,溶解、定容至 ;
;b.取
 溶液于锥形瓶中,加入过量的
溶液于锥形瓶中,加入过量的 的
的 溶液并酸化;
溶液并酸化;c.以淀粉为指示剂,用
 的
的 溶液滴定,进行三次平行实验,消耗标准溶液体积平均值为
溶液滴定,进行三次平行实验,消耗标准溶液体积平均值为 。(涉及的反应为:
。(涉及的反应为: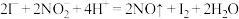 ,
, )
)该产品中
 的质量分数为
的质量分数为
您最近一年使用:0次
9 . NH3与O2作用分别生成N2、NO、N2O的反应均为放热反应。工业尾气中的NH3可通过催化氧化为N2除去。将一定比例的NH3、O2和N2的混合气体以一定流速通过装有催化剂的反应管,NH3的转化率、生成N2的选择性[
 100%]与温度的关系如图所示。
100%]与温度的关系如图所示。

 100%]与温度的关系如图所示。
100%]与温度的关系如图所示。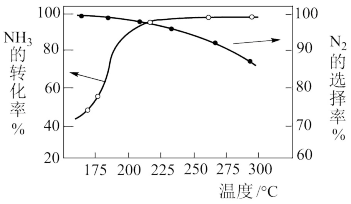
| A.其他条件不变,升高温度,NH3的平衡转化率增大 |
| B.其他条件不变,在175~300 ℃范围,随温度的升高,出口处N2和氮氧化物的量均不断增大 |
| C.催化氧化除去尾气中的NH3应选择反应温度高于250 ℃ |
| D.高效除去尾气中的NH3,需研发低温下NH3转化率高和N2选择性高的催化剂 |
您最近一年使用:0次
2021-11-18更新
|
8343次组卷
|
21卷引用:江苏省镇江市2021-2022学年高三上学期期中考试化学试题
江苏省镇江市2021-2022学年高三上学期期中考试化学试题2021年新高考江苏化学高考真题(已下线)秘籍07 化学反应速率及平衡图象剖析-备战2022年高考化学抢分秘籍(全国通用)(已下线)押江苏卷第14题 反应机理、化学反应速率与平衡 -备战2022年高考化学临考题号押题(江苏卷)湖南省郴州市第一中学2022届高三下学期期中考试化学试题北京市西城区第一六一中学2022届高三考前热身测试化学试题北京市和平街第一中学2021-2022学年高三下学期保温化学试题江苏省平潮高级中学等五校联盟2022届高三高考临门一脚化学试题(已下线)微专题30 非金属及其化合物制备流程与实验探究(S、Se、Te、Cl、Br、I)-备战2023年高考化学一轮复习考点微专题江苏省江阴长泾中学2021-2022学年高二下学期3月份阶段性检测学试题(已下线)专题讲座(七) 常考速率、平衡图像题解题策略(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)微专题38 新情景下的综合图象与突破-备战2023年高考化学一轮复习考点微专题(已下线)易错点11 氮元素及其化合物-备战2023年高考化学考试易错题(已下线)易错点22 化学反应平衡和移动-备战2023年高考化学考试易错题广东省深圳市红岭中学2022-2023学年高二上学期期中考试化学试题湖南省株洲市第四中学2022-2023学年高二上学期期中考试化学试题(已下线)专题15 化学反应速率和化学平衡(已下线)专题15 化学反应速率和化学平衡(已下线)第28讲化化学平衡的移动及反应进行的方向(已下线)题型12 化学平衡图表分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)2024新东方高一上期末考化学01
名校
解题方法
10 . 根据要求回答下列有关问题
I:下列物品或设施:①陶瓷餐具②硅太阳能电池③混凝土桥墩④光导纤维⑤计算机芯片⑥石英钟
(1)使用了硅单质的是___________ (填序号,下同)。
(2)使用了二氧化硅的是___________ 。
(3)使用了硅酸盐材料的是___________ 。
II:我国空气质量预报的内容主要包括:二氧化硫、氮氧化物、悬浮颗粒物等三种大气污染物的浓度。
(4)与氮氧化物有关的全球或区域性大气环境问题有___________ (填字母序号)。
a.酸雨 b.沙尘暴 c.光化学烟雾 d.白色污染
(5)为避免硝酸生产尾气中的氮氧化物对环境的破坏作用。通常用以下两种方法处理。
①纯碱溶液吸收法。写出用纯碱溶液处理NO2的离子方程式_______ 。
②氨催化转化法。写出用NH3将NO还原为无害物质的化学方程式___ 。现有1molNH3和NO的混合气体充分反应,若还原产物比氧化产物多1.4g,则原混合气体中NO和NH3的物质的量之比为__ 。
I:下列物品或设施:①陶瓷餐具②硅太阳能电池③混凝土桥墩④光导纤维⑤计算机芯片⑥石英钟
(1)使用了硅单质的是
(2)使用了二氧化硅的是
(3)使用了硅酸盐材料的是
II:我国空气质量预报的内容主要包括:二氧化硫、氮氧化物、悬浮颗粒物等三种大气污染物的浓度。
(4)与氮氧化物有关的全球或区域性大气环境问题有
a.酸雨 b.沙尘暴 c.光化学烟雾 d.白色污染
(5)为避免硝酸生产尾气中的氮氧化物对环境的破坏作用。通常用以下两种方法处理。
①纯碱溶液吸收法。写出用纯碱溶液处理NO2的离子方程式
②氨催化转化法。写出用NH3将NO还原为无害物质的化学方程式
您最近一年使用:0次
2021-11-05更新
|
307次组卷
|
2卷引用:湖北省华中师范大学第一附属中学2020-2021学年高一下学期期中检测化学试题



