名校
解题方法
1 . 下列每组的叙述Ⅰ、Ⅱ都正确,且有因果关系的是
| 叙述Ⅰ | 叙述Ⅱ | |
| A | 实验室中可通加热固体氯化铵的方法制备氨气 | 氯化铵受热易分解生成氨气 |
| B | 将纯净的 通入紫色石蕊试液中,溶液褪色 通入紫色石蕊试液中,溶液褪色 |  有漂白性 有漂白性 |
| C | 断裂 分子中H-N键要吸收热量 分子中H-N键要吸收热量 | 工业上用液氨作制冷剂 |
| D | 取少量 固体样品溶于蒸馏水,加入足量稀盐酸,再加入足量 固体样品溶于蒸馏水,加入足量稀盐酸,再加入足量 溶液,若有白色沉淀产生,说明产品已变质 溶液,若有白色沉淀产生,说明产品已变质 |  暴露于空气中容易被氧化为 暴露于空气中容易被氧化为 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 下列说法正确的是
| A.实验室中可通过加热氯化铵固体制取氨气 |
| B.常温下,可以用铝罐贮存浓硫酸和浓硝酸,说明铝与浓硫酸和浓硝酸不反应 |
| C.在胆矾中加入浓硫酸后,胆矾由蓝色变为白色,说明浓硫酸具有吸水性 |
| D.将Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红,说明原样品已变质 |
您最近一年使用:0次
2021-07-03更新
|
210次组卷
|
3卷引用:山西省长治第二中学2020-2021学年高一下学期期末考试化学试题
3 . 氨基甲酸铵(NH2COONH4)是一种易分解、易水解的白色固体,难溶于CCl4。实验室可将干燥二氧化碳和干燥氨气通入CCl4中进行制备,化学方程式为:2NH3(g)+CO2(g)=NH2COONH4(s) ΔH<0。
回答下列问题:
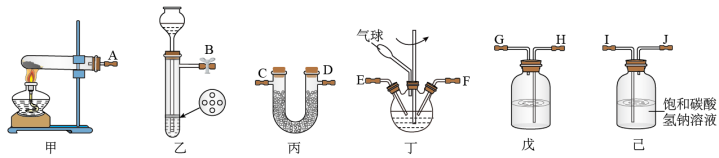
(1)利用装置甲制备氨气的化学方程式为__ 。
(2)简述检查装置乙气密性的操作__ 。
(3)选择图中的装置制备氨基甲酸铵,仪器接口的连接顺序为:B→__ →__ →EF←__ ←A。
(4)反应时为了增加氨基甲酸铵的产量,三颈瓶的加热方式为__ (填“热水浴”或“冷水浴”);丁中气球的作用是__ 。
(5)从装置丁的混合物中分离出产品的方法是__ (填写操作名称)。
(6)取因吸潮变质为碳酸氢铵的氨基甲酸铵样品11.730g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥、称量,质量为15.000g。则样品中氨基甲酸铵的质量分数为__ (已知:Mr(NH2COONH4)=78、Mr(NH4HCO3)=79、Mr(CaCO3)=100。计算结果保留3位有效数字)。
回答下列问题:

(1)利用装置甲制备氨气的化学方程式为
(2)简述检查装置乙气密性的操作
(3)选择图中的装置制备氨基甲酸铵,仪器接口的连接顺序为:B→
(4)反应时为了增加氨基甲酸铵的产量,三颈瓶的加热方式为
(5)从装置丁的混合物中分离出产品的方法是
(6)取因吸潮变质为碳酸氢铵的氨基甲酸铵样品11.730g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥、称量,质量为15.000g。则样品中氨基甲酸铵的质量分数为
您最近一年使用:0次
2020-03-14更新
|
239次组卷
|
2卷引用:武汉市2020届高中毕业生学生质量检测化学试题
名校
解题方法
4 . 氨基甲酸铵(H2NCOONH4)是一种易分解、易水解的白色固体,可用于化肥、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵:
反应式:2NH3(g)+CO2(g) H2NCOONH4△H <0
H2NCOONH4△H <0
(1)如果使用如图所示的装置制取NH3,你所选择的试剂是_____________ 。

(2)备氨基甲酸铵的装置如下图。把氨和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中,当悬浮物较多时,停止制备:(注:四氯化碳与液体石蜡均为惰性介质。)
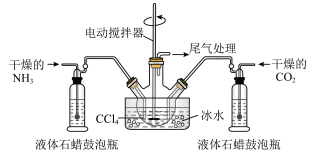
①发生器用冰水冷却的原因是_______ ,液体石蜡鼓泡瓶的作用是__________ ,发生反应的仪器名称是_______________ 。
②从反应后的混合物中过滤分离出产品。为了得到干燥产品,应采取的方法是_____ (选填序号)
a.常压加热烘干 b.高压加热烘干 c.真空40℃以下烘干
(3)尾气有污染,可用________ 溶液吸收处理。
(4)取因部分变质而混有碳酸氢铵的氨基甲酸铵钱样品1.1730g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.500g。样品中氨基甲酸铵的物质的量分数为__________ 。[已知Mr(H2NCOONH4)=78, Mr(NH4HCO3)=79, Mr(CaCO3)=100]
反应式:2NH3(g)+CO2(g)
 H2NCOONH4△H <0
H2NCOONH4△H <0(1)如果使用如图所示的装置制取NH3,你所选择的试剂是

(2)备氨基甲酸铵的装置如下图。把氨和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中,当悬浮物较多时,停止制备:(注:四氯化碳与液体石蜡均为惰性介质。)

①发生器用冰水冷却的原因是
②从反应后的混合物中过滤分离出产品。为了得到干燥产品,应采取的方法是
a.常压加热烘干 b.高压加热烘干 c.真空40℃以下烘干
(3)尾气有污染,可用
(4)取因部分变质而混有碳酸氢铵的氨基甲酸铵钱样品1.1730g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.500g。样品中氨基甲酸铵的物质的量分数为
您最近一年使用:0次
2017-03-15更新
|
810次组卷
|
3卷引用:2017届四川省成都市第七中学高三二诊模拟考试理综化学试卷
5 . 工业上用饱和食盐水吸收尾气 和
和 制备无水
制备无水 。同时得到副产物
。同时得到副产物 。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
。实验室用如图装置模拟该制备过程(加热和固定装置已省略):

已知:浓硫酸的沸点为338℃。回答下列问题:
(1)导气管b的作用___________ 。
(2)装置B中发生的化学反应的化学方程式为___________ 。
(3)固、固加热制取氨气的发生装置可以选择下图中的___________ (填编号),反应的化学方程式为___________ 。
C.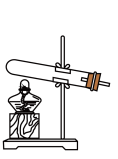 D.
D.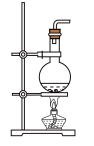 E.
E.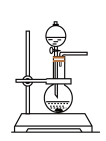 F.
F.
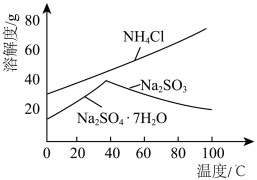
(4)利用各物质的溶解度曲线图(见图)分离产品,取出装置B中的溶液,蒸发浓缩,趁热过滤可得___________ ,然后将滤液___________ 、过滤、洗涤、干燥可得另一产物。
(5)产品中可能混有少量 和
和 杂质,混有
杂质,混有 杂质的原因可能是
杂质的原因可能是___________ ,检验产品中含有 的的实验方法:取少量样品于试管中,加入适量水溶解,
的的实验方法:取少量样品于试管中,加入适量水溶解,___________ 。
【可选试剂:稀硝酸、 溶液、酸性
溶液、酸性 溶液、
溶液、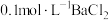 溶液、
溶液、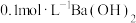 溶液、
溶液、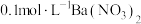 溶液】
溶液】
 和
和 制备无水
制备无水 。同时得到副产物
。同时得到副产物 。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
已知:浓硫酸的沸点为338℃。回答下列问题:
(1)导气管b的作用
(2)装置B中发生的化学反应的化学方程式为
(3)固、固加热制取氨气的发生装置可以选择下图中的
C.
 D.
D. E.
E. F.
F.
(4)利用各物质的溶解度曲线图(见图)分离产品,取出装置B中的溶液,蒸发浓缩,趁热过滤可得

(5)产品中可能混有少量
 和
和 杂质,混有
杂质,混有 杂质的原因可能是
杂质的原因可能是 的的实验方法:取少量样品于试管中,加入适量水溶解,
的的实验方法:取少量样品于试管中,加入适量水溶解,【可选试剂:稀硝酸、
 溶液、酸性
溶液、酸性 溶液、
溶液、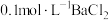 溶液、
溶液、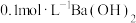 溶液、
溶液、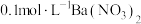 溶液】
溶液】
您最近一年使用:0次
解题方法
6 . 四氮化四硫( ,S为+2价)是重要的硫-氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于
,S为+2价)是重要的硫-氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于 等有机溶剂,可用
等有机溶剂,可用 与
与 (红棕色液体)反应制备,反应装置如图所示(夹持装置略)。
(红棕色液体)反应制备,反应装置如图所示(夹持装置略)。
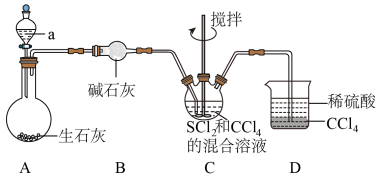
已知:
回答下列问题;
(1)试剂a是___________ (填化学式);B中的碱石灰___________ 用五氧化二磷代替(填“能”或“不能”)。
(2)装置C中生成 的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为
的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为___________ ;证明 反应完全的现象是
反应完全的现象是___________ 。
(3)分离产物后测定产品纯度:
i.蒸氨:取0.1000g样品加入三颈烧瓶中,再加入足量NaOH溶液并加热,蒸出的 。通入含有
。通入含有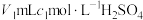 标准溶液的锥形瓶中。
标准溶液的锥形瓶中。
ii.滴定:用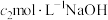 溶液滴定剩余的
溶液滴定剩余的 ,消耗
,消耗 溶液。
溶液。
①若滴定时选用酚酞作指示剂,滴定终点的现象为___________ 。
② 的纯度表达式为
的纯度表达式为___________ (用质量分数表示);若配制NaOH溶液时称量时间过长,测定结果___________ (填“偏高”“偏低”或“无影响”)。
 ,S为+2价)是重要的硫-氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于
,S为+2价)是重要的硫-氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于 等有机溶剂,可用
等有机溶剂,可用 与
与 (红棕色液体)反应制备,反应装置如图所示(夹持装置略)。
(红棕色液体)反应制备,反应装置如图所示(夹持装置略)。
已知:

回答下列问题;
(1)试剂a是
(2)装置C中生成
 的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为
的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为 反应完全的现象是
反应完全的现象是(3)分离产物后测定产品纯度:
i.蒸氨:取0.1000g样品加入三颈烧瓶中,再加入足量NaOH溶液并加热,蒸出的
 。通入含有
。通入含有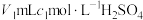 标准溶液的锥形瓶中。
标准溶液的锥形瓶中。ii.滴定:用
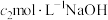 溶液滴定剩余的
溶液滴定剩余的 ,消耗
,消耗 溶液。
溶液。①若滴定时选用酚酞作指示剂,滴定终点的现象为
②
 的纯度表达式为
的纯度表达式为
您最近一年使用:0次
名校
7 . 氨基甲酸铵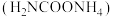 是一种易水解且受热易分解的白色固体,易溶于水,难溶于
是一种易水解且受热易分解的白色固体,易溶于水,难溶于 ,某研究小组用如图所示的实验装置制备氨基甲酸铵。
,某研究小组用如图所示的实验装置制备氨基甲酸铵。
反应原理: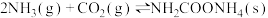

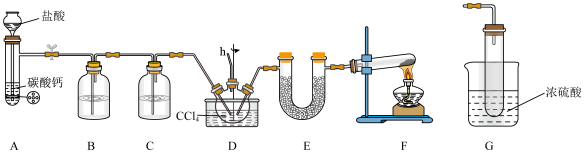
(1)仪器组装完毕后,首先应进行的操作是___________ ,仪器F中发生反应的化学方程式为___________ 。
(2)装置B中所盛的试剂是___________ 溶液,E中所盛的药品可以是___________ (填序号)。
A碱石灰 B. C.无水氯化钙 D.浓硫酸
C.无水氯化钙 D.浓硫酸
(3)对比本实验装置,有同学用如图所示装置来代替产生 气体,其优点有___________(填序号)。
气体,其优点有___________(填序号)。
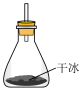
(4)反应过程中需要将装置D放入冰水浴中,从原料转化率和产物纯度的角度分析,原因可能是___________ 、___________ 。
(5)导管h一般与装置G相连,则装置G除了能防倒吸,还具有的作用是___________ 。
(6)产品纯度分析:称取产品3.91g(内含杂质 ),加入足量石灰水充分反应,使碳元素全部转化为碳酸钙,经过滤、洗涤、干燥后称量,测得质量为5.00g,则样品中氨基甲酸铵的质量分数是
),加入足量石灰水充分反应,使碳元素全部转化为碳酸钙,经过滤、洗涤、干燥后称量,测得质量为5.00g,则样品中氨基甲酸铵的质量分数是___________ (计算结果保留小数点后两位)。[摩尔质量: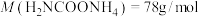 、
、 ]
]
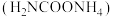 是一种易水解且受热易分解的白色固体,易溶于水,难溶于
是一种易水解且受热易分解的白色固体,易溶于水,难溶于 ,某研究小组用如图所示的实验装置制备氨基甲酸铵。
,某研究小组用如图所示的实验装置制备氨基甲酸铵。反应原理:
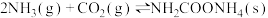


(1)仪器组装完毕后,首先应进行的操作是
(2)装置B中所盛的试剂是
A碱石灰 B.
 C.无水氯化钙 D.浓硫酸
C.无水氯化钙 D.浓硫酸(3)对比本实验装置,有同学用如图所示装置来代替产生
 气体,其优点有___________(填序号)。
气体,其优点有___________(填序号)。
| A.装置简单,操作方便 |
B.避免了 的净化和干燥处理 的净化和干燥处理 |
| C.加快了氨基甲酸胺的生成速率 |
D.对 的流速有更好的调控和掌握 的流速有更好的调控和掌握 |
(5)导管h一般与装置G相连,则装置G除了能防倒吸,还具有的作用是
(6)产品纯度分析:称取产品3.91g(内含杂质
 ),加入足量石灰水充分反应,使碳元素全部转化为碳酸钙,经过滤、洗涤、干燥后称量,测得质量为5.00g,则样品中氨基甲酸铵的质量分数是
),加入足量石灰水充分反应,使碳元素全部转化为碳酸钙,经过滤、洗涤、干燥后称量,测得质量为5.00g,则样品中氨基甲酸铵的质量分数是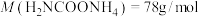 、
、 ]
]
您最近一年使用:0次
名校
8 . 近年来,人们对微生物的氮转化进行了深入研究,将其归纳为如图1所示过程。请回答下列问题:
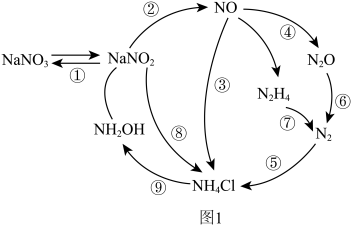
(1)N2的电子式为_____ ;羟胺(NH2OH)的结构式为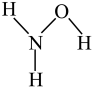 ,属于
,属于_____ (填“离子”或“共价”)化合物。
(2)笑气(N2O)可用作医用麻醉剂、制冷剂,实验室通过加热NH4NO3分解制备N2O,只有两种产物,写出该反应的化学方程式:_____ 。
(3)图1转化过程中具有固氮功能的是_____ (填标号)。
(4)实验室常用氢氧化钙和氯化铵制备氨气,反应装置如图2所示。
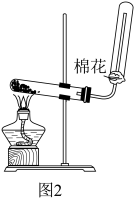
I.写出该反应的化学方程式:_____ 。
Ⅱ.棉花的作用为_____ 。
(5)NaNO2和食盐性状相似,社会上曾多次发生将NaNO2误当食盐食用的事件。可用0.1mol•L-1酸性KMnO4溶液来测定某亚硝酸钠样品中NaNO2的含量(假设杂质不与KMnO4溶液反应),进行三次实验,每次取ag样品,消耗酸性KMnO4溶液的平均体积为20.00mL。测定原理为NO +MnO
+MnO +H+→NO
+H+→NO +Mn2++H2O。
+Mn2++H2O。
I.请配平该离子方程式:_____ 。
Ⅱ.NaNO2的质量分数为_____ %。

(1)N2的电子式为
 ,属于
,属于(2)笑气(N2O)可用作医用麻醉剂、制冷剂,实验室通过加热NH4NO3分解制备N2O,只有两种产物,写出该反应的化学方程式:
(3)图1转化过程中具有固氮功能的是
(4)实验室常用氢氧化钙和氯化铵制备氨气,反应装置如图2所示。

I.写出该反应的化学方程式:
Ⅱ.棉花的作用为
(5)NaNO2和食盐性状相似,社会上曾多次发生将NaNO2误当食盐食用的事件。可用0.1mol•L-1酸性KMnO4溶液来测定某亚硝酸钠样品中NaNO2的含量(假设杂质不与KMnO4溶液反应),进行三次实验,每次取ag样品,消耗酸性KMnO4溶液的平均体积为20.00mL。测定原理为NO
 +MnO
+MnO +H+→NO
+H+→NO +Mn2++H2O。
+Mn2++H2O。I.请配平该离子方程式:
Ⅱ.NaNO2的质量分数为
您最近一年使用:0次
2023-04-18更新
|
403次组卷
|
3卷引用:辽宁省部分学校联考2022-2023学年高一下学期4月月考化学试题
名校
解题方法
9 . 人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,合成氨是人类发展史上的一项重大突破。某化学兴趣小组对氨气进行研究:
I. 催化还原氮氧化物(SCR技术是目前应用最广泛的烟气氮氧化物脱除技术),反应原理如下图所示:
催化还原氮氧化物(SCR技术是目前应用最广泛的烟气氮氧化物脱除技术),反应原理如下图所示:
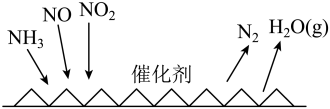
(1)SCR催化反应器中 还原
还原 的化学方程式为
的化学方程式为_______ 。
II.用下图装置可以制取氨气并探究其性质,按下列装置(部分夹持装置已略去)进行实验。

(2)若氨气的发生装置选择A,则其化学反应方程式为_______ 。
(3)若要用C装置来干燥 ,可以选用的干燥剂为
,可以选用的干燥剂为_______ 。
(4)上述D、E、F、G装置可用于作为氨气的尾气处理装置的是_______ 。
(5)用下图装置探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。
已知:CuO在高温时不稳定,会自身分解得到红色的

①实验结束后H处硬质玻璃管中黑色粉末变成红色,该红色粉末的成分能否确定?_______ (填“能”或“否”)。请通过检验其他产物证明 和CuO发生了反应,简述实验方案:
和CuO发生了反应,简述实验方案:_______ 。
②若经实验测定 和CuO反应的产物有Cu和无污染气体,则
和CuO反应的产物有Cu和无污染气体,则 和CuO反应的化学方程式为
和CuO反应的化学方程式为_______ 。
(6)已知加热条件下,氨气可以与铝发生置换反应生成AlN;AlN性质稳定,加热时溶于浓碱溶液且可产生氨气。称取AlN样品23.2 g(假设杂质只含Al),将其放入足量浓碱溶液中加热,若所产生的气体全部逸出并收集,测得其体积为14.56 L(标准状况),则样品中AlN的质量分数为_______ %(保留一位小数)。
I.
 催化还原氮氧化物(SCR技术是目前应用最广泛的烟气氮氧化物脱除技术),反应原理如下图所示:
催化还原氮氧化物(SCR技术是目前应用最广泛的烟气氮氧化物脱除技术),反应原理如下图所示:
(1)SCR催化反应器中
 还原
还原 的化学方程式为
的化学方程式为II.用下图装置可以制取氨气并探究其性质,按下列装置(部分夹持装置已略去)进行实验。

(2)若氨气的发生装置选择A,则其化学反应方程式为
(3)若要用C装置来干燥
 ,可以选用的干燥剂为
,可以选用的干燥剂为(4)上述D、E、F、G装置可用于作为氨气的尾气处理装置的是
(5)用下图装置探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。
已知:CuO在高温时不稳定,会自身分解得到红色的


①实验结束后H处硬质玻璃管中黑色粉末变成红色,该红色粉末的成分能否确定?
 和CuO发生了反应,简述实验方案:
和CuO发生了反应,简述实验方案:②若经实验测定
 和CuO反应的产物有Cu和无污染气体,则
和CuO反应的产物有Cu和无污染气体,则 和CuO反应的化学方程式为
和CuO反应的化学方程式为(6)已知加热条件下,氨气可以与铝发生置换反应生成AlN;AlN性质稳定,加热时溶于浓碱溶液且可产生氨气。称取AlN样品23.2 g(假设杂质只含Al),将其放入足量浓碱溶液中加热,若所产生的气体全部逸出并收集,测得其体积为14.56 L(标准状况),则样品中AlN的质量分数为
您最近一年使用:0次
2023-03-07更新
|
716次组卷
|
2卷引用:湖南省长沙市第一中学2022-2023学年高一下学期第一次月考(3月)化学试题
10 . 工业上用饱和食盐水吸收尾气 和
和 制备无水
制备无水 。同时得到副产物
。同时得到副产物 。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
。实验室用如图装置模拟该制备过程(加热和固定装置已省略):

已知:浓硫酸的沸点为338℃。回答下列问题:
(1)仪器a的名称_______ ,导气管b的作用_______ 。
(2)装置A中发生的化学反应的化学方程式为_______ 。
(3)固、固加热制取氨气的发生装置可以选择下图中的_______ (填编号),反应的化学方程式为_______ 。

(4)利用各物质的溶解度曲线图(见图)分离产品,取出装置B中的溶液,蒸发浓缩,趁热过滤可得_______ ,然后将滤液_______ 、过滤、洗涤、干燥可得另一产物。

(5)产品中可能混有少量 和
和 杂质,混有
杂质,混有 杂质的原因可能是
杂质的原因可能是_______ ,检验产品中含有 的的实验方法:取少量样品于试管中,加入适量水溶解,
的的实验方法:取少量样品于试管中,加入适量水溶解,_______ 。
【可选试剂:稀硝酸、 溶液、酸性
溶液、酸性 溶液、
溶液、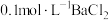 溶液、
溶液、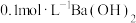 溶液、
溶液、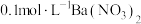 溶液】
溶液】
 和
和 制备无水
制备无水 。同时得到副产物
。同时得到副产物 。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
已知:浓硫酸的沸点为338℃。回答下列问题:
(1)仪器a的名称
(2)装置A中发生的化学反应的化学方程式为
(3)固、固加热制取氨气的发生装置可以选择下图中的

(4)利用各物质的溶解度曲线图(见图)分离产品,取出装置B中的溶液,蒸发浓缩,趁热过滤可得

(5)产品中可能混有少量
 和
和 杂质,混有
杂质,混有 杂质的原因可能是
杂质的原因可能是 的的实验方法:取少量样品于试管中,加入适量水溶解,
的的实验方法:取少量样品于试管中,加入适量水溶解,【可选试剂:稀硝酸、
 溶液、酸性
溶液、酸性 溶液、
溶液、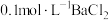 溶液、
溶液、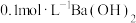 溶液、
溶液、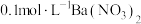 溶液】
溶液】
您最近一年使用:0次
2023-02-25更新
|
986次组卷
|
4卷引用:广东省茂名市电白区2021-2022学年高一下学期期末(选择性)考试化学试题



