1 . 下列装置(部分夹持装置略去)中仪器使用规范且能达到实验目的的是
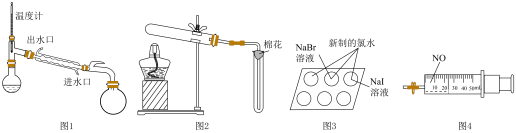
| A.图1:采用蒸馏法分离正己烷(沸点69℃)和正庚烷(沸点98℃) |
B.图2:用 和 和 制备并收集 制备并收集 |
| C.图3:通过观察实验现象,验证氯、溴和碘元素性质的递变规律 |
D.图4:利用该装置实现NO、 和 和 充分反应转化为 充分反应转化为 |
您最近一年使用:0次
2024-05-14更新
|
92次组卷
|
2卷引用:2024届河南省平许济洛四市高三下学期第四次质量检测理科综合试题-高中化学
名校
解题方法
2 . 亚硝酸钠 是一种化工产品,易溶于水,无漂白性。亚硝酸钠的制备原理为
是一种化工产品,易溶于水,无漂白性。亚硝酸钠的制备原理为
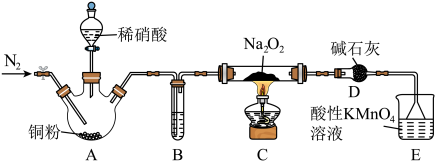
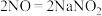 。某小组设计实验制备亚硝酸钠并测定其纯度和探究其性质,装置如图所示。已知:常温下,酸性
。某小组设计实验制备亚硝酸钠并测定其纯度和探究其性质,装置如图所示。已知:常温下,酸性 溶液能吸收
溶液能吸收 生成无色的
生成无色的 和
和 。
。
(1) 装置的作用是
装置的作用是___________ 。
(2)写出 装置中发生反应的化学方程式:
装置中发生反应的化学方程式:___________ 。
(3) 装置中紫红色变为无色,发生反应的离子方程式为
装置中紫红色变为无色,发生反应的离子方程式为___________ 。
(4)实验完毕,设计实验证明产品是否含有 :
:___________ 。
(5)为了探究 的性质,设计如下实验:
的性质,设计如下实验:
上述实验能证明 具有氧化性的是
具有氧化性的是___________ (填“I”或“II”)。
(6)取
 产品溶于水配制成
产品溶于水配制成 溶液,准确量取
溶液,准确量取 所配溶液于锥形瓶中,恰好与
所配溶液于锥形瓶中,恰好与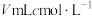 酸性
酸性 溶液完全反应。该产品中
溶液完全反应。该产品中 的质量分数为
的质量分数为___________ (已知: 和酸性
和酸性 溶液反应生成
溶液反应生成 和
和 )。
)。
 是一种化工产品,易溶于水,无漂白性。亚硝酸钠的制备原理为
是一种化工产品,易溶于水,无漂白性。亚硝酸钠的制备原理为
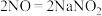 。某小组设计实验制备亚硝酸钠并测定其纯度和探究其性质,装置如图所示。已知:常温下,酸性
。某小组设计实验制备亚硝酸钠并测定其纯度和探究其性质,装置如图所示。已知:常温下,酸性 溶液能吸收
溶液能吸收 生成无色的
生成无色的 和
和 。
。
(1)
 装置的作用是
装置的作用是(2)写出
 装置中发生反应的化学方程式:
装置中发生反应的化学方程式:(3)
 装置中紫红色变为无色,发生反应的离子方程式为
装置中紫红色变为无色,发生反应的离子方程式为(4)实验完毕,设计实验证明产品是否含有
 :
:(5)为了探究
 的性质,设计如下实验:
的性质,设计如下实验:| 序号 | 操作 | 现象 |
| I | 取少量 溶于水,滴加酚酞溶液 溶于水,滴加酚酞溶液 | 溶液变红色 |
| II | 取少量  溶于水,滴加稀硫酸和 溶于水,滴加稀硫酸和 溶液,再滴加淀粉溶液 溶液,再滴加淀粉溶液 | 溶液变蓝色 |
 具有氧化性的是
具有氧化性的是(6)取

 产品溶于水配制成
产品溶于水配制成 溶液,准确量取
溶液,准确量取 所配溶液于锥形瓶中,恰好与
所配溶液于锥形瓶中,恰好与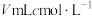 酸性
酸性 溶液完全反应。该产品中
溶液完全反应。该产品中 的质量分数为
的质量分数为 和酸性
和酸性 溶液反应生成
溶液反应生成 和
和 )。
)。
您最近一年使用:0次
名校
解题方法
3 . 亚硝酸钠广泛用于工业、建筑业及食品加工业.某课外活动小组的同学拟制备亚硝酸钠、测定其产品的纯度并验证亚硝酸钠的某些性质。
(1)甲组同学采用下图装置制取亚硝酸钠。______ 。
②A中用 的硫酸而不用稀硫酸的原因是
的硫酸而不用稀硫酸的原因是______ 。
③若通入装置 中的
中的 与
与 按物质的量之比1:1被
按物质的量之比1:1被 溶液完全吸收,反应过程中无气体生成,则装置
溶液完全吸收,反应过程中无气体生成,则装置 中发生反应的化学方程式为
中发生反应的化学方程式为______ 。
(2)乙组同学测定甲组制得的产品中 的纯度。称取
的纯度。称取 试样于锥形瓶中,加入适量水溶解,与
试样于锥形瓶中,加入适量水溶解,与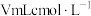 的酸性
的酸性 溶液恰好完全反应,则产品的纯度为
溶液恰好完全反应,则产品的纯度为______ (用含c、m、V的代数式表示)。
(3)现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应气体产物的成分。已知:气体液化的温度 为
为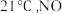 为
为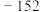 ℃。
℃。 中生成的气体产物,仪器的连接顺序(按左
中生成的气体产物,仪器的连接顺序(按左 右连接)为
右连接)为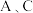 、
、______ 、______ 、______ 。
②装置 的作用是
的作用是______ 。
③滴入硫酸后,观察到A中有红棕色气体产生。依据______ 的现象,确定该气体中还有NO。
④通过上述实验探究过程,可得出装置A中反应的化学方程式是______ 。
(1)甲组同学采用下图装置制取亚硝酸钠。
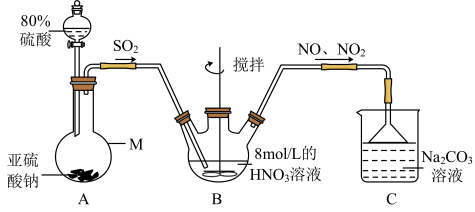
②A中用
 的硫酸而不用稀硫酸的原因是
的硫酸而不用稀硫酸的原因是③若通入装置
 中的
中的 与
与 按物质的量之比1:1被
按物质的量之比1:1被 溶液完全吸收,反应过程中无气体生成,则装置
溶液完全吸收,反应过程中无气体生成,则装置 中发生反应的化学方程式为
中发生反应的化学方程式为(2)乙组同学测定甲组制得的产品中
 的纯度。称取
的纯度。称取 试样于锥形瓶中,加入适量水溶解,与
试样于锥形瓶中,加入适量水溶解,与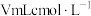 的酸性
的酸性 溶液恰好完全反应,则产品的纯度为
溶液恰好完全反应,则产品的纯度为(3)现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应气体产物的成分。已知:气体液化的温度
 为
为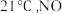 为
为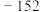 ℃。
℃。
 中生成的气体产物,仪器的连接顺序(按左
中生成的气体产物,仪器的连接顺序(按左 右连接)为
右连接)为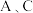 、
、②装置
 的作用是
的作用是③滴入硫酸后,观察到A中有红棕色气体产生。依据
④通过上述实验探究过程,可得出装置A中反应的化学方程式是
您最近一年使用:0次
23-24高二上·浙江杭州·期末
解题方法
4 . 亚硝酰氯(NOCl)是一种红褐色液体或黄色气体,熔点:-64.5℃,沸点:-5.5℃, 遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可用下图装置由氯气与一氧化氮在常温常压下合成。
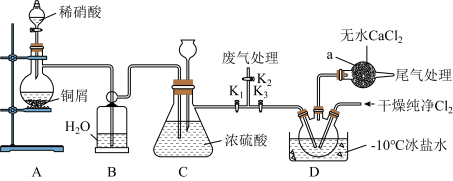
简要步骤如下:实验开始时,关闭K1,打开K2、K3,通入一段时间的氯气,直至三颈烧瓶中充满黄绿色气体,关闭K3,打开K1,打开分液漏斗塞子,向烧瓶中滴入适量稀硝酸;待装置C中某一现象发生时,关闭K2,打开K3,在三颈烧瓶中制备亚硝酰氯。
请回答:
(1)仪器a的名称是___________ ,装置B的作用是___________ 。
(2)步骤划线处,装置C出现的现象是___________ 。
(3)该实验用高锰酸钾和浓盐酸来制取氯气,写出该反应的离子方程式:___________ 。
(4)写出亚硝酰氯与NaOH溶液反应生成亚硝酸钠的化学方程式:___________ 。
(5)不列说法不正确的是___________

简要步骤如下:实验开始时,关闭K1,打开K2、K3,通入一段时间的氯气,直至三颈烧瓶中充满黄绿色气体,关闭K3,打开K1,打开分液漏斗塞子,向烧瓶中滴入适量稀硝酸;待装置C中某一现象发生时,关闭K2,打开K3,在三颈烧瓶中制备亚硝酰氯。
请回答:
(1)仪器a的名称是
(2)步骤划线处,装置C出现的现象是
(3)该实验用高锰酸钾和浓盐酸来制取氯气,写出该反应的离子方程式:
(4)写出亚硝酰氯与NaOH溶液反应生成亚硝酸钠的化学方程式:
(5)不列说法不正确的是___________
| A.从安全或避免环境污染方面考虑,宜在通风橱内进行实验 |
| B.为加快反应速率,装置A中可用酒精灯大火加热制取NO |
| C.浓硫酸和无水CaCl2可以阻止水蒸气进入,避免亚硝酰氯水解 |
| D.冰盐水温度可达-10℃,装置D三颈烧瓶中充满黄色气体NOCl |
您最近一年使用:0次
5 . 氮元素的价类二维图如下图所示,请据此回答:

(1)X的化学式为___________ ;从物质性质上看, 属于
属于___________ 性氧化(填“酸”或碱) 转化为
转化为
___________ 氧化还原反应(填“是”或“不是”)。
(2)亚硝酸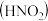 可由上图中的两种气体(已知:
可由上图中的两种气体(已知: 常温下为固体)按一定比例通入水中制得,两种气体分别为
常温下为固体)按一定比例通入水中制得,两种气体分别为___________ (填化学式)。
(3)工业上以 、空气、水为原料通过三步反应生产硝酸:
、空气、水为原料通过三步反应生产硝酸:
①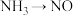 ,其化学方程式为
,其化学方程式为___________ 。
② ,其实验现象为
,其实验现象为___________ 。
③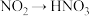 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(4)实验室欲制备一瓶干燥的氨气,装置如下图所示:

①氨气的发生装置可以选择上图中的___________ ,反应的化学方程式为___________ 。
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为(按气流方向):发生装置
___________ ,用小写字母表示 。
。

(1)X的化学式为
 属于
属于 转化为
转化为
(2)亚硝酸
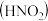 可由上图中的两种气体(已知:
可由上图中的两种气体(已知: 常温下为固体)按一定比例通入水中制得,两种气体分别为
常温下为固体)按一定比例通入水中制得,两种气体分别为(3)工业上以
 、空气、水为原料通过三步反应生产硝酸:
、空气、水为原料通过三步反应生产硝酸:①
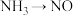 ,其化学方程式为
,其化学方程式为②
 ,其实验现象为
,其实验现象为③
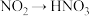 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为(4)实验室欲制备一瓶干燥的氨气,装置如下图所示:

①氨气的发生装置可以选择上图中的
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为(按气流方向):发生装置

 。
。
您最近一年使用:0次
6 . 根据题意解答
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:_______ 。
(2)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。NOx在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式:_______ 。
(3)Cu与稀硝酸反应制备NO的离子方程式_______ 。
(4)实验室常用铵盐和碱的混合物制取氨气,写出化学方程式_______
(5)设计实验检验铵盐溶液中的阳离子,写出实验操作、现象和结论。_______ 。
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:
(2)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。NOx在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式:
(3)Cu与稀硝酸反应制备NO的离子方程式
(4)实验室常用铵盐和碱的混合物制取氨气,写出化学方程式
(5)设计实验检验铵盐溶液中的阳离子,写出实验操作、现象和结论。
您最近一年使用:0次
解题方法
7 . 外观与氯化钠相似的亚硝酸钠NaNO2)在生活中应用十分广泛,如可用作建筑钢材缓蚀剂、肉制品发色剂等。
已知: ,
, 在溶液中呈棕色
在溶液中呈棕色

某学习小组设计如图装置制备亚硝酸钠(夹持及加热装置略去)。
(1)仪器a的名称为___________ ,为了使A中分液漏斗内的稀硝酸顺利滴下,可将分液漏斗上部的玻璃塞打开或___________ 。
(2)反应开始时先打开止水夹K,通入过量氮气,该操作的目的是___________ 。
(3)装置D中发生反应的实验现象是___________ 。
(4)如果取消B装置,D中固体产物除 外,可能含有副产物
外,可能含有副产物___________ 。
(5)取1 溶液(pH=0.5)2mL于试管中,用胶头滴管滴加1
溶液(pH=0.5)2mL于试管中,用胶头滴管滴加1
 溶液,溶液变黄后迅速变为棕色,再滴加KSCN溶液变红。
溶液,溶液变黄后迅速变为棕色,再滴加KSCN溶液变红。
①“溶液变黄后迅速变为棕色”的原因___________ 、___________ (用离子方程式表示)。
②取少量上述未加入KSCN溶液的棕色溶液于试管中,加热,有无色气体逸出,在试管口处变为红棕色,溶液中有红褐色沉淀生成,解释上述现象产生的原因___________ 。
已知:
 ,
, 在溶液中呈棕色
在溶液中呈棕色
某学习小组设计如图装置制备亚硝酸钠(夹持及加热装置略去)。
(1)仪器a的名称为
(2)反应开始时先打开止水夹K,通入过量氮气,该操作的目的是
(3)装置D中发生反应的实验现象是
(4)如果取消B装置,D中固体产物除
 外,可能含有副产物
外,可能含有副产物(5)取1
 溶液(pH=0.5)2mL于试管中,用胶头滴管滴加1
溶液(pH=0.5)2mL于试管中,用胶头滴管滴加1
 溶液,溶液变黄后迅速变为棕色,再滴加KSCN溶液变红。
溶液,溶液变黄后迅速变为棕色,再滴加KSCN溶液变红。①“溶液变黄后迅速变为棕色”的原因
②取少量上述未加入KSCN溶液的棕色溶液于试管中,加热,有无色气体逸出,在试管口处变为红棕色,溶液中有红褐色沉淀生成,解释上述现象产生的原因
您最近一年使用:0次
名校
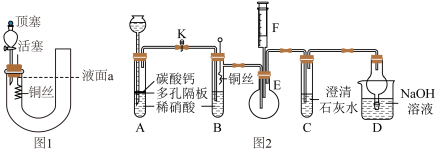
8 . 为了探究铜与稀硝酸反应产生的气体是NO,某课外活动小组设计了如下两套装置进行实验,请回答相关问题。
(1)如何检查该装置的气密性?___________ 。
(2)检验气密性后,重新组装好装置,打开分液漏斗的顶塞和活塞,从长管加入稀硝酸至液面到达a处,关闭活塞,微热短管,可观察到的实验现象为___________ 。
(二)乙同学设计了如图2所示装置(加热装置和固定装置均已略去)。装置气密性已检查,A中大理石,B、C、D中溶液均已装好,铜丝未浸入稀硝酸,止水夹K处于关闭状态,F是一半空的注射器。
(3)设计A装置的目的是___________ 。
(4)为达到上述目的应如何操作?___________ 。
(5)B装置中发生反应的离子方程式为___________ 。
(6)反应进行一段时间后,关闭止水夹K,将铜丝旋出稀硝酸液面。为验证铜和稀硝酸产生的气体是NO,应进行的操作和对应的现象是___________ 。
(1)如何检查该装置的气密性?
(2)检验气密性后,重新组装好装置,打开分液漏斗的顶塞和活塞,从长管加入稀硝酸至液面到达a处,关闭活塞,微热短管,可观察到的实验现象为
(二)乙同学设计了如图2所示装置(加热装置和固定装置均已略去)。装置气密性已检查,A中大理石,B、C、D中溶液均已装好,铜丝未浸入稀硝酸,止水夹K处于关闭状态,F是一半空的注射器。
(3)设计A装置的目的是
(4)为达到上述目的应如何操作?
(5)B装置中发生反应的离子方程式为
(6)反应进行一段时间后,关闭止水夹K,将铜丝旋出稀硝酸液面。为验证铜和稀硝酸产生的气体是NO,应进行的操作和对应的现象是
您最近一年使用:0次
9 . 氨氧化法是工业生产中制取硝酸的主要途径。某兴趣小组在实验室利用如下装置模拟氨氧化法制硝酸,通过观察装置 中溶液颜色变化检验硝酸的生成。
中溶液颜色变化检验硝酸的生成。

已知: 和
和 溶液不反应,
溶液不反应, 。
。
回答下列问题:
(1)组装好装置后,下一步应进行的操作为___________ 。装置B中的试剂名称为___________ 。
(2)实验时,点燃C中的酒精灯应在鼓入空气之___________ (填“前”或“后”),装置C中发生反应的化学方程式为___________ 。
(3)装置D的作用为___________ 。反应开始后,装置E中可观察到的现象为___________ 。
(4)将装置 替换为装置
替换为装置 更好,原因是
更好,原因是___________ 。
 中溶液颜色变化检验硝酸的生成。
中溶液颜色变化检验硝酸的生成。
已知:
 和
和 溶液不反应,
溶液不反应, 。
。回答下列问题:
(1)组装好装置后,下一步应进行的操作为
(2)实验时,点燃C中的酒精灯应在鼓入空气之
(3)装置D的作用为
(4)将装置
 替换为装置
替换为装置 更好,原因是
更好,原因是
您最近一年使用:0次
解题方法
10 . 某课外活动小组为了探究铜与稀硝酸反应产生的是 气体,设计了如下实验:
气体,设计了如下实验:

回答下列问题:
(1)仪器a的名称为_______ 。
(2)装置A制取 的目的是
的目的是_______ 。
(3)当_______ (填某装置中出现的实验现象)时,关闭K,将装置B中铜丝插入稀硝酸,并微热之,装置B中生成 时发生反应的离子方程式为
时发生反应的离子方程式为_______ 。
(4)验证装置B中生成的是 气体,某同学将注射器F中的空气推入装置E中,装置E中出现的实验现象为
气体,某同学将注射器F中的空气推入装置E中,装置E中出现的实验现象为_______ 。
(5)若产生的氮氧化物尾气用 溶液吸收,主要反应为
溶液吸收,主要反应为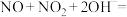
 。
。
①下列措施能提高 和
和 吸收率的是
吸收率的是_______ (填字母)。
A.微微加热装置B,加快气流速率
B.在实验过程中补充适量 溶液
溶液
C.在干燥管末端加一个多孔球泡
②实验结束时,装置内的 被完全吸收,若装置B中生成
被完全吸收,若装置B中生成 气体的体积为
气体的体积为 ,注射器内空气有
,注射器内空气有 (氧气体积按
(氧气体积按 计算),则最终生成的
计算),则最终生成的 的物质的量约为
的物质的量约为_______ (装置内气体的摩尔体积均视为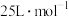 )。
)。
 气体,设计了如下实验:
气体,设计了如下实验:
回答下列问题:
(1)仪器a的名称为
(2)装置A制取
 的目的是
的目的是(3)当
 时发生反应的离子方程式为
时发生反应的离子方程式为(4)验证装置B中生成的是
 气体,某同学将注射器F中的空气推入装置E中,装置E中出现的实验现象为
气体,某同学将注射器F中的空气推入装置E中,装置E中出现的实验现象为(5)若产生的氮氧化物尾气用
 溶液吸收,主要反应为
溶液吸收,主要反应为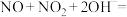
 。
。①下列措施能提高
 和
和 吸收率的是
吸收率的是A.微微加热装置B,加快气流速率
B.在实验过程中补充适量
 溶液
溶液C.在干燥管末端加一个多孔球泡
②实验结束时,装置内的
 被完全吸收,若装置B中生成
被完全吸收,若装置B中生成 气体的体积为
气体的体积为 ,注射器内空气有
,注射器内空气有 (氧气体积按
(氧气体积按 计算),则最终生成的
计算),则最终生成的 的物质的量约为
的物质的量约为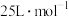 )。
)。
您最近一年使用:0次



