真题
名校
1 . 玻璃仪器内壁残留的硫单质可用热KOH溶液洗涤除去,发生如下反应:
3S+6KOH 2K2S+K2SO3+3H2O
2K2S+K2SO3+3H2O
(x-1)S+K2S K2Sx(x=2~6)
K2Sx(x=2~6)
S+ K2SO3 K2S2O3
K2S2O3
请计算:
(1)0.480 g硫单质与V mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成K2S和K2SO3,则V=______ 。
(2)2.560 g硫单质与60.0 mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成K2Sx和K2S2O3,则x=______ 。(写出计算过程)
3S+6KOH
 2K2S+K2SO3+3H2O
2K2S+K2SO3+3H2O(x-1)S+K2S
 K2Sx(x=2~6)
K2Sx(x=2~6)S+ K2SO3
 K2S2O3
K2S2O3请计算:
(1)0.480 g硫单质与V mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成K2S和K2SO3,则V=
(2)2.560 g硫单质与60.0 mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成K2Sx和K2S2O3,则x=
您最近一年使用:0次
2021-01-09更新
|
4106次组卷
|
12卷引用:2021年1月新高考浙江化学高考真题
2021年1月新高考浙江化学高考真题(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)考向02 物质的量浓度及其相关计算-备战2022年高考化学一轮复习考点微专题(已下线)专题18.化学计算-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)2021年1月浙江高考化学试题变式题26-31(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)浙江省金华市曙光学校2021-2022学年高三下学期5月模拟考试化学试题浙江省宁波市北仑中学2022-2023学年高一下学期期初返校考试化学(学考)试题(已下线)专题03 阿伏加德罗常数与化学计算 -2023年高考化学真题题源解密(新高考专用)浙江省宁波市鄞州中学(宁波鄞州蓝青高级中学)2023-2024学年高一上学期12月月考化学学科试题
解题方法
2 . 下列实验操作不能 达到实验目的是
| 选项 | 实验目的 | 实验操作 |
| A | 除去试管中附着的硫单质 | 加入适量氢氧化钠溶液并加热 |
| B | 配置银氨溶液 | 将氨水逐滴滴入硝酸银溶液至沉淀恰好溶解 |
| C | 比较HClO和CH3COOH的酸性强弱 | 常温下,用pH计分别测定浓度均为0.1 mol·L-1的NaClO溶液和CH3COONa 溶液的pH |
| D | 检验加碘盐中的碘元素 | 取适量加碘盐溶解后,滴加数滴淀粉溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . A是中学化学中常见的单质,B、C为化合物。它们有如图所示的转化关系(部分产物及反应条件省略)。下列判断正确的是


| A.A、B、C含有一种相同的元素 |
| B.A可能是金属,也可能是非金属 |
| C.A对应氧化物的水化物为强酸 |
| D.反应①②互为可逆反应 |
您最近一年使用:0次
2021-02-16更新
|
717次组卷
|
2卷引用:(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第一节 硫及其化合物
20-21高一下·全国·课时练习
名校
解题方法
4 . 下列说法中不正确的是( )
| A.在自然界中有游离态的硫存在 |
| B.试管内壁的硫粉可以用热的碱液除去 |
| C.硫与金属反应,生成低价态的金属化合物 |
| D.硫的氧化性比氯气的强 |
您最近一年使用:0次
2021-03-08更新
|
698次组卷
|
4卷引用:5.1.1 硫与二氧化硫(练好题)(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)
(已下线)5.1.1 硫与二氧化硫(练好题)(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)海南省儋州市第二中学2020-2021学年高一下学期3月月考化学试题河北省石家庄市元氏县第四中学2021-2022学年高一下学期月考化学试题天津市南开中学2022-2023学年高一下学期3月月考化学试题
5 . 为探究铁和硫反应产物中铁的化合价,某同学设计了如下实验过程:
Fe、S混合粉末 黑色固体
黑色固体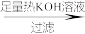 滤渣
滤渣 溶液A
溶液A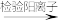 ……
……
已知:①铁和硫反应产物不溶于碱,能溶于硫酸;
②硫可溶于热碱溶液,发生类似Cl2和NaOH溶液的化学反应。
下列说法不正确的是
Fe、S混合粉末
 黑色固体
黑色固体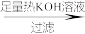 滤渣
滤渣 溶液A
溶液A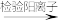 ……
……已知:①铁和硫反应产物不溶于碱,能溶于硫酸;
②硫可溶于热碱溶液,发生类似Cl2和NaOH溶液的化学反应。
下列说法不正确的是
| A.混合粉末应在N2氛围中进行加热,所用H2SO4溶液应先煮沸 |
| B.取溶液A,滴加KSCN溶液,未出现红色,可证明铁和硫反应只有+2价铁生成 |
| C.滤渣用稀H2SO4溶解时应在通风橱中进行 |
D.硫溶于热碱溶液可能发生的离子反应是3S+6OH-  2S2-+ 2S2-+ +3H2O +3H2O |
您最近一年使用:0次
6 . 氯化硫( )是一种橡胶硫化剂,可以利用它改变生橡胶热发粘,冷变硬的不良性能。实验室可以由氯气与熔化的硫反应制取
)是一种橡胶硫化剂,可以利用它改变生橡胶热发粘,冷变硬的不良性能。实验室可以由氯气与熔化的硫反应制取 ,装置(夹持和加热装置已省略)如图所示:
,装置(夹持和加热装置已省略)如图所示:

已知:① 和
和 反应生成
反应生成 ,同时有少量
,同时有少量 及其他氯化物生成。
及其他氯化物生成。
②常温下, 是一种浅黄色的油状液体,极易水解。
是一种浅黄色的油状液体,极易水解。
③ 的沸点为
的沸点为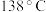 ,
, 的沸点为
的沸点为 ,硫的熔点为
,硫的熔点为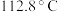 、沸点为
、沸点为 。
。
回答下列问题:
(1) 的电子式为
的电子式为_______ 。
(2)加热装置 时发生反应的离子方程式为
时发生反应的离子方程式为_______ 。装置 的作用为
的作用为_______ 。
(3)对装置 进行加热温度应控制在
进行加热温度应控制在_______ 之间。装置 除了有除去
除了有除去 和
和 尾气的作用之外,还有
尾气的作用之外,还有_______ 作用。
(4)已知 水解时,只有一种元素的化合价发生了变化,且被氧化和被还原的该元素的物质的量之比为
水解时,只有一种元素的化合价发生了变化,且被氧化和被还原的该元素的物质的量之比为 ,请写出该反应的化学方程式
,请写出该反应的化学方程式_______ 。
(5)实验结束时,装置 中烧瓶底部有少量硫附着,可用热的
中烧瓶底部有少量硫附着,可用热的 浓溶液洗涤,已知产物之一为
浓溶液洗涤,已知产物之一为 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
 )是一种橡胶硫化剂,可以利用它改变生橡胶热发粘,冷变硬的不良性能。实验室可以由氯气与熔化的硫反应制取
)是一种橡胶硫化剂,可以利用它改变生橡胶热发粘,冷变硬的不良性能。实验室可以由氯气与熔化的硫反应制取 ,装置(夹持和加热装置已省略)如图所示:
,装置(夹持和加热装置已省略)如图所示:
已知:①
 和
和 反应生成
反应生成 ,同时有少量
,同时有少量 及其他氯化物生成。
及其他氯化物生成。②常温下,
 是一种浅黄色的油状液体,极易水解。
是一种浅黄色的油状液体,极易水解。③
 的沸点为
的沸点为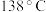 ,
, 的沸点为
的沸点为 ,硫的熔点为
,硫的熔点为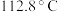 、沸点为
、沸点为 。
。回答下列问题:
(1)
 的电子式为
的电子式为(2)加热装置
 时发生反应的离子方程式为
时发生反应的离子方程式为 的作用为
的作用为(3)对装置
 进行加热温度应控制在
进行加热温度应控制在 除了有除去
除了有除去 和
和 尾气的作用之外,还有
尾气的作用之外,还有(4)已知
 水解时,只有一种元素的化合价发生了变化,且被氧化和被还原的该元素的物质的量之比为
水解时,只有一种元素的化合价发生了变化,且被氧化和被还原的该元素的物质的量之比为 ,请写出该反应的化学方程式
,请写出该反应的化学方程式(5)实验结束时,装置
 中烧瓶底部有少量硫附着,可用热的
中烧瓶底部有少量硫附着,可用热的 浓溶液洗涤,已知产物之一为
浓溶液洗涤,已知产物之一为 ,该反应的化学方程式为
,该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
7 . 关于硫的叙述正确的是
| A.硫单质质脆,微溶于酒精和二硫化碳 |
| B.硫的非金属性较强,在自然界中只以化合态存在 |
| C.硫单质与金属单质或非金属单质反应时都作氧化剂 |
| D.从硫的化合价角度分析,单质硫既具有氧化性又具有还原性 |
您最近一年使用:0次
2021-04-08更新
|
522次组卷
|
2卷引用:重庆市巴蜀中学2020-2021学年高一3月月考化学试题
名校
解题方法
8 . 把硫和强碱(如NaOH)加热至沸,反应后,硫转化为S2-和SO ,则反应的S和生成的S2-、SO
,则反应的S和生成的S2-、SO 的物质的量之比为
的物质的量之比为
 ,则反应的S和生成的S2-、SO
,则反应的S和生成的S2-、SO 的物质的量之比为
的物质的量之比为| A.2:1:1 | B.3:2:1 | C.3:1:2 | D.4:1:3 |
您最近一年使用:0次
解题方法
9 . 含钠化合物与含硫化合物可发生多种反应,请回答下列问题:
(1)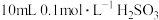 溶液与6.9gNa反应,生成的H2在标准状况下的体积为
溶液与6.9gNa反应,生成的H2在标准状况下的体积为___ L。
(2)SO2与少量NaOH溶液反应的离子方程式为___ 。
(3)查阅资料知Na2O2具有强氧化性,Na2O2与SO2反应的化学方程式为____ 。
(4)用热的NaOH溶液与硫粉反应中,氧化剂与还原剂的质量之比为___ ,当转移0.4mol电子时,生成Na2S的质量为___ g。
(1)
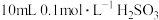 溶液与6.9gNa反应,生成的H2在标准状况下的体积为
溶液与6.9gNa反应,生成的H2在标准状况下的体积为(2)SO2与少量NaOH溶液反应的离子方程式为
(3)查阅资料知Na2O2具有强氧化性,Na2O2与SO2反应的化学方程式为
(4)用热的NaOH溶液与硫粉反应中,氧化剂与还原剂的质量之比为
您最近一年使用:0次
10 . 有关下列三个反应的叙述正确的是
①2H2S+SO2=3S↓+2H2O
②S+2H2SO4(浓)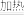 3SO2↑+2H2O
3SO2↑+2H2O
③3S+6KOH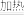 2K2S+K2SO3+3H2O
2K2S+K2SO3+3H2O
①2H2S+SO2=3S↓+2H2O
②S+2H2SO4(浓)
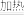 3SO2↑+2H2O
3SO2↑+2H2O③3S+6KOH
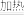 2K2S+K2SO3+3H2O
2K2S+K2SO3+3H2O| A.反应①说明SO2能与酸反应,具有碱性氧化物的性质 |
| B.反应②改用稀H2SO4,则能放出氢气 |
| C.反应②和③说明S具有两性元素的性质 |
| D.反应③中被氧化的硫元素与被还原的硫元素的质量之比为1∶2 |
您最近一年使用:0次
2020-09-02更新
|
513次组卷
|
10卷引用:黑龙江省绥化一中2020-2021学年高一下学期第一阶段考试化学试题
黑龙江省绥化一中2020-2021学年高一下学期第一阶段考试化学试题(已下线)4.2.1 含硫物质之间的转化(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)苏教版(2020)高一必修第一册专题4第二单元 硫及其化合物的相互转化鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第2节 硫的转化 课时3 硫和含硫化合物的相互转化高一必修第二册(人教2019版)第五章 第一节 硫及其化合物 课时3 不同价态含硫物质的转化河南省安阳市第二中学2021-2022学年高一下学期第一次段考化学试题天津市武清区2022-2023学年高一下学期7月期末化学试题第4课时 酸雨、不同价态硫元素间的转化(已下线)专题01 硫、氮及其化合物-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(天津专用)(已下线)综合 期末压轴80题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(天津专用)



