真题
名校
1 . 实验室由安息香制备二苯乙二酮的反应式如下:
装置示意图如下图所示,实验步骤为:
①在圆底烧瓶中加入 冰乙酸、
冰乙酸、 水及
水及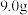
 ,边搅拌边加热,至固体全部溶解。
,边搅拌边加热,至固体全部溶解。
②停止加热,待沸腾平息后加入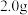 安息香,加热回流
安息香,加热回流 。
。
③加入 水,煮沸后冷却,有黄色固体析出。
水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用 的乙醇重结晶,干燥后得淡黄色结晶
的乙醇重结晶,干燥后得淡黄色结晶 。
。
(1)仪器A中应加入_______ (填“水”或“油”)作为热传导介质。
(2)仪器B的名称是_______ ;冷却水应从_______ (填“a”或“b”)口通入。
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是_______ 。
(4)在本实验中, 为氧化剂且过量,其还原产物为
为氧化剂且过量,其还原产物为_______ ;某同学尝试改进本实验:采用催化量的 并通入空气制备二苯乙二酮。该方案是否可行
并通入空气制备二苯乙二酮。该方案是否可行_______ ?简述判断理由_______ 。
(5)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是_______ 。
(6)若粗品中混有少量未氧化的安息香,可用少量_______ 洗涤的方法除去(填标号)。若要得到更高纯度的产品,可用重结晶的方法进一步提纯。
a.热水 b.乙酸 c.冷水 d.乙醇
(7)本实验的产率最接近于_______ (填标号)。
a. b.
b. c.
c. d.
d.
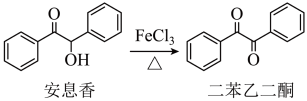
| 物质 | 性状 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 安息香 | 白色固体 | 133 | 344 | 难溶于冷水 溶于热水、乙醇、乙酸 |
| 二苯乙二酮 | 淡黄色固体 | 95 | 347 | 不溶于水 溶于乙醇、苯、乙酸 |
| 冰乙酸 | 无色液体 | 17 | 118 | 与水、乙醇互溶 |
①在圆底烧瓶中加入
 冰乙酸、
冰乙酸、 水及
水及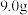
 ,边搅拌边加热,至固体全部溶解。
,边搅拌边加热,至固体全部溶解。②停止加热,待沸腾平息后加入
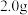 安息香,加热回流
安息香,加热回流 。
。③加入
 水,煮沸后冷却,有黄色固体析出。
水,煮沸后冷却,有黄色固体析出。④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用
 的乙醇重结晶,干燥后得淡黄色结晶
的乙醇重结晶,干燥后得淡黄色结晶 。
。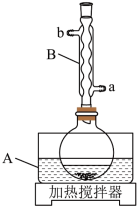
(1)仪器A中应加入
(2)仪器B的名称是
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是
(4)在本实验中,
 为氧化剂且过量,其还原产物为
为氧化剂且过量,其还原产物为 并通入空气制备二苯乙二酮。该方案是否可行
并通入空气制备二苯乙二酮。该方案是否可行(5)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是
(6)若粗品中混有少量未氧化的安息香,可用少量
a.热水 b.乙酸 c.冷水 d.乙醇
(7)本实验的产率最接近于
a.
 b.
b. c.
c. d.
d.
您最近一年使用:0次
2023-06-10更新
|
16256次组卷
|
15卷引用:湖南省株洲市第一中学2021届高三下学期第三次模拟检测化学试题
湖南省株洲市第一中学2021届高三下学期第三次模拟检测化学试题2023年高考新课标理综化学真题(已下线)T27-实验题(已下线)2023年高考化学真题完全解读(新课标卷:适用安徽、云南、山西、吉林、黑龙江五省)(PPT+Word)(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)T27-实验题(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)广东省广州市第二中学2022-2023学年高二下学期期末考试化学试题(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)江西省宜春市丰城中学2023-2024学年高二上学期12月月考化学试题(已下线)题型三 以分离提纯为主的有机制备类实验-备战2024年高考化学答题技巧与模板构建山东省东营市利津县高级中学2023-2024学年高二下学期5月月考化学试题
2 . 下列过程中的化学反应,相应的离子方程式正确的是
A.用碳酸钠溶液处理水垢中的硫酸钙: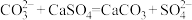 |
B.过量铁粉加入稀硝酸中: |
C.硫酸铝溶液中滴加少量氢氧化钾溶液: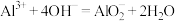 |
D.氯化铜溶液中通入硫化氢: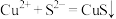 |
您最近一年使用:0次
2021-06-09更新
|
27408次组卷
|
67卷引用:2021年高考全国乙卷化学真题
2021年高考全国乙卷化学真题河南省三门峡市实验高中2020-2021学年高二下学期6月月考化学试题河北省石家庄一中2020-2021学年高二下学期期末考试化学试题(已下线)课时05 电解质与离子方程式-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点04 离子反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点04 离子反应-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第4讲 离子反应 (讲)— 2022年高考化学一轮复习讲练测(新教材新高考)宁夏中卫市中宁县第一中学2021-2022学年高三上学期第一次月考化学试题江西省赣州市第十四中学2022届高三上学期第二次月考化学试题重庆市开州中学高 2021-2022学年高三上学期10月月考化学试题江西省宜春市第九中学2021-2022学年高三上学期10月月考化学试题陕西省西安中学2022届高三上学期第一次月考化学试题福建省福清西山学校2021-2022学年高三上学期10月月考化学试题(已下线)考点03 离子反应-备战2022年高考化学学霸纠错(全国通用)(已下线)2021年高考全国乙卷化学试题变式题广东省河源正德中学2021-2022学年高二上学期第一次段考化学试题(已下线)解密04 离子反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)新疆石河子第一中学2021-2022学年高三上学期8月月考(A卷)化学试题云南省峨山彝族自治县第一中学2021-2022学年高二上学期12月月考化学试题安徽省亳州市第五完全中学2021-2022学年高三上学期期中考试化学试题山东省临沂市兰陵县第四中学2021-2022学年高三12月月考化学试题内蒙古巴彦淖尔市临河区第三中学2021-2022学年高三上学期第二次阶段性测试理综化学试题天津市实验中学滨海学校黄南民族班2021-2022学年高三上学期期中质量监测化学试题(已下线)专题04 离子反应-2022年高考化学二轮复习重点专题常考点突破练(已下线)解密04 离子反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)专题08 化学方程式正误判断—2022年高考化学二轮复习讲练测(全国版)-讲义陕西省咸阳市武功县普集高级中学2021-2022学年高三上学期期末考试化学试题(已下线)卷11 溶液中的离子平衡-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)卷03 离子方程式正误判断-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)秘籍03 化学用语-备战2022年高考化学抢分秘籍(全国通用)(已下线)查补易混易错点04 离子反应-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题03离子反应-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题03离子反应-五年(2018~2022)高考真题汇编(全国卷)(已下线)第03练 用分类思想突破离子反应-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)考点04 离子反应-备战2023年高考化学一轮复习考点帮(全国通用)江西省景德镇市乐平中学2021-2022学年高二下学期期末质量检测化学试题(已下线)第02讲 离子反应(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)微专题06 “四型和四法”破解与量有关离子方程式书写-备战2023年高考化学一轮复习考点微专题(已下线)微专题05 破解“六大陷阱”突破离子方程式书写正误判断-备战2023年高考化学一轮复习考点微专题(已下线)第02练 离子反应-2023年高考化学一轮复习小题多维练(全国通用)陕西省咸阳市武功县普集高级中学2022-2023学年高三上学期第一次月考化学试题 (已下线)专题03 离子反应方程式和离子共存 (练)-2023年高考化学二轮复习讲练测(新高考专用)黑龙江省哈尔滨市第一二二中学2021-2022学年高三假期检验性考试化学试题安徽省六安市裕安区新安中学2022-2023学年高三上学期第三次月考化学试题(已下线)专题04 突破离子共存、离子推断、离子方程式正误判断(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)第一部分 二轮专题突破 专题3 离子方程式的书写及正误判断(已下线)第一章 化学物质及其变化 第2练 离子反应 离子方程式(已下线)题型10 离子方程式正误的判断(已下线)专题卷05 离子方程式正误判断-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)第2讲 离子反应 离子方程式(已下线)专题04 离子反应(已下线)专题04 离子反应(已下线)微专题 与量有关的离子方程式的书写(已下线)第04练 离子共存 离子方程式的正误判断 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点04 离子反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题12 水溶液中的离子反应与平衡-2023年高考化学真题题源解密(全国通用)黑龙江省哈尔滨市第三十二中学校2023-2024学年高三上学期9月月考化学试题四川省江油中学2023-2024学年高三上学期9月月考理科综合化学试题四川省攀枝花市第十五中学校2023-2024学年高三上学期8月考试化学试题安徽省安庆市第一中学龙山校区2021-2022学年高一下学期3月阶段性考试化学试题北京工业大学附属中学2022-2023学年高三上学期开学测试化学试题山东省聊城颐中外国语学校2023-2024学年高三上学期期中考试化学试题湖南省邵东市第三中学2023-2024学年高二上学期1月期末考试化学试卷 甘肃省平凉市泾川县第三中学2023-2024学年高三上学期第3次月考化学试题新疆喀什市第五中学2023-2024学年高三上学期12月大联考化学预测卷(已下线)第02讲 离子反应、离子方程式(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)天津市耀华中学2023-2024学年高一下学期开学考试化学学科试题
3 . 磁选后的炼铁高钛炉渣,主要成分有 、
、 、
、 、
、 、
、 以及少量的
以及少量的 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。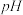 见下表
见下表
回答下列问题:
(1)“焙烧”中, 、
、 几乎不发生反应,
几乎不发生反应, 、
、 、
、 、
、 转化为相应的硫酸盐,写出
转化为相应的硫酸盐,写出 转化为
转化为 的化学方程式
的化学方程式_______ 。
(2)“水浸”后“滤液”的 约为2.0,在“分步沉淀”时用氨水逐步调节
约为2.0,在“分步沉淀”时用氨水逐步调节 至11.6,依次析出的金属离子是
至11.6,依次析出的金属离子是_______ 。
(3)“母液①"中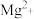 浓度为
浓度为_______  。
。
(4)“水浸渣”在160℃“酸溶”最适合的酸是_______ 。“酸溶渣”的成分是_______ 、_______ 。
(5)“酸溶”后,将溶液适当稀释并加热, 水解析出
水解析出 沉淀,该反应的离子方程式是
沉淀,该反应的离子方程式是_______ 。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得_______ ,循环利用。
 、
、 、
、 、
、 、
、 以及少量的
以及少量的 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。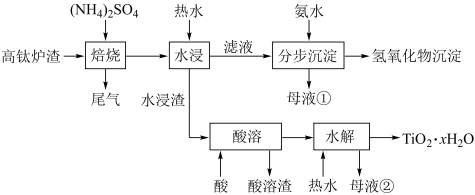
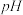 见下表
见下表| 金属离子 |  |  |  |  |
开始沉淀的 | 2.2 | 3.5 | 9.5 | 12.4 |
沉淀完全 的 的 | 3.2 | 4.7 | 11.1 | 13.8 |
(1)“焙烧”中,
 、
、 几乎不发生反应,
几乎不发生反应, 、
、 、
、 、
、 转化为相应的硫酸盐,写出
转化为相应的硫酸盐,写出 转化为
转化为 的化学方程式
的化学方程式(2)“水浸”后“滤液”的
 约为2.0,在“分步沉淀”时用氨水逐步调节
约为2.0,在“分步沉淀”时用氨水逐步调节 至11.6,依次析出的金属离子是
至11.6,依次析出的金属离子是(3)“母液①"中
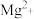 浓度为
浓度为 。
。(4)“水浸渣”在160℃“酸溶”最适合的酸是
(5)“酸溶”后,将溶液适当稀释并加热,
 水解析出
水解析出 沉淀,该反应的离子方程式是
沉淀,该反应的离子方程式是(6)将“母液①”和“母液②”混合,吸收尾气,经处理得
您最近一年使用:0次
2021-06-09更新
|
27328次组卷
|
56卷引用:2021年高考全国乙卷化学真题
2021年高考全国乙卷化学真题吉林省长春外国语学校2020-2021学年高二下学期第二次月考化学试题河南省三门峡市实验高中2020-2021学年高二下学期6月月考化学试题(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点31 化学实验与工艺流程-备战2022年高考化学一轮复习考点帮(浙江专用)广东省深圳市第七高级中学2022届高三第一次月考化学试卷(已下线)专题讲座(六)化工流程的解题策略(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第12周 周测卷-备战2022年高考化学周测与晚练(新高考专用)内蒙古北京八中乌兰察布分校2021-2022学年高三上学期学科素养评估一化学试题(已下线)专题06 常见金属及其化合物-备战2022年高考化学学霸纠错(全国通用)(已下线)2021年高考全国乙卷化学试题变式题黑龙江省牡丹江市第一高级中学2021-2022学年高二上学期期中考试化学试题 (已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)武汉市第一中学2021-2022学年高三上学期10月月考化学试题(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)专题11 无机工艺流程题—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)押全国卷理综第27题 工业流程-备战2022年高考化学临考题号押题(全国卷)(已下线)回归教材重难点08 化学工艺流程分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)安徽省青阳县第一中学2021-2022学年高二下学期5月月考化学试题(已下线)专题16工艺流程题-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题16工艺流程题-五年(2018~2022)高考真题汇编(全国卷)(已下线)2022年湖南卷高考真题变式题(15-19)(已下线)2022年全国甲卷高考真题变式题(非选择题)广东省揭阳市普宁市华侨中学2021-2022学年高二下学期第三次月考化学试题(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)微专题28 有关工艺流程和实验探究方程式的书写-备战2023年高考化学一轮复习考点微专题西藏自治区拉萨中学2022届高三第六次月考理综化学试题(已下线)第09讲 无机非金属材料(讲)-2023年高考化学一轮复习讲练测(新教材新高考)湖南省衡南县第一中学2022届高三下学期第二次模考化学试题湖南省邵阳市第一中学2022届高三下学期第三次模拟考试化学试题新疆岳普湖县2021-2022学年高一下学期第一次学情调研测试化学试题(已下线)2022年北京高考真题变式题15-19江西省瑞金市第二中学2022-2023学年高三上学期开学考试化学试题(已下线)易错点25 盐类水解-备战2023年高考化学考试易错题河南省洛阳市新安县第一高级中学2022-2023学年高三上学期入学测试(实验小班)化学试题第二部分 热点专项突破——解题能力稳提升 专项1 物质制备类的工艺流程 热点2 以废水、废渣、废气等为原料的工艺流程(已下线)专题29 无机化工流程综合分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第八章 水溶液中的离子反应与平衡 第55讲 无机化工流程题的解题策略(已下线)题型141 Ksp的相关计算(已下线)专题01 工艺流程专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)(已下线)2022年北京高考真题化学试题变式题(工业流程题)(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题福建省永春第一中学2022-2023学年高二下学期6月月考化学试题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)章末综合评价(八)黑龙江省哈尔滨市第三十二中学校2023-2024学年高三上学期11月期中考试化学试题四川省眉山市彭山区第一中学2023-2024学年高三上学期11月月考理综试题2024新东方高一上期末考化学01陕西省渭南市蒲城县尧山中学2023-2024学年高三下学期开学收心考试理综试题-高中化学山东省日照神州天立高级中学高复部2023-2024学年高三上学期12月份阶段性测试化学试题四川省成都锦江区嘉祥外国语高级中学2023-2024学年高三下学期第一次诊断性考试理科综合试题-高中化学2024年辽宁省锦州市渤海大学附属高级中学模拟化学试题四川省攀枝花市第十五中学校2023-2024学年高三上学期第3次统一考试理科综合-高中化学
真题
名校
4 . 一种活性物质的结构简式为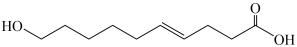 ,下列有关该物质的叙述正确的是
,下列有关该物质的叙述正确的是
| A.能发生取代反应,不能发生加成反应 |
| B.既是乙醇的同系物也是乙酸的同系物 |
C.与 互为同分异构体 互为同分异构体 |
D. 该物质与碳酸钠反应得 该物质与碳酸钠反应得 |
您最近一年使用:0次
2021-06-09更新
|
27695次组卷
|
64卷引用:2021年高考全国乙卷化学真题
2021年高考全国乙卷化学真题陕西省榆林市清源中学2020-2021学年高二下学期第二次月考化学试题广西南宁市邕宁高中2020-2021学年高一下学期期末考试化学试题湖南省岳阳县第一中学2020-2021年高一下学期期末考试化学试题安徽省滁州市定远县育才学校2020-2021学年高二下学期期末考试化学试题(已下线)考点38 烃的含氧衍生物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点39 醛 羧酸 酯-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第十一章能力提升检测卷(精练)-2022年一轮复习讲练测(已下线)课时59 醇和酚-2022年高考化学一轮复习小题多维练(全国通用)四川省成都外国语学校2021-2022学年高二上学期入学考试化学试题吉林省吉林市第二中学2020-2021学年高二下学期期末考试化学试题(已下线)【苏州新东方】 江苏省吴江中学2021-2022学年高二上学期开学检测化学试卷宁夏中卫市中宁县第一中学2021-2022学年高三上学期第一次月考化学试题湖南省邵阳邵东市第一中学2022届高三上学期第一次月考化学试题重庆市开州中学高 2021-2022学年高三上学期10月月考化学试题天津市耀华中学2021-2022学年高三上学期第一次月考化学试题(已下线)专题08 常见有机物及其应用-备战2022年高考化学学霸纠错(全国通用)(已下线)第25讲 烃 有机高分子材料(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)2021年高考全国乙卷化学试题变式题江苏省徐州市铜山区2021-2022学年高二上学期期中考试(选择考)化学试题北京市第二十二中学2021-2022学年高三上学期期中考试化学试题云南省峨山彝族自治县第一中学2021-2022学年高二上学期12月月考化学试题(已下线)第35讲 烃的衍生物(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)上海市徐汇区2022届高三一模化学试题(已下线)解密12 有机化学基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)专题03 常见有机物的性质及应用—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)解密12 有机化学基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题08 有机化学基础(必修)-2022年高考化学二轮复习重点专题常考点突破练(已下线)卷07 有机物的结构、性质及应用-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)秘籍06 有机物结构与性质-备战2022年高考化学抢分秘籍(全国通用)云南省丽江市第一高级中学2021-2022学年高二下学期4月月考化学试题(已下线)押全国卷理综第8题 有机化学基础(选择题)-备战2022年高考化学临考题号押题(课标全国卷)(已下线)查补易混易错点07 常见有机化合物及其应用-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)河南省周口市文昌中学2021-2022学年高二下学期第三次调研考试化学试题(已下线)专题13有机化合物-五年(2018~2022)高考真题汇编(全国卷)河南省郑州市第四高级中学2021-2022学年高一下学期第三次调研考试化学试题上海南汇中学2021-2022学年高三下学期阶段考试化学试题(已下线)专题13有机化合物-三年(2020~2022)高考真题汇编(全国卷)湖南省郴州市2021-2022学年高一下学期期末考试化学试题(已下线)考点36 醇 酚-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第54练 羧酸与羧酸衍生物-2023年高考化学一轮复习小题多维练(全国通用)第三~五节综合拔高练安徽省砀山县第四中学2022-2023学年高三上学期第一次月考化学试题山东省菏泽市单县第二中学2021-2022学年高三下学期开学考试化学试题(已下线)第32讲 有机化合物的结构特点与研究方法(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第34讲 烃的衍生物(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第34讲 烃的衍生物(讲)-2023年高考化学一轮复习讲练测(新教材新高考)云南省昭通市昭阳区第二中学2021-2022学年高二下学期期末考试化学试题上海市虹口区复兴高级中学2022-2023学年高三上学期期中考试化学试题(已下线)【知识图鉴】单元讲练测必修第二册第七单元01讲核心(已下线)第一部分 二轮专题突破 专题19 有机选择题题型分析上海市实验学校2023届高三下学期3月月考化学试题(已下线)专题卷18 结构给予型多官能团有机物分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)题型11 陌生有机物结构与性质推断-高考必备50个题型(已下线)专题11 有机化学基础(已下线)专题11 有机化学基础四川省广元中学2022-2023学年高二下学期5月期中考试化学试题福建省永春第一中学2022-2023学年高二下学期6月月考化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高二下学期期末考试化学试题(已下线)专题06 有机物的结构与性质-2023年高考化学真题题源解密(全国通用)(已下线)考点35 烃的含氧衍生物(醇、酚、醛、酮)(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)河南省焦作市博爱县第一中学2023届高三下学期三模化学试题(已下线)第4讲 醛、酮、羧酸和羧酸衍生物河南省济源英才学校2023-2024学年高三上学期11月月考 化学试卷
5 . 一氯化碘(ICl)是一种卤素互化物,具有强氧化性,可与金属直接反应,也可用作有机合成中的碘化剂。回答下列问题:
(1)历史上海藻提碘中得到一种红棕色液体,由于性质相似,Liebig误认为是ICl,从而错过了一种新元素的发现,该元素是_______ 。
(2)氯铂酸钡(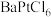 )固体加热时部分分解为
)固体加热时部分分解为 、
、 和
和 ,376.8℃时平衡常数
,376.8℃时平衡常数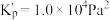 ,在一硬质玻璃烧瓶中加入过量
,在一硬质玻璃烧瓶中加入过量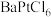 ,抽真空后,通过一支管通入碘蒸气(然后将支管封闭),在376.8℃,碘蒸气初始压强为
,抽真空后,通过一支管通入碘蒸气(然后将支管封闭),在376.8℃,碘蒸气初始压强为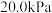 。376.8℃平衡时,测得烧瓶中压强为
。376.8℃平衡时,测得烧瓶中压强为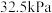 ,则
,则
_______  ,反应
,反应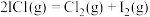 的平衡常数K=
的平衡常数K=_______ (列出计算式即可)。
(3)McMorris测定和计算了在136~180℃范围内下列反应的平衡常数 。
。
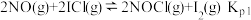

得到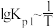 和
和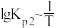 均为线性关系,如下图所示:
均为线性关系,如下图所示:

①由图可知,NOCl分解为NO和 反应的
反应的
_______ 0(填“大于”或“小于”)
②反应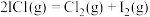 的K=
的K=_______ (用 、
、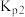 表示):该反应的
表示):该反应的
_______ 0(填“大于”或“小于”),写出推理过程_______ 。
(4)Kistiakowsky曾研究了NOCl光化学分解反应,在一定频率(v)光的照射下机理为:
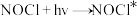

其中 表示一个光子能量,
表示一个光子能量,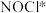 表示NOCl的激发态。可知,分解1mol的NOCl需要吸收
表示NOCl的激发态。可知,分解1mol的NOCl需要吸收_______ mol光子。
(1)历史上海藻提碘中得到一种红棕色液体,由于性质相似,Liebig误认为是ICl,从而错过了一种新元素的发现,该元素是
(2)氯铂酸钡(
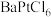 )固体加热时部分分解为
)固体加热时部分分解为 、
、 和
和 ,376.8℃时平衡常数
,376.8℃时平衡常数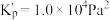 ,在一硬质玻璃烧瓶中加入过量
,在一硬质玻璃烧瓶中加入过量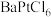 ,抽真空后,通过一支管通入碘蒸气(然后将支管封闭),在376.8℃,碘蒸气初始压强为
,抽真空后,通过一支管通入碘蒸气(然后将支管封闭),在376.8℃,碘蒸气初始压强为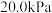 。376.8℃平衡时,测得烧瓶中压强为
。376.8℃平衡时,测得烧瓶中压强为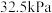 ,则
,则
 ,反应
,反应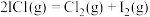 的平衡常数K=
的平衡常数K=(3)McMorris测定和计算了在136~180℃范围内下列反应的平衡常数
 。
。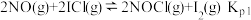

得到
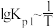 和
和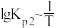 均为线性关系,如下图所示:
均为线性关系,如下图所示:
①由图可知,NOCl分解为NO和
 反应的
反应的
②反应
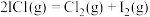 的K=
的K= 、
、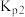 表示):该反应的
表示):该反应的
(4)Kistiakowsky曾研究了NOCl光化学分解反应,在一定频率(v)光的照射下机理为:
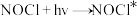

其中
 表示一个光子能量,
表示一个光子能量,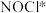 表示NOCl的激发态。可知,分解1mol的NOCl需要吸收
表示NOCl的激发态。可知,分解1mol的NOCl需要吸收
您最近一年使用:0次
2021-06-09更新
|
22009次组卷
|
18卷引用:2021年高考全国乙卷化学真题
2021年高考全国乙卷化学真题吉林省长春外国语学校2020-2021学年高二下学期第二次月考化学试题(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)2021年高考全国乙卷化学试题变式题(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题12 化学反应原理综合题—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)回归教材重难点09 化学反应原理综合-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)押全国卷理综第28题 化学反应原理-备战2022年高考化学临考题号押题(课标全国卷)(已下线)专题15化学反应原理综合-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题15化学反应原理综合-五年(2018~2022)高考真题汇编(全国卷)(已下线)考点23 化学平衡常数-备战2023年高考化学一轮复习考点帮(全国通用)河南省平顶山市汝州第一高级中学2022-2023学年高二10月月考化学试题(已下线)专题05 反应原理专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)(已下线)专题17 原理综合题(已下线)专题17 原理综合题(已下线)专题15 化学反应原理综合题-2023年高考化学真题题源解密(全国通用)
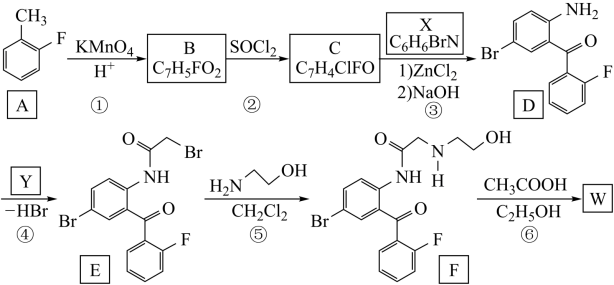
6 . 卤沙唑仑W是一种抗失眠药物,在医药工业中的一种合成方法如下:
(1)A的化学名称是_______ 。
(2)写出反应③的化学方程式_______ 。
(3)D具有的官能团名称是_______ 。(不考虑苯环)
(4)反应④中,Y的结构简式为_______ 。
(5)反应⑤的反应类型是_______ 。
(6)C的同分异构体中,含有苯环并能发生银镜反应的化合物共有_______ 种。
(7)写出W的结构简式_______ 。
已知:(ⅰ)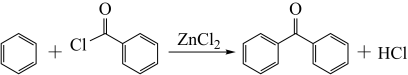
(ⅱ)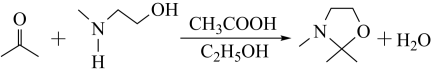
(1)A的化学名称是
(2)写出反应③的化学方程式
(3)D具有的官能团名称是
(4)反应④中,Y的结构简式为
(5)反应⑤的反应类型是
(6)C的同分异构体中,含有苯环并能发生银镜反应的化合物共有
(7)写出W的结构简式
您最近一年使用:0次
2021-06-09更新
|
25425次组卷
|
30卷引用:2021年高考全国乙卷化学真题
2021年高考全国乙卷化学真题(已下线)考点40 有机合成高分子-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点41 合成高分子 有机合成-备战2022年高考化学一轮复习考点帮(浙江专用)吉林省吉林市第二中学2020-2021学年高二下学期期末考试化学试题湖南省邵阳邵东市第一中学2022届高三上学期第一次月考化学试题(已下线)专题15 有机化学基础-备战2022年高考化学学霸纠错(全国通用)(已下线)2021年高考全国乙卷化学试题变式题2021年广东省高考化学试卷变式题11-21(已下线)2021年6月浙江高考化学试题变式题26-312021年辽宁高考化学试题变式题11-192020年全国卷Ⅰ理综化学高考真题变式题(已下线)解密12 有机化学基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密12 有机化学基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题20 有机化学基础-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题14 有机化学基础—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)回归教材重难点12 有机化学基础(选考)-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)押全国卷理综第36题 有机化学基础-备战2022年高考化学临考题号押题(课标全国卷)(已下线)专题19有机化学基础(选修)-五年(2018~2022)高考真题汇编(全国卷)湖南省常德市石门县第一中学2022届高三下学期月考化学试题(已下线)微专题48 限定条件下的同分异构体的书写判断-备战2023年高考化学一轮复习考点微专题(已下线)专题32 有机推断及合成-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)2022年福建省高考真题变式题(有机综合题)(已下线)第五部分 有机合成流程 综合提能训练(已下线)专题04 有机化学专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)(已下线)专题21 有机推断题(已下线)专题21 有机推断题(已下线)专题17 有机化学基础综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点39 有机推断(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)2024届河南省郑州市第一中学高三下学期考前全真模拟考试理科综合试题-高中化学2024届陕西省西安市第一中学高三下学期第十六次模拟考试理综试题-高中化学
7 . 卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)氟原子激发态的电子排布式有_______ ,其中能量较高的是_______ 。(填标号)
a. b.
b. c.
c.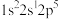 d.
d.
(2)①一氯乙烯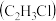 分子中,C的一个
分子中,C的一个_______ 杂化轨道与Cl的 轨道形成
轨道形成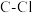
_______ 键,并且Cl的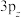 轨道与C的
轨道与C的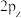 轨道形成3中心4电子的大
轨道形成3中心4电子的大 键
键 。
。
②一氯乙烷 、一氯乙烯
、一氯乙烯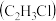 、一氯乙炔
、一氯乙炔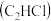 分子中,
分子中,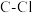 键长的顺序是
键长的顺序是_______ ,理由:(ⅰ)C的杂化轨道中s成分越多,形成的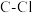 键越强;(ⅱ)
键越强;(ⅱ)_______ 。
(3)卤化物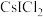 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为
受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为_______ 。解释X的熔点比Y高的原因_______ 。
(4)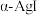 晶体中
晶体中 离子作体心立方堆积(如图所示),
离子作体心立方堆积(如图所示), 主要分布在由
主要分布在由 构成的四面体、八面体等空隙中。在电场作用下,
构成的四面体、八面体等空隙中。在电场作用下, 不需要克服太大的阻力即可发生迁移。因此,
不需要克服太大的阻力即可发生迁移。因此,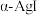 晶体在电池中可作为
晶体在电池中可作为_______ 。
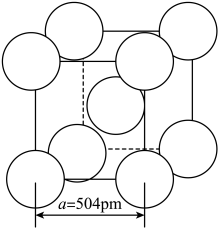
已知阿伏加德罗常数为 ,则
,则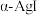 晶体的摩尔体积
晶体的摩尔体积
_______  (列出算式)。
(列出算式)。
(1)氟原子激发态的电子排布式有
a.
 b.
b. c.
c.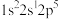 d.
d.
(2)①一氯乙烯
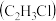 分子中,C的一个
分子中,C的一个 轨道形成
轨道形成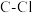
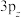 轨道与C的
轨道与C的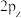 轨道形成3中心4电子的大
轨道形成3中心4电子的大 键
键 。
。②一氯乙烷
 、一氯乙烯
、一氯乙烯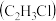 、一氯乙炔
、一氯乙炔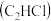 分子中,
分子中,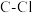 键长的顺序是
键长的顺序是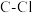 键越强;(ⅱ)
键越强;(ⅱ)(3)卤化物
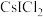 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为
受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为(4)
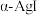 晶体中
晶体中 离子作体心立方堆积(如图所示),
离子作体心立方堆积(如图所示), 主要分布在由
主要分布在由 构成的四面体、八面体等空隙中。在电场作用下,
构成的四面体、八面体等空隙中。在电场作用下, 不需要克服太大的阻力即可发生迁移。因此,
不需要克服太大的阻力即可发生迁移。因此,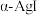 晶体在电池中可作为
晶体在电池中可作为
已知阿伏加德罗常数为
 ,则
,则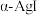 晶体的摩尔体积
晶体的摩尔体积
 (列出算式)。
(列出算式)。
您最近一年使用:0次
2022-06-09更新
|
20300次组卷
|
18卷引用:专题九 物质结构与性质-实战高考·二轮复习核心突破
(已下线)专题九 物质结构与性质-实战高考·二轮复习核心突破2022年高考全国乙卷化学真题(已下线)专题18物质结构与性质(选修)-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题17物质结构与性质(综合题)-2022年高考真题+模拟题汇编(全国卷)(已下线)专题18物质结构与性质(选修)-五年(2018~2022)高考真题汇编(全国卷)(已下线)2022年全国乙卷高考变式题(非选择题)(已下线)第19练 物质结构与性质综合题难点突破-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)专题17 物质结构与性质综合题-备战2023年高考化学母题题源解密(全国通用)(已下线)专题19 物质结构与性质综合题-备战2023年高考化学母题题源解密(广东卷)河北省石家庄市第四十三中学2022-2023学年高三上学期10月月考化学试题(已下线)第一部分 二轮专题突破 大题突破4 物质结构与性质大题研究(选考)(已下线)题型11 物质结构与性质的综合分析与推断(已下线)专题02 物质结构专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)(已下线)专题20 结构与性质(已下线)专题20 结构与性质(已下线)第21练 物质结构与性质综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)专题17 物质结构与性质综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题16 物质结构与性质综合题-2023年高考化学真题题源解密(全国通用)
8 . 已知相同温度下, 。某温度下,饱和溶液中
。某温度下,饱和溶液中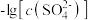 、
、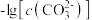 、与
、与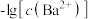 的关系如图所示。
的关系如图所示。
 。某温度下,饱和溶液中
。某温度下,饱和溶液中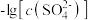 、
、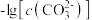 、与
、与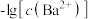 的关系如图所示。
的关系如图所示。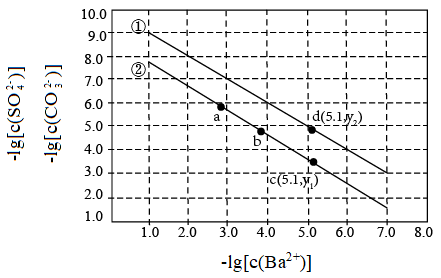
A.曲线①代表 的沉淀溶解曲线 的沉淀溶解曲线 |
B.该温度下 的 的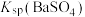 值为 值为 |
C.加适量 固体可使溶液由a点变到b点 固体可使溶液由a点变到b点 |
D. 时两溶液中 时两溶液中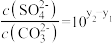 |
您最近一年使用:0次
2021-06-11更新
|
25698次组卷
|
71卷引用:2021年高考全国甲卷化学真题
2021年高考全国甲卷化学真题重庆市缙云教育联盟2020-2021学年高二下学期期末质量检测化学试题(已下线)第八章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)湖南省邵阳邵东市第一中学2022届高三上学期第一次月考化学试题河北省石家庄市第一中学2021-2022学年高二上学期10月月考化学试卷(已下线)第24讲 沉淀溶解平衡(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)辽宁省东北育才学校2021-2022学年高二上学期期中考试化学试题河北省石家庄市第二中学2022届高三上学期11月第三次考试化学试题(已下线)2021年高考全国甲卷化学试题变式题(已下线)专题27 难溶电解质的溶解平衡(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)专题12 水溶液中的离子平衡-备战2022年高考化学学霸纠错(全国通用)(已下线)第八单元 水溶液中的离子平衡(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)浙江省绍兴市诸暨中学2021-2022学年高二上学期期中考试(实验班)化学试题浙江省绍兴市诸暨中学2021-2022学年高二上学期期中考试(平行班)化学试题福建省三明第一中学2021-2022学年高二上学期第二次月考化学试题云南省大理白族自治州实验中学2021-2022学年高二上学期10月月考化学试题(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题13 水溶液中的离子平衡-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题07 电解质溶液—2022年高考化学二轮复习讲练测(全国版)-练习山东省泰安市2021-2022学年高三下学期3月一模考试化学试题吉林省长春市2022届高三质量监测线上考试(三)理综化学试题(已下线)卷11 溶液中的离子平衡-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)卷09 水溶液中的离子平衡-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)【奋进985】08-备战2022年高考化学名校进阶模拟卷(通用版)云南省丽江市第一高级中学2021-2022学年高二下学期4月月考化学试题(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(全国卷)(已下线)回归教材重难点07 图像数据和结果的分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)回归教材重难点04 水溶液中的离子平衡-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)河南省商丘市五校2021-2022学年高二下学期5月联考化学试题(已下线)专题6 Ksp专练(已下线)专题10水溶液中的离子平衡-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题10水溶液中的离子平衡-五年(2018~2022)高考真题汇编(全国卷)黑龙江省饶河县高级中学2021-2022学年上学期期末考试化学试题(已下线)考点29 沉淀溶解平衡-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第33练 沉淀溶解平衡-2023年高考化学一轮复习小题多维练(全国通用)云南省玉溪市通海县第一中学2021-2022学年高二上学期期末考试化学试题第三章 综合拔高练(已下线)微专题39 水溶液中平衡图像的拓展与探析-备战2023年高考化学一轮复习考点微专题(已下线)第24讲 沉淀溶解平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)微专题42 四大平衡常数的计算与应用-备战2023年高考化学一轮复习考点微专题江苏省海安市立发中学2022-2023学年高三上学期学情检测卷(二)化学试题辽宁省沈阳市五校协作体2022-2023学年高二上学期期中考试化学试题(已下线)专题06 水溶液中的离子平衡(讲)-2023年高考化学二轮复习讲练测(新高考专用)广东省华南师范大学附属中学2022-2023学年高二上学期阶段检测化学B卷试题吉林省长春市第二实验中学2022-2023学年高二上学期期末考试化学试题湖南省株洲市第二中学2022-2023学年高二上学期期中考试化学试题湖南省株洲九方中学2022-2023学年高二上学期期中考试化学试题湖南省株洲市第八中学2022-2023学年高二上学期期中考试化学试题(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 题型专攻4 电解质溶液各类图像的分析(已下线)第八章 水溶液中的离子反应与平衡 第53讲 沉淀溶解平衡图像的分析(已下线)题型142 有关沉淀溶解平衡图像湖南省岳阳市华容县普通高中2023届高三新高考适应性考试化学试题江西省赣州市重点中学九校联盟2022-2023学年高二下学期第一次月考化学试题(已下线)素养卷05 电解质溶液中微粒变化图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)题型27 沉淀溶解平衡常数及其应用图象(已下线)专题16 水溶液中的离子平衡(已下线)专题16 水溶液中的离子平衡(已下线)专题09 水溶液中的离子平衡-2023年高考化学真题题源解密(新高考专用)黑龙江省齐齐哈尔市讷河市第二中学等3校2022-2023学年高二下学期开学考试化学试题微专题(12) 电解质溶液中的两类特殊图像微专题(九)——沉淀溶解平衡曲线(已下线)考点29 沉淀溶解平衡(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 沉淀溶解平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)广东省广州市真光中学2023-2024学年高二上学期12月月考化学试题山东省菏泽市鄄城县第一中学2023-2024学年高三上学期1月月考化学试题山东省青岛第一中学2023-2024学年高二上学期第二次月考化学试卷福建省福建师范大学附属中学2023-2024学年高三上学期开学考化学试题
9 . 过渡金属元素铬 是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)对于基态Cr原子,下列叙述正确的是_______ (填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为
B.4s轨道上电子能量较高,总是在比3s轨道上电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)三价铬离子能形成多种配位化合物。 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是_______ ,中心离子的配位数为_______ 。
(3) 中配体分子
中配体分子 、
、 以及分子
以及分子 的空间结构和相应的键角如图所示。
的空间结构和相应的键角如图所示。
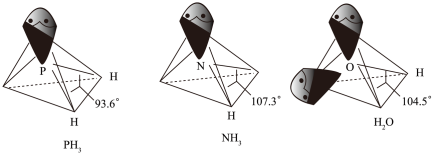
 中P的杂化类型是
中P的杂化类型是_______ 。 的沸点比
的沸点比 的
的_______ ,原因是_______ , 的键角小于
的键角小于 的,分析原因
的,分析原因_______ 。
(4)在金属材料中添加 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。
颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。 具有体心四方结构,如图所示,处于顶角位置的是
具有体心四方结构,如图所示,处于顶角位置的是_______ 原子。设Cr和Al原子半径分别为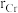 和
和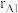 ,则金属原子空间占有率为
,则金属原子空间占有率为_______ %(列出计算表达式)。

 是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:(1)对于基态Cr原子,下列叙述正确的是
A.轨道处于半充满时体系总能量低,核外电子排布应为

B.4s轨道上电子能量较高,总是在比3s轨道上电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)三价铬离子能形成多种配位化合物。
 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是(3)
 中配体分子
中配体分子 、
、 以及分子
以及分子 的空间结构和相应的键角如图所示。
的空间结构和相应的键角如图所示。
 中P的杂化类型是
中P的杂化类型是 的沸点比
的沸点比 的
的 的键角小于
的键角小于 的,分析原因
的,分析原因(4)在金属材料中添加
 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。
颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。 具有体心四方结构,如图所示,处于顶角位置的是
具有体心四方结构,如图所示,处于顶角位置的是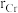 和
和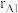 ,则金属原子空间占有率为
,则金属原子空间占有率为
您最近一年使用:0次
2021-06-09更新
|
20393次组卷
|
19卷引用:2021年高考全国乙卷化学真题
2021年高考全国乙卷化学真题吉林省长春外国语学校2020-2021学年高二下学期第二次月考化学试题(已下线)专题14 物质结构与性质-备战2022年高考化学学霸纠错(全国通用)(已下线)2021年高考全国乙卷化学试题变式题吉林省汪清县汪清四中2020-2021学年高二下学期期末考试化学试题(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题19 物质结构与性质-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)回归教材重难点11 物质结构与性质(选考)-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)押全国卷理综第35题 物质结构与性质-备战2022年高考化学临考题号押题(课标全国卷)(已下线)专题18物质结构与性质(选修)-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题18物质结构与性质(选修)-五年(2018~2022)高考真题汇编(全国卷)新疆柯坪县柯坪湖州国庆中学2021-2022学年高二下学期期末考试化学试题广东省茂名市电白区2021-2022学年高二下学期期中(选择性)考试化学试题(已下线)专题02 物质结构专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)广东省广州市真光中学2022-2023学年高二下学期期中考试化学试题(已下线)专题20 结构与性质(已下线)专题20 结构与性质(已下线)专题16 物质结构与性质综合题-2023年高考化学真题题源解密(全国通用)
10 . HA是一元弱酸,难溶盐MA的饱和溶液中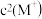 随c(H+)而变化,
随c(H+)而变化, 不发生水解。实验发现,
不发生水解。实验发现, 时
时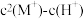 为线性关系,如下图中实线所示。
为线性关系,如下图中实线所示。
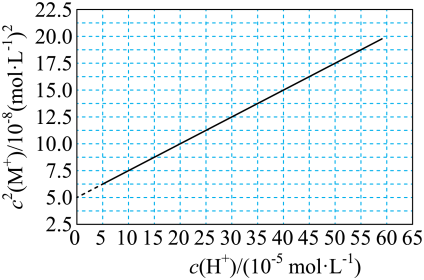
下列叙述错误的是
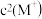 随c(H+)而变化,
随c(H+)而变化, 不发生水解。实验发现,
不发生水解。实验发现, 时
时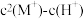 为线性关系,如下图中实线所示。
为线性关系,如下图中实线所示。
下列叙述错误的是
A.溶液 时, 时,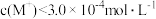 |
B.MA的溶度积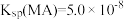 |
C.溶液 时, 时, |
D.HA的电离常数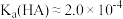 |
您最近一年使用:0次
2021-06-09更新
|
25627次组卷
|
50卷引用:2021年高考全国乙卷化学真题
2021年高考全国乙卷化学真题(已下线)第八章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第21讲 电离平衡(讲)-2022年高考化学一轮复习讲练测(新教材新高考)辽宁省东北育才学校2021-2022学年高二上学期期中考试化学试题(已下线)专题12 水溶液中的离子平衡-备战2022年高考化学学霸纠错(全国通用)(已下线)2021年高考全国乙卷化学试题变式题(已下线)第八单元 水溶液中的离子平衡(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)江苏省泰州中学2021-2022学年高二上学期第二次质量检测化学试题(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题13 水溶液中的离子平衡-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题07 电解质溶液—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)卷11 溶液中的离子平衡-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(全国卷)(已下线)回归教材重难点07 图像数据和结果的分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)回归教材重难点04 水溶液中的离子平衡-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题6 Ksp专练(已下线)专题10水溶液中的离子平衡-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题10水溶液中的离子平衡-五年(2018~2022)高考真题汇编(全国卷)四川省绵阳市2023届高三零诊模拟检测试题理科综合化学试题(已下线)考点29 沉淀溶解平衡-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第14练 用“五点”法突破盐类水解及酸碱混合相关图像-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)第33练 沉淀溶解平衡-2023年高考化学一轮复习小题多维练(全国通用)第三章 综合拔高练(已下线)第21讲 电离平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)微专题39 水溶液中平衡图像的拓展与探析-备战2023年高考化学一轮复习考点微专题(已下线)第24讲 沉淀溶解平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)微专题42 四大平衡常数的计算与应用-备战2023年高考化学一轮复习考点微专题(已下线)易错点23 弱电解质的电离平衡-备战2023年高考化学考试易错题(已下线)第一部分 二轮专题突破 题型专攻4 电解质溶液各类图像的分析疑难压轴1 电解质溶液中“四大常数”的相关计算(已下线)第八章 水溶液中的离子反应与平衡 第53讲 沉淀溶解平衡图像的分析(已下线)题型28 沉淀溶解平衡常数及其应用图像甘肃省张掖市高台县第一中学2022-2023学年高二下学期2月月考化学试题湖南省长沙市长郡中学2022-2023学年高三下学期第七次月考化学试题重庆市南开中学校2023届高三模拟考试化学试题(已下线)素养卷05 电解质溶液中微粒变化图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题16 水溶液中的离子平衡(已下线)专题16 水溶液中的离子平衡(已下线)专题09 水溶液中的离子平衡-2023年高考化学真题题源解密(新高考专用)微专题(13) 四大常数(K、Ka或Kb、Kw、Ksp)的应用微专题(九)——沉淀溶解平衡曲线(已下线)考点29 沉淀溶解平衡(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题12 水溶液中的离子反应与平衡-2023年高考化学真题题源解密(全国通用)(已下线)考点4 沉淀溶解平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)第6讲 沉淀溶解平衡图像分析辽宁省鞍山市普通高中2023-2024学年高三上学期期末联考化学试题四川省合江县马街中学校2023-2024学年高二上学期1月期末化学试题湖南省长沙市雅礼中学2023-2024学年高二下学期第一次月考化学试卷



