名校
1 . 某化学小组进行 制备和性质的实验探究,设计了如图装置制备并验证
制备和性质的实验探究,设计了如图装置制备并验证 的性质(部分夹持装置略去,a-d处均为浸有相应试液的脱脂棉)。
的性质(部分夹持装置略去,a-d处均为浸有相应试液的脱脂棉)。
(1)写出装置A中发生反应的化学方程式_______ 。
(2)打开K,点燃酒精灯开始反应,能证明 具有漂白性的现象是
具有漂白性的现象是_______ ,c处发生反应的离子方程式是_______ 。
(3)关闭K停止加热,由于余热Cu和浓 还要反应一段时间,装置B的作用是
还要反应一段时间,装置B的作用是_______ ,此时装置B中现象是_______ 。
(4)取一定质量的铜片和一定体积的浓硫酸于圆底烧瓶中共热至反应完全。发现烧瓶中有铜片剩余,该同学根据所学知识认为还有一定量的 剩余。下列药品中能用来证明反应结束后的烧瓶中存在余酸的是_______。
剩余。下列药品中能用来证明反应结束后的烧瓶中存在余酸的是_______。
(5)工业生产过程中产生的尾气需要测定 的含量,符合标准才能排放。已知有VL(已换算成标准状况)尾气,通入足量
的含量,符合标准才能排放。已知有VL(已换算成标准状况)尾气,通入足量 溶液吸收再加入足量
溶液吸收再加入足量 溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥,称量得到bg沉淀。
溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥,称量得到bg沉淀。 溶液的作用是
溶液的作用是_______ ,尾气中 含量(体积分数)的计算式是
含量(体积分数)的计算式是_______ (用含V、b的代数式表示)。
 制备和性质的实验探究,设计了如图装置制备并验证
制备和性质的实验探究,设计了如图装置制备并验证 的性质(部分夹持装置略去,a-d处均为浸有相应试液的脱脂棉)。
的性质(部分夹持装置略去,a-d处均为浸有相应试液的脱脂棉)。
(1)写出装置A中发生反应的化学方程式
(2)打开K,点燃酒精灯开始反应,能证明
 具有漂白性的现象是
具有漂白性的现象是(3)关闭K停止加热,由于余热Cu和浓
 还要反应一段时间,装置B的作用是
还要反应一段时间,装置B的作用是(4)取一定质量的铜片和一定体积的浓硫酸于圆底烧瓶中共热至反应完全。发现烧瓶中有铜片剩余,该同学根据所学知识认为还有一定量的
 剩余。下列药品中能用来证明反应结束后的烧瓶中存在余酸的是_______。
剩余。下列药品中能用来证明反应结束后的烧瓶中存在余酸的是_______。| A.铁粉 | B. 溶液 溶液 |
C. 溶液 溶液 | D.银粉 |
(5)工业生产过程中产生的尾气需要测定
 的含量,符合标准才能排放。已知有VL(已换算成标准状况)尾气,通入足量
的含量,符合标准才能排放。已知有VL(已换算成标准状况)尾气,通入足量 溶液吸收再加入足量
溶液吸收再加入足量 溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥,称量得到bg沉淀。
溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥,称量得到bg沉淀。 溶液的作用是
溶液的作用是 含量(体积分数)的计算式是
含量(体积分数)的计算式是
您最近一年使用:0次
名校
2 . 二氧化硫是一把“双刃剑”,既是重要的化工原料,又是大气污染物。某化学小组用如图装置制备 ,并验证
,并验证 的部分性质(夹持及加热仪器已省略)。
的部分性质(夹持及加热仪器已省略)。
I.检查气密性后,加入药品,开始实验,关闭 ,打开
,打开 和仪器a活塞,至B处固体变蓝。
和仪器a活塞,至B处固体变蓝。
II.关闭 ,打开
,打开 。
。
回答下列问题:
(1)仪器a的名称为___________ ,装置D的作用是___________ 。
(2)实验过程中观察到C处蘸有酸性 溶液的棉花褪色,写出C处发生反应的离子方程式:
溶液的棉花褪色,写出C处发生反应的离子方程式:___________ (已知 转化为
转化为 )。
)。
(3)装置A___________ (填“需要”或“不需要”)加热,装置A中发生的化学反应方程式为___________ 。
(4)若试剂X是品红溶液,则可验证 的
的___________ 性。
(5)若试剂X是 溶液,反应一段时间,可观察到现象为
溶液,反应一段时间,可观察到现象为___________ ,该反应中 表现
表现___________ 性。
(6)若试剂X是 的
的 溶液,装置E中得到了大量白色沉淀;而用
溶液,装置E中得到了大量白色沉淀;而用 的
的 溶液,装置E中无白色沉淀生成。
溶液,装置E中无白色沉淀生成。
①前者生成的白色沉淀为 ,生成该沉淀的原因是
,生成该沉淀的原因是___________ (由语言描述)。
②后者无白色沉淀生成,可说明酸性:
___________ (填“>”或“<”)HCl。
 ,并验证
,并验证 的部分性质(夹持及加热仪器已省略)。
的部分性质(夹持及加热仪器已省略)。
I.检查气密性后,加入药品,开始实验,关闭
 ,打开
,打开 和仪器a活塞,至B处固体变蓝。
和仪器a活塞,至B处固体变蓝。II.关闭
 ,打开
,打开 。
。回答下列问题:
(1)仪器a的名称为
(2)实验过程中观察到C处蘸有酸性
 溶液的棉花褪色,写出C处发生反应的离子方程式:
溶液的棉花褪色,写出C处发生反应的离子方程式: 转化为
转化为 )。
)。(3)装置A
(4)若试剂X是品红溶液,则可验证
 的
的(5)若试剂X是
 溶液,反应一段时间,可观察到现象为
溶液,反应一段时间,可观察到现象为 表现
表现(6)若试剂X是
 的
的 溶液,装置E中得到了大量白色沉淀;而用
溶液,装置E中得到了大量白色沉淀;而用 的
的 溶液,装置E中无白色沉淀生成。
溶液,装置E中无白色沉淀生成。①前者生成的白色沉淀为
 ,生成该沉淀的原因是
,生成该沉淀的原因是②后者无白色沉淀生成,可说明酸性:

您最近一年使用:0次
名校
3 . 类比推理是研究物质性质的常用方法,下列推理正确的是
| A.已知Na2O2与CO2反应生成Na2CO3和O2,推测Na2O2与SO2反应生成Na2SO3和O2 |
| B.浓硫酸与Na2SO3反应可以制备SO2,推测浓硫酸与Na2S反应可以制备H2S |
| C.已知Fe与S能直接化合生成FeS,推测Cu与S可直接化合生成Cu2S |
| D.SO2通入BaCl2溶液不产生沉淀,推测SO2通入Ba(NO3)2溶液也不产生沉淀 |
您最近一年使用:0次
4 . Na2S2O5可用作防腐剂、棉布漂白后脱氯剂。某兴趣小组欲利用如图装置制备Na2S2O5。
步骤:检验装置气密性后装入药品。打开弹簧夹和仪器a的活塞,逐滴滴入70%硫酸,在碳酸钠悬浊液中通入SO2至悬浊液变澄清后又析出大量晶体时,关闭活塞,将C装置中的反应液过滤﹑洗涤、干燥,即得Na2S2O5晶体。 的名称为
的名称为______________ 。
(2)B装置的作用是______________ 。
(3)C装置中的反应分两步进行,第一步为Na2CO3 + 2SO2 + H2O = 2NaHSO3 + CO2,该反应能发生的原因为______________ ;第二步为NaHSO3转化成Na2S2O5,写出该步反应的化学方程式:___________ 。
(4)C装置中的反应液过滤后,用饱和SO2水溶液洗涤,其目的是____________ 。
(5)D装置中NaOH溶液的作用是______________ 。
(6)已知Na2S2O5不稳定,在空气中易被氧化成Na2SO4,与强酸反应生成相应的盐和SO2,请设计简单实验检验Na2S2O5是否变质:___________ 。
步骤:检验装置气密性后装入药品。打开弹簧夹和仪器a的活塞,逐滴滴入70%硫酸,在碳酸钠悬浊液中通入SO2至悬浊液变澄清后又析出大量晶体时,关闭活塞,将C装置中的反应液过滤﹑洗涤、干燥,即得Na2S2O5晶体。

 的名称为
的名称为(2)B装置的作用是
(3)C装置中的反应分两步进行,第一步为Na2CO3 + 2SO2 + H2O = 2NaHSO3 + CO2,该反应能发生的原因为
(4)C装置中的反应液过滤后,用饱和SO2水溶液洗涤,其目的是
(5)D装置中NaOH溶液的作用是
(6)已知Na2S2O5不稳定,在空气中易被氧化成Na2SO4,与强酸反应生成相应的盐和SO2,请设计简单实验检验Na2S2O5是否变质:
您最近一年使用:0次
名校
5 . 下列气体除杂的方法中,不能达到目的的是
| 选项 | 气体(杂质) | 除杂方法 |
| A | NO(NO2) | 通过NaOH溶液洗气 |
| B | CO2(SO2) | 通过饱和NaHCO3溶液洗气 |
| C | N2(O2) | 通过灼热的铜网 |
| D | Cl2(HCl) | 通过饱和食盐水洗气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 物质的性质决定用途。下列两者对应关系不正确的是
| A.生铁硬度大、抗压性强,可用于铸造机器底座 |
| B.氯化铁溶液有氧化性,可用于蚀刻不锈钢广告牌上的图形 |
| C.二氧化硫具有漂白性,食品中添加适量的SO2有防腐和抗氧化作用 |
| D.新型陶瓷碳化硅硬度很大,可用作砂纸和砂轮的磨料 |
您最近一年使用:0次
名校
7 . 将 分别通入无氧、有氧的浓度均为0.1
分别通入无氧、有氧的浓度均为0.1 的
的 溶液和
溶液和 溶液中,除
溶液中,除 溶液(无氧)外,都产生白色沉淀。实验测得各溶液pH变化曲线如图。下列说法正确的是
溶液(无氧)外,都产生白色沉淀。实验测得各溶液pH变化曲线如图。下列说法正确的是
 分别通入无氧、有氧的浓度均为0.1
分别通入无氧、有氧的浓度均为0.1 的
的 溶液和
溶液和 溶液中,除
溶液中,除 溶液(无氧)外,都产生白色沉淀。实验测得各溶液pH变化曲线如图。下列说法正确的是
溶液(无氧)外,都产生白色沉淀。实验测得各溶液pH变化曲线如图。下列说法正确的是
A.曲线a所示溶液pH降低的原因: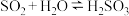 , ,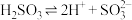 |
B.依据曲线b可推知0.2  溶液(无氧)不能氧化 溶液(无氧)不能氧化 |
C.曲线d所表示的过程中 是氧化 是氧化 的主要微粒 的主要微粒 |
D.曲线c所示溶液中发生反应的离子方程式为: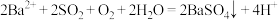 |
您最近一年使用:0次
名校
8 . 下列说法中正确的有
①燃煤中添加CaO可以减少 和温室气体的排放
和温室气体的排放
②二氧化硫具有抗氧化性,可用作葡萄酒的食品添加剂
③液氨汽化时吸热,可用作制冷剂
④加入 溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有
溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有 存在
存在
⑤单质硫易溶于 ,实验室可用
,实验室可用 清洗沾有硫单质的试管
清洗沾有硫单质的试管
⑥足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化
⑦二氧化硅与氢氧化钠溶液、氢氟酸均反应,属两性氧化物
⑧陶瓷、普通玻璃、水泥、金刚砂(SiC)都属于硅酸盐材料
①燃煤中添加CaO可以减少
 和温室气体的排放
和温室气体的排放②二氧化硫具有抗氧化性,可用作葡萄酒的食品添加剂
③液氨汽化时吸热,可用作制冷剂
④加入
 溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有
溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有 存在
存在⑤单质硫易溶于
 ,实验室可用
,实验室可用 清洗沾有硫单质的试管
清洗沾有硫单质的试管⑥足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化

⑦二氧化硅与氢氧化钠溶液、氢氟酸均反应,属两性氧化物
⑧陶瓷、普通玻璃、水泥、金刚砂(SiC)都属于硅酸盐材料
| A.①③⑤ | B.②③⑤ | C.④⑥⑧ | D.⑤⑥⑦ |
您最近一年使用:0次
名校
9 . 部分含S和Cl的物质分类与相应化合价的关系如图所示。下列说法正确的是

| A.b或f与金属Cu反应的产物中Cu的化合价均为+2 |
| B.向h的溶液中通入c,溶液的酸性增强 |
| C.d的浓溶液具有脱水性,可使胆矾晶体由蓝色变为白色 |
| D.c和g都具有漂白性,能使湿润的蓝色石蕊试纸先变红后褪色 |
您最近一年使用:0次
名校
解题方法
10 . 某同学设计了如下装置用于制取 和验证
和验证 的性质。
的性质。 具有一定氧化性。
具有一定氧化性。
(1)装置A中发生反应的化学方程式为_______ 。
(2)在框图内选择合适装置依次验证 的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为A→
的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为A→_______ (填装置字母,还原性设计两个装置)。_______ (化学式),分析F中产生白色沉淀原因_______ (用离子方程式表示)。
(4)实验中发现装置A中 可能部分被氧化,现需测定
可能部分被氧化,现需测定 的纯度:称取10.00g样品,配成100mL溶液;取其中的25.00mL溶液,与0.2000mol/L酸性
的纯度:称取10.00g样品,配成100mL溶液;取其中的25.00mL溶液,与0.2000mol/L酸性 溶液发生以下反应:
溶液发生以下反应: ,实验消耗
,实验消耗 溶液20.00mL,以上样品中
溶液20.00mL,以上样品中 的质量分数为
的质量分数为_______ (保留三位有效数字)。
 和验证
和验证 的性质。
的性质。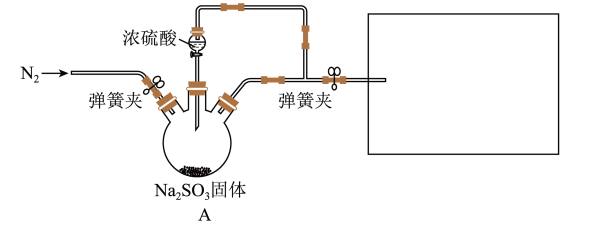
 具有一定氧化性。
具有一定氧化性。(1)装置A中发生反应的化学方程式为
(2)在框图内选择合适装置依次验证
 的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为A→
的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为A→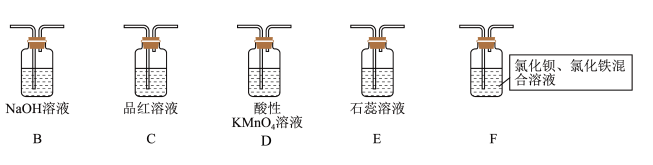
(4)实验中发现装置A中
 可能部分被氧化,现需测定
可能部分被氧化,现需测定 的纯度:称取10.00g样品,配成100mL溶液;取其中的25.00mL溶液,与0.2000mol/L酸性
的纯度:称取10.00g样品,配成100mL溶液;取其中的25.00mL溶液,与0.2000mol/L酸性 溶液发生以下反应:
溶液发生以下反应: ,实验消耗
,实验消耗 溶液20.00mL,以上样品中
溶液20.00mL,以上样品中 的质量分数为
的质量分数为
您最近一年使用:0次



