1 .  在生活、生产中有重要用途,使用不当会造成环境污染。某同学利用如图所示装置研究二氧化硫的性质。
在生活、生产中有重要用途,使用不当会造成环境污染。某同学利用如图所示装置研究二氧化硫的性质。___________ 。
(2)向仪器a中滴加浓硫酸之前,需先通入一段时间 ,此操作的目的是
,此操作的目的是___________ 。
(3)若将 气体直接通入澄清石灰水中,溶液变浑浊,则该反应的离子方程式为
气体直接通入澄清石灰水中,溶液变浑浊,则该反应的离子方程式为___________ 。
(4)实验时,装置B中没有明显变化。实验结束后取下装置B,向其中滴加适量氨水,生成的白色沉淀为___________ (填化学式)。
 在生活、生产中有重要用途,使用不当会造成环境污染。某同学利用如图所示装置研究二氧化硫的性质。
在生活、生产中有重要用途,使用不当会造成环境污染。某同学利用如图所示装置研究二氧化硫的性质。
(2)向仪器a中滴加浓硫酸之前,需先通入一段时间
 ,此操作的目的是
,此操作的目的是(3)若将
 气体直接通入澄清石灰水中,溶液变浑浊,则该反应的离子方程式为
气体直接通入澄清石灰水中,溶液变浑浊,则该反应的离子方程式为(4)实验时,装置B中没有明显变化。实验结束后取下装置B,向其中滴加适量氨水,生成的白色沉淀为
您最近一年使用:0次
2 . 下列实验结论与实验现象相符合的一组是
选项 | 实验 | 现象 | 结论 |
A | 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液 | 先变橙色,后变蓝色 | 氧化性: |
B | 向品红溶液中通入某气体 | 品红褪色 | 气体一定是 |
C | 向蔗糖中滴加浓硫酸 | 蔗糖变黑 | 浓硫酸具有吸水性 |
D | 向某盐溶液中加入浓NaOH溶液,加热 | 产生的气体能使湿润的红色石蕊试纸变蓝 | 原溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 物质的性质决定用途,下列两者对应关系不正确的是
| A.SiC熔点高硬度大,可作耐高温结构材料 |
| B.常温下,浓硫酸使铁、铝钝化,所以铁质、铝质容器能盛放浓硫酸 |
| C.乙醇和水的沸点相差较大,故可以通过直接蒸馏制备无水乙醇 |
| D.SO2具有还原性,可作抗氧化剂 |
您最近一年使用:0次
解题方法
4 . 下列离子或化学方程式书写正确的是
A.用足量的NaOH溶液吸收SO2尾气:2OH﹣+SO2= +H2O +H2O |
| B.Cl2和H2O反应:Cl2+H2O=2H++Cl﹣+ClO﹣ |
C.用石英和焦炭制取粗硅:SiO2+C Si+CO2 Si+CO2 |
| D.硫化氢通入氯化铁溶液:S2﹣+2Fe3+=2Fe2++S↓ |
您最近一年使用:0次
名校
5 . 化学与生产、生活息息相关,下列叙述正确的是
| A.SO2可用于杀菌消毒,故不能作食品添加剂 |
| B.医疗上,BaCO3可用作消化系统X射线检查的内服药剂 |
| C.燃煤中加入 CaO可以减少CO2的排放 |
| D.可用CS2清洗试管中残留的硫粉 |
您最近一年使用:0次
2024-04-03更新
|
313次组卷
|
3卷引用:云南省昆明市第十二中学2023-2024学年高一下学期期中考试化学试题
名校
解题方法
6 . 下列解释事实的化学用语不正确 的是
A.浓硝酸用棕色瓶保存: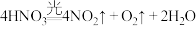 |
B.氯化铝溶液与过量氨水反应: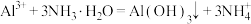 |
C.氯水可用于吸收 : : |
D.Fe溶于过量稀 : :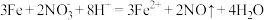 |
您最近一年使用:0次
2024-04-03更新
|
233次组卷
|
2卷引用:云南省昆明市第十二中学2023-2024学年高一下学期期中考试化学试题
解题方法
7 . 下列由相关实验现象所推出的结论正确的是
| A.Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 |
B.向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO |
| C.分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者易溶于水 |
| D.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应 |
您最近一年使用:0次
解题方法
8 . 已知:稀硝酸能与SO2发生氧化还原反应:3SO2+2HNO3+2H2O=3H2SO4+2NO。下列过程中最终的白色沉淀不一定是BaSO4的是
| A.Fe(NO3)2溶液→通入SO2+过量盐酸→加BaCl2溶液→白色沉淀 |
| B.Ba(NO3)2溶液→加过量盐酸→加Na2SO3溶液→白色沉淀 |
| C.无色溶液→加稀HNO3→加BaCl2溶液→白色沉淀 |
| D.无色溶液→加过量盐酸→无色溶液→加BaCl2溶液→白色溶液 |
您最近一年使用:0次
9 . 化学与生产和生活密切相关。下列说法错误的是
A.可用 漂白纸张 漂白纸张 | B.水玻璃可用作木材防火剂 |
C.可用 制作半导体芯片 制作半导体芯片 | D.可用 作食品防腐剂 作食品防腐剂 |
您最近一年使用:0次
解题方法
10 . 浓硫酸是中学常见的一种化学试剂,某学校实验小组为探究浓硫酸与金属的反应并检验生成的气体设计了相关实验。

(1)常温下,将铝片插入浓H2SO4中未发现有明显的变化,其原因为______ 。
(2)在加热的条件下,浓H2SO4可将铜氧化,写出该反应的化学方程式:______ 。
(3)实验中使用可抽动的铜丝,其优点是______ 。
(4)C中的实验现象为_______ ,通过对该实验现象的分析,说明SO2有_______ (填“还原性”或“氧化性”)。
(5)该装置设计有没有缺陷______ (填“有”或“无”);若有,如何改进______ (若无缺陷则此空不用作答)。

(1)常温下,将铝片插入浓H2SO4中未发现有明显的变化,其原因为
(2)在加热的条件下,浓H2SO4可将铜氧化,写出该反应的化学方程式:
(3)实验中使用可抽动的铜丝,其优点是
(4)C中的实验现象为
(5)该装置设计有没有缺陷
您最近一年使用:0次



