名校
1 . A、B、C、D、E、F 均为短周期元素,且原子序数依次增大,A 是原子半径最小的元素,B 的最高价氧化物的水化物可与其氢化物反应形成盐类物质甲;A 与 D 可以按照原子个数比 4∶1 形成化合物乙,且乙分子中含有 18 个电子,E 与 B 同主族,C 的阳离子与 F 的阴离子相差一个电子层,且可形成离子个数比为 2∶1 的离子化合物丙。
(1)E 在周期表中的位置为_________ 。
(2)下列说法正确的有_____ 。
①化合物乙分子中只含有极性共价键
②C、D、E、F 原子半径由大到小的顺序为 C>D>E>F
③B、E 形成的氢化物中,B 的氢化物更稳定,沸点也最高
④化合物甲和化合物丙都既含有离子键也含有共价键
(3)将 F 燃烧的产物通入 BaCl2和 HNO3的混合溶液中,生成白色沉淀并放出无色气体, 请用一个离子方程式表示该反应________
(4)写出一个由以上元素构成的 10 电子与 18 电子分子反应的化学方程式______
(5)A 与 B 可形成一种二元化合物 X,其中 A 元素质量分数为 2.33%.据研究 X 显弱酸性。X 电离的阴离子结构与二氧化碳相似,则该阴离子的电子式为_____
(6)F 的某种氧化物是大气污染物之一,也是某工业生产中的主要尾气之一。某校兴趣小组欲采用下列方案测定此工业尾气中的 F 的氧化物的含量。
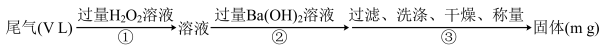
通过的尾气体积为 VL(已换算成标准状况)时,该尾气中 F 的氧化物含量(体积分数)为____ (用含有 V、m 的代数式表示)
(1)E 在周期表中的位置为
(2)下列说法正确的有
①化合物乙分子中只含有极性共价键
②C、D、E、F 原子半径由大到小的顺序为 C>D>E>F
③B、E 形成的氢化物中,B 的氢化物更稳定,沸点也最高
④化合物甲和化合物丙都既含有离子键也含有共价键
(3)将 F 燃烧的产物通入 BaCl2和 HNO3的混合溶液中,生成白色沉淀并放出无色气体, 请用一个离子方程式表示该反应
(4)写出一个由以上元素构成的 10 电子与 18 电子分子反应的化学方程式
(5)A 与 B 可形成一种二元化合物 X,其中 A 元素质量分数为 2.33%.据研究 X 显弱酸性。X 电离的阴离子结构与二氧化碳相似,则该阴离子的电子式为
(6)F 的某种氧化物是大气污染物之一,也是某工业生产中的主要尾气之一。某校兴趣小组欲采用下列方案测定此工业尾气中的 F 的氧化物的含量。
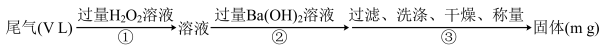
通过的尾气体积为 VL(已换算成标准状况)时,该尾气中 F 的氧化物含量(体积分数)为

您最近一年使用:0次
名校
2 . 硫的含量影响钢铁性能。一种测定硫含量的方法是将钢样中硫转化为二氧化硫气体,再用测硫装置进行测定。某测定硫含量的流程如下:
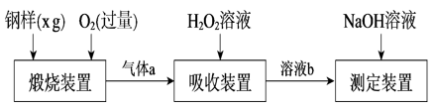
(1)气体a的主要成分有CO2、______ 、______ 。
(2)若钢样中硫以FeS的形式存在,煅烧装置中发生的化学反应为3FeS+5O2 1
1______ +3_______
(3)吸收装置中,H2O2氧化SO2的化学方程式是_________________ 。
(4)用NaOH溶液中和生成的溶液b,消耗z mLNaOH溶液,若消耗1 mLNaOH溶液相当于硫的质量为y g,则该钢样中硫的质量分数为______ 。

(1)气体a的主要成分有CO2、
(2)若钢样中硫以FeS的形式存在,煅烧装置中发生的化学反应为3FeS+5O2
 1
1(3)吸收装置中,H2O2氧化SO2的化学方程式是
(4)用NaOH溶液中和生成的溶液b,消耗z mLNaOH溶液,若消耗1 mLNaOH溶液相当于硫的质量为y g,则该钢样中硫的质量分数为
您最近一年使用:0次
2019-01-24更新
|
664次组卷
|
7卷引用:湖北省鄂东南联盟2019-2020学年高一下学期期中联考化学试题
名校
3 . 碳、硫的含量影响钢铁性能。某兴趣小组用如下流程对钢样进行探究。
(1)钢样中硫元素以FeS形式存在,FeS在足量氧气中灼烧,生成的固体产物中Fe、O两种元素的质量比为21:8,则该固体产物的化学式为_____________ 。
(2)检验钢样灼烧生成气体中的CO2,需要的试剂是____________ (填字母)。
a.酸性KMnO4溶液b.澄清石灰水c.饱和小苏打溶液d.浓H2SO4
(3)取10.00 g钢样在足量氧气中充分灼烧,将生成的气体用足量1%的H2O2溶液充分吸收,再用0.1000mol·L-1NaOH溶液滴定吸收液至终点,消耗NaOH溶液20.00mL;另取10.00g钢样在足量氧气中充分灼烧,将生成的气体通过盛有足量碱石灰的U形管(如下图),碱石灰增重0.614 g。
①用l%H2O2溶液吸收SO2,发生反应的离子方程式为___________________ 。
②分别计算该钢样中硫、碳元素的质量分数(写出计算过程)。
③实验测得的碳元素质量分数比真实值偏高,其可能的原因是______________ (填字母)
a.U型管中生成的亚硫酸盐吸收了O2
b.碱石灰吸收了空气中的CO2
c.气体通过碱石灰的流速过快,末被充分吸收

(1)钢样中硫元素以FeS形式存在,FeS在足量氧气中灼烧,生成的固体产物中Fe、O两种元素的质量比为21:8,则该固体产物的化学式为
(2)检验钢样灼烧生成气体中的CO2,需要的试剂是
a.酸性KMnO4溶液b.澄清石灰水c.饱和小苏打溶液d.浓H2SO4
(3)取10.00 g钢样在足量氧气中充分灼烧,将生成的气体用足量1%的H2O2溶液充分吸收,再用0.1000mol·L-1NaOH溶液滴定吸收液至终点,消耗NaOH溶液20.00mL;另取10.00g钢样在足量氧气中充分灼烧,将生成的气体通过盛有足量碱石灰的U形管(如下图),碱石灰增重0.614 g。

①用l%H2O2溶液吸收SO2,发生反应的离子方程式为
②分别计算该钢样中硫、碳元素的质量分数(写出计算过程)。
③实验测得的碳元素质量分数比真实值偏高,其可能的原因是
a.U型管中生成的亚硫酸盐吸收了O2
b.碱石灰吸收了空气中的CO2
c.气体通过碱石灰的流速过快,末被充分吸收
您最近一年使用:0次
2017-03-24更新
|
469次组卷
|
5卷引用:2017届江苏省丹阳高级中学高三下学期期中考试化学试卷
2017届江苏省丹阳高级中学高三下学期期中考试化学试卷2017届江苏省南京市、盐城市高三第二次模拟考试化学试卷江苏省淮安市淮海中学2020届高三第一次模拟考试化学试题(已下线)专题讲座(九) 热点实验综合探究 (精练)-2021年高考化学一轮复习讲练测江苏省南京市第一中学2021届高三年级上学期10月月考化学试题
名校
解题方法
4 . 某同学为了测定某生铁(仅含C、 )中铁的质量分数,设计了如图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究.
)中铁的质量分数,设计了如图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究.

回答下列问题:
(1)仪器a的名称为________ ,仪器e的名称为________ ;
(2)B装置的作用为________ ,D装置的作用为________ ;
(3)点燃酒精灯,A装置中发生的反应化学方程式为_______________ 、_________________
(4)待 生铁完全溶解后,停止加热,拆下装置E并称重.若装置E增重
生铁完全溶解后,停止加热,拆下装置E并称重.若装置E增重 ,则生铁中铁的质量分数为
,则生铁中铁的质量分数为________ (用含m、b的表达式表示);
(5)利用该装置测得实验结果不够准确,改良的方法为____________________ 。
 )中铁的质量分数,设计了如图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究.
)中铁的质量分数,设计了如图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究.
回答下列问题:
(1)仪器a的名称为
(2)B装置的作用为
(3)点燃酒精灯,A装置中发生的反应化学方程式为
(4)待
 生铁完全溶解后,停止加热,拆下装置E并称重.若装置E增重
生铁完全溶解后,停止加热,拆下装置E并称重.若装置E增重 ,则生铁中铁的质量分数为
,则生铁中铁的质量分数为(5)利用该装置测得实验结果不够准确,改良的方法为
您最近一年使用:0次
名校
解题方法
5 .  是一种重要的化工产品,也是重要的化工原料。某化学兴趣小组在实验室制备
是一种重要的化工产品,也是重要的化工原料。某化学兴趣小组在实验室制备 并完成相关性质实验。
并完成相关性质实验。
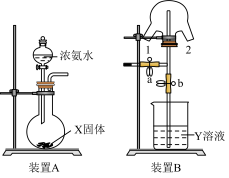
Ⅰ.实验室制取 通常有两种方法:①选择药品氢氧化钙与氯化铵固体;②选择药品NaOH固体与浓氨水。
通常有两种方法:①选择药品氢氧化钙与氯化铵固体;②选择药品NaOH固体与浓氨水。 应选择的装置是
应选择的装置是_______ (填“甲”或“乙”),发生反应的化学方程式为___________________ 。检验 已收集满的方法是
已收集满的方法是________________ 。
(2)利用装置乙还可制取下列气体中的______ (填字母)。
a. b.
b. c.
c.
(3)下列能用作 尾气吸收装置的是
尾气吸收装置的是______ (填序号)。 的性质。
的性质。 均为红色固体,
均为红色固体, 。
。
①若溶液不变蓝,A中发生的总反应方程式为_______________________ 。
②若溶液变蓝,证明红色固体中______ (填“有”或“没有”) ,经称量反应前A中CuO质量为8g,反应后A中红色固体质量为6.8g,则红色固体中金属铜的质量分数为
,经称量反应前A中CuO质量为8g,反应后A中红色固体质量为6.8g,则红色固体中金属铜的质量分数为__________ (精确至0.01%)。
(5)若将B与C装置中a相连,通入 后,
后, 溶液中产生白A沉淀,写出生成白色沉淀的总离子方程式
溶液中产生白A沉淀,写出生成白色沉淀的总离子方程式_________________________ 。
 是一种重要的化工产品,也是重要的化工原料。某化学兴趣小组在实验室制备
是一种重要的化工产品,也是重要的化工原料。某化学兴趣小组在实验室制备 并完成相关性质实验。
并完成相关性质实验。Ⅰ.实验室制取
 通常有两种方法:①选择药品氢氧化钙与氯化铵固体;②选择药品NaOH固体与浓氨水。
通常有两种方法:①选择药品氢氧化钙与氯化铵固体;②选择药品NaOH固体与浓氨水。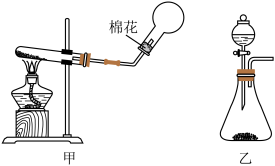
 应选择的装置是
应选择的装置是 已收集满的方法是
已收集满的方法是(2)利用装置乙还可制取下列气体中的
a.
 b.
b. c.
c.
(3)下列能用作
 尾气吸收装置的是
尾气吸收装置的是
 的性质。
的性质。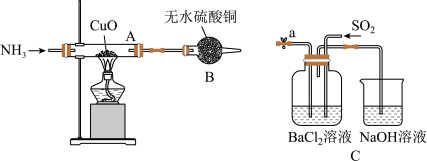
 均为红色固体,
均为红色固体, 。
。①若溶液不变蓝,A中发生的总反应方程式为
②若溶液变蓝,证明红色固体中
 ,经称量反应前A中CuO质量为8g,反应后A中红色固体质量为6.8g,则红色固体中金属铜的质量分数为
,经称量反应前A中CuO质量为8g,反应后A中红色固体质量为6.8g,则红色固体中金属铜的质量分数为(5)若将B与C装置中a相连,通入
 后,
后, 溶液中产生白A沉淀,写出生成白色沉淀的总离子方程式
溶液中产生白A沉淀,写出生成白色沉淀的总离子方程式
您最近一年使用:0次
2024-03-25更新
|
249次组卷
|
2卷引用:湖南省常德市汉寿县第一中学2023-2024学年高一下学期4月期中考试化学试题
名校
6 . 葡萄酒中含有CH3CH2OH、CH3COOH、SO2和CO2等多种成分。若NA代表阿伏加德罗常数的值,下列说法正确的是
| A.1molCH3COOH和1molCH3CH2OH充分反应生成H2O的数目为1NA |
| B.1molCO2中含有共用电子对数4NA |
| C.100g质量分数为46%的乙醇溶液中所含氧原子数为1NA |
| D.11.2L(标准状况)SO2恰好完全溶于新制氯水,转移电子数为2NA |
您最近一年使用:0次
名校
解题方法
7 . 某同学设计了如下装置用于制取 和验证
和验证 的性质。
的性质。 具有一定氧化性。
具有一定氧化性。
(1)装置A中发生反应的化学方程式为_______ 。
(2)在框图内选择合适装置依次验证 的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为A→
的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为A→_______ (填装置字母,还原性设计两个装置)。_______ (化学式),分析F中产生白色沉淀原因_______ (用离子方程式表示)。
(4)实验中发现装置A中 可能部分被氧化,现需测定
可能部分被氧化,现需测定 的纯度:称取10.00g样品,配成100mL溶液;取其中的25.00mL溶液,与0.2000mol/L酸性
的纯度:称取10.00g样品,配成100mL溶液;取其中的25.00mL溶液,与0.2000mol/L酸性 溶液发生以下反应:
溶液发生以下反应: ,实验消耗
,实验消耗 溶液20.00mL,以上样品中
溶液20.00mL,以上样品中 的质量分数为
的质量分数为_______ (保留三位有效数字)。
 和验证
和验证 的性质。
的性质。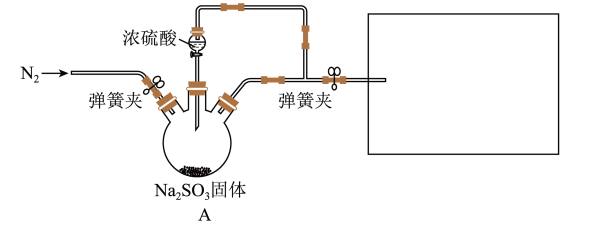
 具有一定氧化性。
具有一定氧化性。(1)装置A中发生反应的化学方程式为
(2)在框图内选择合适装置依次验证
 的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为A→
的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为A→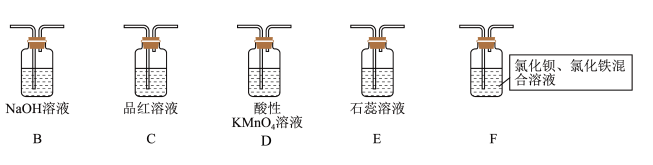
(4)实验中发现装置A中
 可能部分被氧化,现需测定
可能部分被氧化,现需测定 的纯度:称取10.00g样品,配成100mL溶液;取其中的25.00mL溶液,与0.2000mol/L酸性
的纯度:称取10.00g样品,配成100mL溶液;取其中的25.00mL溶液,与0.2000mol/L酸性 溶液发生以下反应:
溶液发生以下反应: ,实验消耗
,实验消耗 溶液20.00mL,以上样品中
溶液20.00mL,以上样品中 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
8 . 某工厂每天燃烧含硫质量分数为0.64%的煤100吨,如果煤中的硫元素全部转化为 气体,且产生的
气体,且产生的 全部用来生产硫酸,理论上每年(按365天计)可得到质量分数为98%的浓硫酸的质量为
全部用来生产硫酸,理论上每年(按365天计)可得到质量分数为98%的浓硫酸的质量为_______ 吨。
 气体,且产生的
气体,且产生的 全部用来生产硫酸,理论上每年(按365天计)可得到质量分数为98%的浓硫酸的质量为
全部用来生产硫酸,理论上每年(按365天计)可得到质量分数为98%的浓硫酸的质量为
您最近一年使用:0次
名校
解题方法
9 . 硫酸工业在国民经济中占有极其重要的地位。下图是工业制硫酸的生产流程示意图,读图后回答下列问题。
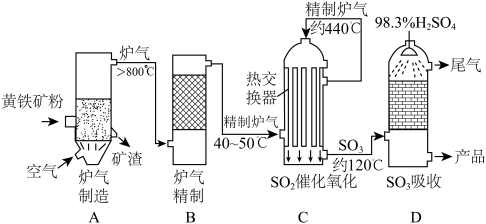
请回答下列问题:
(1)在炉气制造中,黄铁矿粉碎的目的是___________ 。
(2)炉气精制的目的是___________ 。
(3)二氧化硫催化氧化的化学方程式是___________ ,反应温度维持在475℃左右的原因是___________ 、___________ 。
(4)工业上用质量分数为98.3%的浓硫酸吸收三氧化硫,而不是用水或稀硫酸直接吸收的原因是___________
(5)在硫酸工业生产中,热交换器的作用是将二氧化硫转化为三氧化硫产生的热量传递给进入转化器的原料气,原料气通过热交换器预热后进入催化层,发生催化氧化反应,充分利用了___________ 。
(6)工业上以硫铁矿为原料制硫酸所产生的尾气除了含有 、
、 外,还含有
外,还含有 、微量的
、微量的 和酸雾。为了保护环境,同时提高硫酸工业的综合经济效益,按照下图工艺流程,将尾气中的
和酸雾。为了保护环境,同时提高硫酸工业的综合经济效益,按照下图工艺流程,将尾气中的 转化为有用的副产品。请回答下列问题。
转化为有用的副产品。请回答下列问题。
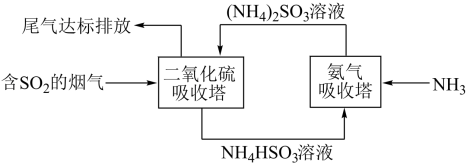
①写出氨吸收塔中主要发生的化学方程式___________ ;
②写出二氧化硫吸收塔中主要发生的离子方程式___________ ;
③当含 烟气通入二氧化硫吸收塔中,可能发生氧化还原反应吗?如可能,请写出至少一个氧化还原反应的化学方程式
烟气通入二氧化硫吸收塔中,可能发生氧化还原反应吗?如可能,请写出至少一个氧化还原反应的化学方程式___________ ;
④上述流程可循环利用的物质是___________ 。

请回答下列问题:
(1)在炉气制造中,黄铁矿粉碎的目的是
(2)炉气精制的目的是
(3)二氧化硫催化氧化的化学方程式是
(4)工业上用质量分数为98.3%的浓硫酸吸收三氧化硫,而不是用水或稀硫酸直接吸收的原因是
(5)在硫酸工业生产中,热交换器的作用是将二氧化硫转化为三氧化硫产生的热量传递给进入转化器的原料气,原料气通过热交换器预热后进入催化层,发生催化氧化反应,充分利用了
(6)工业上以硫铁矿为原料制硫酸所产生的尾气除了含有
 、
、 外,还含有
外,还含有 、微量的
、微量的 和酸雾。为了保护环境,同时提高硫酸工业的综合经济效益,按照下图工艺流程,将尾气中的
和酸雾。为了保护环境,同时提高硫酸工业的综合经济效益,按照下图工艺流程,将尾气中的 转化为有用的副产品。请回答下列问题。
转化为有用的副产品。请回答下列问题。
①写出氨吸收塔中主要发生的化学方程式
②写出二氧化硫吸收塔中主要发生的离子方程式
③当含
 烟气通入二氧化硫吸收塔中,可能发生氧化还原反应吗?如可能,请写出至少一个氧化还原反应的化学方程式
烟气通入二氧化硫吸收塔中,可能发生氧化还原反应吗?如可能,请写出至少一个氧化还原反应的化学方程式④上述流程可循环利用的物质是
您最近一年使用:0次
名校
解题方法
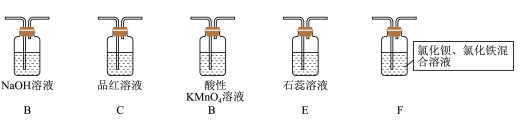
10 . 某同学设计了如下装置用于制取SO2和验证SO2的性质。
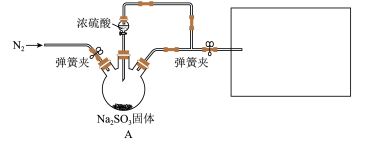
已知:Fe3+具有一定氧化性。
(1)装置 中发生反应的化学方程式为
中发生反应的化学方程式为_______ 。
(2)在框图内选择合适装置依次验证 的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为
的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为
_______ (填装置字母,还原性设计两个装置)。
(3)实验前必须鼓入N2,目的是_______ 。
(4)装置F中产生了白色沉淀,其成分是_______ (化学式),分析F中产生白色沉淀原因_______ 。
(5)实验中发现装置A中Na2SO3可能部分被氧化,现需测定Na2SO3的纯度:称取10.00g样品,配成100mL溶液;取其中的25.00mL溶液,与0.2000mol/L酸性KMnO4溶液发生以下反应:2MnO +5SO
+5SO +6H+=2Mn2++5SO
+6H+=2Mn2++5SO +3H2O,实验消耗KMnO4溶液20.00mL,以上样品中Na2SO3的质量分数为
+3H2O,实验消耗KMnO4溶液20.00mL,以上样品中Na2SO3的质量分数为_______ (保留三位有效数字)。
(6)查阅资料知:“尾气”可用双碱脱硫法处理,其过程如图所示:
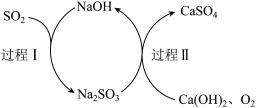
写出过程I的离子反应方程式_______ 。


已知:Fe3+具有一定氧化性。
(1)装置
 中发生反应的化学方程式为
中发生反应的化学方程式为(2)在框图内选择合适装置依次验证
 的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为
的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为
(3)实验前必须鼓入N2,目的是
(4)装置F中产生了白色沉淀,其成分是
(5)实验中发现装置A中Na2SO3可能部分被氧化,现需测定Na2SO3的纯度:称取10.00g样品,配成100mL溶液;取其中的25.00mL溶液,与0.2000mol/L酸性KMnO4溶液发生以下反应:2MnO
 +5SO
+5SO +6H+=2Mn2++5SO
+6H+=2Mn2++5SO +3H2O,实验消耗KMnO4溶液20.00mL,以上样品中Na2SO3的质量分数为
+3H2O,实验消耗KMnO4溶液20.00mL,以上样品中Na2SO3的质量分数为(6)查阅资料知:“尾气”可用双碱脱硫法处理,其过程如图所示:

写出过程I的离子反应方程式
您最近一年使用:0次



