1 . 环己烯是重要的化工原料。其实验室制备流程如下:
Ⅰ.环己烯的制备与提纯
(1)原料环己醇中若含苯酚杂质,检验试剂为_______ ,现象为_______ 。
(2)操作1的装置如图所示(加热和夹持装置已略去)。____ ,浓硫酸也可作该反应的催化剂,选择 而不用浓硫酸的原因为
而不用浓硫酸的原因为____ (填序号)。
a.浓硫酸易使原料炭化并产生
b. 污染小、可循环使用,符合绿色化学理念
污染小、可循环使用,符合绿色化学理念
c.同等条件下,用 比浓硫酸的平衡转化率高
比浓硫酸的平衡转化率高
②仪器C的名称为_______ 。仪器B的作用为_______ 。
(3)操作2用到的玻璃仪器是_______ 。
(4)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,_______ ,弃去前馏分,收集83℃的馏分。
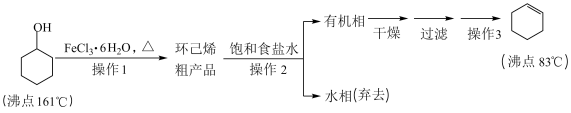
Ⅰ.环己烯的制备与提纯
(1)原料环己醇中若含苯酚杂质,检验试剂为
(2)操作1的装置如图所示(加热和夹持装置已略去)。

 而不用浓硫酸的原因为
而不用浓硫酸的原因为a.浓硫酸易使原料炭化并产生

b.
 污染小、可循环使用,符合绿色化学理念
污染小、可循环使用,符合绿色化学理念c.同等条件下,用
 比浓硫酸的平衡转化率高
比浓硫酸的平衡转化率高②仪器C的名称为
(3)操作2用到的玻璃仪器是
(4)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,
您最近一年使用:0次
解题方法
2 . 根据下列实验目的,对应的实验操作、实验现象和结论都正确的是
| 选项 | 实验目的 | 实验操作 | 实验现象和结论 |
| A | 探究钠在氧气中燃烧所得固体粉末的成分 | 取少量固体粉末,加入 蒸馏水 蒸馏水 | 若无气体生成,则固体粉末为 ;若有气体生成,则固体粉末为 ;若有气体生成,则固体粉末为 |
| B | 探究浓硫酸的性质 | 加热浓硫酸、 固体与 固体与 固体的混合物 固体的混合物 | 有黄绿色气体产生,证明浓硫酸具有强氧化性 |
| C | 探究麦芽糖的水解情况 | 向麦芽糖溶液中滴加稀硫酸,水浴加热,再加入 溶液至碱性,加入新制的 溶液至碱性,加入新制的 悬浊液,加热 悬浊液,加热 | 有砖红色沉淀产生,则可说明麦芽糖已发生水解 |
| D | 验证 和 和 的水解能力 的水解能力 | 将 液体和 液体和 固体分别暴露在潮湿空气中 固体分别暴露在潮湿空气中 | 只有前者会冒“白烟”,则水解能力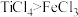 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 自然界中的含硫矿物有硫磺、黄铁矿(主要含FeS2)、雄黄(As4S4)、芒硝(Na2SO4·10H2O)等。以黄铁矿为原料经过煅烧可以获得SO2,SO2经过催化氧化反应2SO2(g)+O2(g) 2SO3(g)可制取SO3。SO3与H2O反应可以制取H2SO4。工业制硫酸尾气中的SO2可用氨水吸收。As4S4结构如下图所示,各原子最外层均达到8电子稳定结构。下列关于硫及其化合物的说法正确的是
2SO3(g)可制取SO3。SO3与H2O反应可以制取H2SO4。工业制硫酸尾气中的SO2可用氨水吸收。As4S4结构如下图所示,各原子最外层均达到8电子稳定结构。下列关于硫及其化合物的说法正确的是
 2SO3(g)可制取SO3。SO3与H2O反应可以制取H2SO4。工业制硫酸尾气中的SO2可用氨水吸收。As4S4结构如下图所示,各原子最外层均达到8电子稳定结构。下列关于硫及其化合物的说法正确的是
2SO3(g)可制取SO3。SO3与H2O反应可以制取H2SO4。工业制硫酸尾气中的SO2可用氨水吸收。As4S4结构如下图所示,各原子最外层均达到8电子稳定结构。下列关于硫及其化合物的说法正确的是
| A.自然界中硫都以化合态形式存在 |
| B.SO2大量排放到空气中会形成酸雨 |
| C.催化氧化时1molSO2可生成1molSO3 |
| D.硫酸浓度越大,挥发性越强 |
您最近一年使用:0次
4 . 关于实验室制备乙烯的实验,下列说法不正确的是
| A.将浓硫酸和乙醇以3∶1体积比混合加热反应得到 |
| B.实验结束后应该先熄灭酒精灯,再撤离导管 |
| C.使用乙醇制取乙烯发生了分子内脱水的反应 |
| D.生成的气体中除乙烯外还有浓硫酸被还原后生成的SO2 |
您最近一年使用:0次
名校
5 . 木炭与浓硫酸可发生反应: ,实验室利用下列装置进行实验并检验混合气体的成分,下列不能达到实验目的的是
,实验室利用下列装置进行实验并检验混合气体的成分,下列不能达到实验目的的是
 ,实验室利用下列装置进行实验并检验混合气体的成分,下列不能达到实验目的的是
,实验室利用下列装置进行实验并检验混合气体的成分,下列不能达到实验目的的是
| A.用装置甲发生木炭与浓硫酸的反应 | B.用装置乙检验气体产物中含水蒸气 |
C.用装置丙检验气体产物中含 | D.用装置丁检验气体产物中含 |
您最近一年使用:0次
6 . 某化学兴趣小组将制丝插入热浓硫酸中,进行如下图所示的 性质的探究实验。(a、b、c、d均为没有相应浴液的棉花,部分夹持仪器已略去)
性质的探究实验。(a、b、c、d均为没有相应浴液的棉花,部分夹持仪器已略去)_______ 。
(2)铜丝与热浓硫酸反应的化学方程式为_______ 。
(3)实验进行一段时间后:
①a处实验现象为_______ 。
②b处品红溶液褪色,原因是_______ 。
③c处酸性 溶液褪色,证明
溶液褪色,证明 具有
具有_______ 性。
④d处NaOH溶液的作用是_______ ,写出反应的离子方程式:_______ 。
(4)该实验装置中使用可抽动铜丝的优点是_______ 。
 性质的探究实验。(a、b、c、d均为没有相应浴液的棉花,部分夹持仪器已略去)
性质的探究实验。(a、b、c、d均为没有相应浴液的棉花,部分夹持仪器已略去)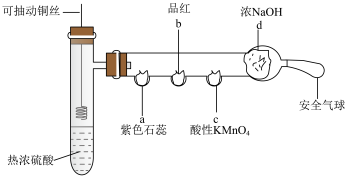
(2)铜丝与热浓硫酸反应的化学方程式为
(3)实验进行一段时间后:
①a处实验现象为
②b处品红溶液褪色,原因是
③c处酸性
 溶液褪色,证明
溶液褪色,证明 具有
具有④d处NaOH溶液的作用是
(4)该实验装置中使用可抽动铜丝的优点是
您最近一年使用:0次
2024-03-29更新
|
106次组卷
|
2卷引用:2023年6月福建省普通高中学业水平合格性考试化学试题
名校
解题方法
7 . 下列设计的实验方案能达到相应实验目的的是
| 选项 | 实验目的 | 实验方案 |
 | 探究化学反应的限度 | 取5 mL 0.1 mol/LKI溶液,滴加0.1 mol/LFeCl3溶液5~6滴,充分反应,可根据溶液中既含 又含 又含 的实验事实判断该反应是可逆反应 的实验事实判断该反应是可逆反应 |
 | 探究浓度对化学反应速率的影响 | 用两支试管各取5mL 0.1mol/L的KMnO4溶液,分别加入2mL 0.1mol/L和 0.2mol/L的H2C2O4(草酸)溶液,记录溶液褪色所需的时间 |
 | 抑制 水解,并防止 水解,并防止 被氧化 被氧化 | 配制 溶液时,先将 溶液时,先将 溶于适量浓盐酸中,再用蒸馏水稀释到所需浓度,最后在试剂瓶中加入少量铁粉 溶于适量浓盐酸中,再用蒸馏水稀释到所需浓度,最后在试剂瓶中加入少量铁粉 |
 | 比较不同浓度硫酸的酸性强弱 | 室温下,用 试纸分别测定浓度为 试纸分别测定浓度为 和 和 溶液的 溶液的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-03更新
|
95次组卷
|
2卷引用:江西省抚州市2022-2023学年高二上学期学生学业质量监测化学试题
8 . 下列离子方程式正确的是
A. 的水解方程:HS-+H2O=H2S+OH- 的水解方程:HS-+H2O=H2S+OH- |
B.铜与浓硫酸反应:Cu+4H++SO  Cu2++SO2↑+2H2O Cu2++SO2↑+2H2O |
C.向含1 mol NH4Al(SO4)2的溶液中加入含1.5 mol Ba(OH)2的溶液: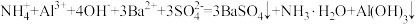 |
D.Na2CO3溶液中吸收少量Cl2[已知: : : |
您最近一年使用:0次
名校
解题方法
9 . 蔗糖与浓硫酸发生作用的过程如下图所示。

| A.过程①白色固体变黑,主要体现了浓硫酸的脱水性 |
| B.过程②固体体积膨胀,与产生的大量气体有关 |
| C.过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性 |
D.过程中发生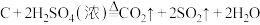 的反应 的反应 |
您最近一年使用:0次
2024-02-19更新
|
679次组卷
|
4卷引用:河南省南阳市邓州市第六高级中学校2023-2024学年高二下学期开学测试化学试题
名校
10 . NA为阿伏加德罗常数的值,下列说法正确的是
| A.0.1molCl2通入足量水中,溶液中的含氯微粒数目之和为0.2NA |
| B.10mL18mol/L的浓硫酸与足量Zn完全反应,转移的电子数大于0.18NA |
| C.0.01molFeCl3加入沸水制取的胶体中,含胶粒的数目为0.01NA |
| D.标准状况下,22.4LSO3中含有SO3分子NA |
您最近一年使用:0次



