名校
解题方法
1 . 将Na2O2分别投入到含有下列离子的溶液中,离子浓度明显减小的是
① ②I- ③
②I- ③ ④Ca2+ ⑤Cl- ⑥Na+
④Ca2+ ⑤Cl- ⑥Na+
①
 ②I- ③
②I- ③ ④Ca2+ ⑤Cl- ⑥Na+
④Ca2+ ⑤Cl- ⑥Na+| A.②③④⑤ | B.①③④⑤ | C.①②③④ | D.②③④ |
您最近一年使用:0次
2022-12-21更新
|
307次组卷
|
2卷引用:吉林省通化市梅河口市第五中学2022-2023学年高一上学期期末考试化学试题
解题方法
2 . 将过氧化钠投入FeCl2溶液中,可观察到的实验现象是
| A.无气体产生 | B.没有沉淀生成 |
| C.有红褐色沉淀生成 | D.有白色沉淀生成 |
您最近一年使用:0次
名校
解题方法
3 . 向盛有少量Na2O2的密闭容器(体积不变)中通入SO2,测定容器中O2的含量随时间变化曲线如图
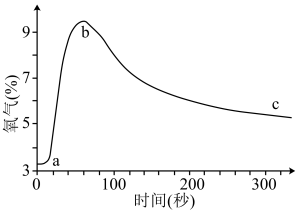
则下列说法错误的是

则下列说法错误的是
| A.ab段O2含量增加的原因:2Na2O2+2SO2=2Na2SO3+O2 |
| B.bc段O2含量缓慢降低的可能原因:反应生成O2的速率小于消耗O2的速率 |
| C.c点O2含量高于a点,则此时反应产物中含有Na2SO3 |
| D.取c点少量固体,加入BaCl2溶液有白色固体生成,证实有Na2SO4生成 |
您最近一年使用:0次
2022-10-17更新
|
191次组卷
|
3卷引用:陕西省西安交通大学附属中学2023-2024学年高一上学期期末考试化学试卷
4 . 实验小组研究SO2与Na2O2的反应。
(1)实验前分析物质的化学性质,提出假设:
假设1:SO2和CO2都是酸性氧化物。类比CO2与Na2O2的反应可知,SO2与Na2O2反应生成Na2SO3和O2;
假设2:SO2具有_______ 性,SO2与Na2O2反应生成Na2SO4。
(2)用如图所示装置进行SO2与Na2O2反应的实验。实验过程中,观察到C中淡黄色粉末逐渐变为白色,用带火星的木条靠近D中导气管口,木条复燃。

①A中反应产生SO2的化学方程式是_______ 。
②B中的试剂为_______ ,其主要作用是_______ 。
③实验证明假设_______ 正确。
(3)为检验C中是否有Na2SO4生成,设计如下方案:取少量C中反应后的白色固体溶解于水,加入BaCl2溶液,产生白色沉淀,再加入足量的稀HNO3,仍有白色沉淀不溶解,证明有Na2SO4生成。该方案是否合理?_______ (填“合理”或“不合理”)。请简要说明理由:_______ 。
(4)进一步实验证明C中反应后的固体中既有Na2SO3又有Na2SO4.从氧化还原反应的角度分析,+4价硫元素能被氧化为+6价。在上述实验条件下,+4价硫元素未完全转化为+6价,可见化学反应实际进行的情况与反应的_______ (只写一条)有关。
(1)实验前分析物质的化学性质,提出假设:
假设1:SO2和CO2都是酸性氧化物。类比CO2与Na2O2的反应可知,SO2与Na2O2反应生成Na2SO3和O2;
假设2:SO2具有
(2)用如图所示装置进行SO2与Na2O2反应的实验。实验过程中,观察到C中淡黄色粉末逐渐变为白色,用带火星的木条靠近D中导气管口,木条复燃。

①A中反应产生SO2的化学方程式是
②B中的试剂为
③实验证明假设
(3)为检验C中是否有Na2SO4生成,设计如下方案:取少量C中反应后的白色固体溶解于水,加入BaCl2溶液,产生白色沉淀,再加入足量的稀HNO3,仍有白色沉淀不溶解,证明有Na2SO4生成。该方案是否合理?
(4)进一步实验证明C中反应后的固体中既有Na2SO3又有Na2SO4.从氧化还原反应的角度分析,+4价硫元素能被氧化为+6价。在上述实验条件下,+4价硫元素未完全转化为+6价,可见化学反应实际进行的情况与反应的
您最近一年使用:0次
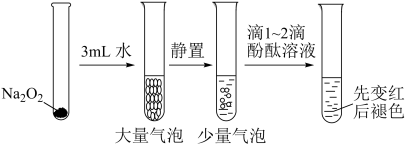
5 . 有关Na2O2性质实验如下:
②酚酞褪色原因与溶液的强碱性或强氧化性有关。
根据上述实验可以得出的结论是
②酚酞褪色原因与溶液的强碱性或强氧化性有关。
根据上述实验可以得出的结论是
| A.双氧水能使酚酞褪色 |
| B.浓氢氧化钠能使酚酞褪色 |
| C.双氧水和浓氢氧化钠都能使酚酞褪色 |
| D.可利用二氧化锰和水来完善实验方案 |
您最近一年使用:0次
2022-06-14更新
|
2198次组卷
|
10卷引用:上海市川沙中学2021-2022学年高一下学期期末考试化学试题
上海市川沙中学2021-2022学年高一下学期期末考试化学试题江苏省盐城市亭湖高级中学2023-2024学年高一上学期期末考试化学试题(已下线)第二章《海水中的重要元素----钠和氯》能力提升单元检测-【帮课堂】2022-2023学年高一化学同步精品讲义(人教版2019必修第一册)内蒙古乌兰浩特第一中学2022-2023学年高一上学期第三次月考化学试题上海市建平中学2022-2023学年高一下学期期中考试化学试题湖北省十堰市郧阳中学2022-2023学年高一上学期10月月考化学试题河北省石家庄市第二十四中学2023-2024学年高一上学期期中考试化学试题上海市浦东新区2021-2022学年高三下学期教学质量检测化学试题上海市育才中学2022-2023学年高三上学期10月月考化学试题(已下线)易错点05 钠及其化合物-备战2023年高考化学考试易错题
名校
6 . 许多非金属氧化物在一定条件下能与Na2O2反应,且反应有一定规律,如Na2O2+SO2═Na2SO4,2Na2O2+2SO3═2Na2SO4+O2据此,你认为下列反应方程式中正确的是
| A.Na2O2+2NO2═2NaNO3 | B.Na2O2+2NO2═2NaNO2+O2 |
| C.2Na2O2+2N2O3═4NaNO2+O2 | D.2Na2O2+2Mn2O7═4Na2MnO4+O2 |
您最近一年使用:0次
2022-06-02更新
|
695次组卷
|
3卷引用:云南省镇沅彝族哈尼族拉祜族自治县第一中学2022-2023学年高一下学期期末考试化学试题
云南省镇沅彝族哈尼族拉祜族自治县第一中学2022-2023学年高一下学期期末考试化学试题上海市嘉定区第一中学2021-2022学年高一下学期质量诊断二 化学试题(已下线)第07讲 钠及其氧化物-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )
7 . 下列关于钠及其化合物的说法正确的是
A. 与 与 都具有强还原性 都具有强还原性 |
B. 和 和 长期露置于空气中最终产物不相同 长期露置于空气中最终产物不相同 |
C.将足量的 、 、 和 和 分别加入含有酚酞的水中,最终溶液均变为红色 分别加入含有酚酞的水中,最终溶液均变为红色 |
D.将少量 和 和 分别投入 分别投入 溶液中,均既有沉淀生成又有气体放出 溶液中,均既有沉淀生成又有气体放出 |
您最近一年使用:0次
2022-05-11更新
|
1307次组卷
|
6卷引用:山东省日照市2021-2022学年高一上学期期末联考化学试题
山东省日照市2021-2022学年高一上学期期末联考化学试题浙江省舟山市普陀中学2021-2022学年高一下学期6月月考化学试题作业(八) 氧化钠和过氧化钠重庆市缙云教育联盟2022届高三第三次诊断性检测化学试题(已下线)专题05 元素及其化合物-2022年高考真题模拟题分项汇编(已下线)第07讲 钠及其重要化合物(练)-2023年高考化学一轮复习讲练测(全国通用)
8 . 已知:① 可与过氧化钠粉末发生化合反应生成
可与过氧化钠粉末发生化合反应生成 ,②
,② 能被酸性
能被酸性 溶液氧化成
溶液氧化成 。某兴趣小组设计了如下图所示的装置制备
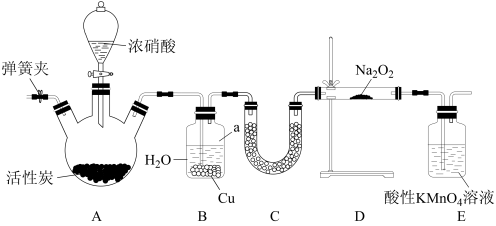
。某兴趣小组设计了如下图所示的装置制备 ,下列说法
,下列说法不正确 的是
 可与过氧化钠粉末发生化合反应生成
可与过氧化钠粉末发生化合反应生成 ,②
,② 能被酸性
能被酸性 溶液氧化成
溶液氧化成 。某兴趣小组设计了如下图所示的装置制备
。某兴趣小组设计了如下图所示的装置制备 ,下列说法
,下列说法
| A.装置A无需加热,滴入浓硝酸就能发生反应 |
| B.装置B中铜的作用是提高NO的生成率 |
| C.装置C中装的药品可以是氢氧化钠固体 |
D.装置E中的酸性 溶液的主要作用是吸收多余的NO 溶液的主要作用是吸收多余的NO |
您最近一年使用:0次
2022-05-05更新
|
1231次组卷
|
6卷引用:福建省福州金山中学2021-2022学年高一下学期期末考化学试题
福建省福州金山中学2021-2022学年高一下学期期末考化学试题江苏省高邮市重点中学2022届高三第一次诊断测试化学试题(已下线)第13练 氮及其化合物-2023年高考化学一轮复习小题多维练(全国通用)(已下线)2022年江苏卷高考真题变式题1-13山东省历城第二中学等学校2023届高三上学期10月月考联合考试化学试题 (已下线)江苏省2022年普通高中学业水平选择性考试变式题(选择题1-5)
名校
9 . 外观与NaCl相似的亚硝酸钠(NaNO2)可用作建筑钢材缓蚀剂。某学习小组设计如图装置制备亚硝酸钠(夹持装置已省略)。
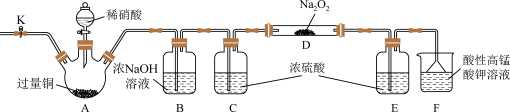
已知:2NO+Na2O2=2NaNO2,2NO2+Na2O2=2NaNO3。
回答下列问题:
(1)实验前应检查装置气密性,写出检查装置A气密性的操作步骤和结论:____ 。
(2)装置A中铜与稀硝酸反应的化学方程式为____ 。
(3)反应开始前先打开止水夹K,通入一段时间的氮气的目的是____ 。
(4)若想制备的亚硝酸钠更纯,装置B中浓NaOH溶液的作用是____ 。
(5)若没有装置C,则装置D中剩余固体为____ 。
(6)装置F处理尾气时,酸性高锰酸钾溶液中Mn全部转化为Mn2+,写出该反应的离子方程式:___ 。

已知:2NO+Na2O2=2NaNO2,2NO2+Na2O2=2NaNO3。
回答下列问题:
(1)实验前应检查装置气密性,写出检查装置A气密性的操作步骤和结论:
(2)装置A中铜与稀硝酸反应的化学方程式为
(3)反应开始前先打开止水夹K,通入一段时间的氮气的目的是
(4)若想制备的亚硝酸钠更纯,装置B中浓NaOH溶液的作用是
(5)若没有装置C,则装置D中剩余固体为
(6)装置F处理尾气时,酸性高锰酸钾溶液中Mn全部转化为Mn2+,写出该反应的离子方程式:
您最近一年使用:0次
2022-05-01更新
|
176次组卷
|
2卷引用:山西长治上党区第一中学校2021-2022学年高一下学期期末考试化学试题
名校
解题方法
10 . 下列物质的性质与应用关系的描述不正确的是
| A.氧化镁的熔点高,可用作耐高温材料 |
| B.金属钠具有还原性,可从CuSO4溶液中置换出铜 |
| C.过氧化钠有漂白性,可用于漂白纸浆及草帽等编织物 |
| D.碳酸钠溶液显碱性,其热溶液可除去物品表面的油污 |
您最近一年使用:0次



