1 . 实验室常采用点滴板来完成部分实验,这样既可以节约药品的用量,又便于观察实验现象。图中所示的实验点滴板上描述的实验现象或推论正确的是

A.往 固体中滴加FeCl2溶液,有气体产生且生成大量的白色沉淀 固体中滴加FeCl2溶液,有气体产生且生成大量的白色沉淀 |
| B.新制氯水滴加到pH试纸或淀粉KI 溶液孔穴中,都体现新制氯水的漂白性 |
C.生锈铁屑加过量稀硫酸后,通过滴加KMnO4溶液的褪色来验证原溶液中存在 |
| D.生锈铁屑加过量稀硫酸后,若滴加 KSCN溶液产生血红色沉淀可验证原溶液存在Fe3+ |
您最近一年使用:0次
2 .  是一种高效多功能水处理剂,应用前景十分看好。一种制备
是一种高效多功能水处理剂,应用前景十分看好。一种制备 的方法可用化学方程式表示为:
的方法可用化学方程式表示为: ,对此反应下列说法中不正确的是
,对此反应下列说法中不正确的是
 是一种高效多功能水处理剂,应用前景十分看好。一种制备
是一种高效多功能水处理剂,应用前景十分看好。一种制备 的方法可用化学方程式表示为:
的方法可用化学方程式表示为: ,对此反应下列说法中不正确的是
,对此反应下列说法中不正确的是A. 既作氧化剂又作还原剂 既作氧化剂又作还原剂 |
B.2  发生反应时,反应中共有8 发生反应时,反应中共有8 电子转移 电子转移 |
C.每生成 氧气就有 氧气就有  被氧化 被氧化 |
D. 既是还原产物又是氧化产物 既是还原产物又是氧化产物 |
您最近一年使用:0次
解题方法
3 . “奋斗者”号载人潜水器完成万米深潜海试,这标志着我国在大深度载人深潜领域达到世界领先水平。 可作载人潜水器供氧剂,下列关于
可作载人潜水器供氧剂,下列关于 的说法正确的有
的说法正确的有
①是一种白色固体
②与 反应有
反应有 生成
生成
③加入紫色石蕊试液中溶液最终变成蓝色
④可由Na与 在常温下反应制得
在常温下反应制得
⑤阴、阳离子的个数比为1:2
 可作载人潜水器供氧剂,下列关于
可作载人潜水器供氧剂,下列关于 的说法正确的有
的说法正确的有①是一种白色固体
②与
 反应有
反应有 生成
生成③加入紫色石蕊试液中溶液最终变成蓝色
④可由Na与
 在常温下反应制得
在常温下反应制得⑤阴、阳离子的个数比为1:2
| A.1种 | B.2种 | C.3种 | D.4种 |
您最近一年使用:0次
2024-03-27更新
|
67次组卷
|
2卷引用:云南省保山市腾冲市第八中学2023--2024学年高一上学期期末化学强化训练
解题方法
4 . 过氧化钠可用于医药、印染、漂白等。某学习兴趣小组探究Na2O2与NO2、NO的反应,设计如图所示实验。

(1)盛放浓硝酸的仪器M名称为_________ ,A中发生反应的离子方程式为________ 。
(2)Na2O2与NO2反应,根据化合价升降原则有下列两种观点。
观点一:Na2O2氧化NO2,生成NaNO3;
观点二:NO2氧化Na2O2,生成O2。
为验证以上观点的正确性进行如下实验:
①关闭K2和弹簧夹,打开K1和A中仪器M的活塞,再将带火星的木条放在a处,观察到_______ 。甲同学认为观点二正确。
②乙同学认为该装置不能确认观点二正确,应在A、G之间增加一个装置,该装置的作用为______ 。改进后重复甲同学的实验操作,观察到红棕色气体迅速消失,带火星的木条没有复燃。判断观点一正确。
(3)丙同学根据NO易与O2反应,预测NO也易与Na2O2反应。
①丙同学关闭K1,打开K2,用上图的装置进行实验,为防止NO与空气中氧气反应,反应前的操作是___________ 。
②装置B的作用为___________ 。
③反应一段时间后,取D装置中产物少许,加入稀硫酸,产生无色气体遇到空气变为红棕色。完成反应的化学方程式:___________ 。
6___________ 4___________
4___________
④根据D装置中产物的判断结果,说明Na2O2与NO反应中Na2O2的作用是___________ 。(填标号)
A.氧化剂 B.还原剂 C.即是氧化剂也是还原剂

(1)盛放浓硝酸的仪器M名称为
(2)Na2O2与NO2反应,根据化合价升降原则有下列两种观点。
观点一:Na2O2氧化NO2,生成NaNO3;
观点二:NO2氧化Na2O2,生成O2。
为验证以上观点的正确性进行如下实验:
①关闭K2和弹簧夹,打开K1和A中仪器M的活塞,再将带火星的木条放在a处,观察到
②乙同学认为该装置不能确认观点二正确,应在A、G之间增加一个装置,该装置的作用为
(3)丙同学根据NO易与O2反应,预测NO也易与Na2O2反应。
①丙同学关闭K1,打开K2,用上图的装置进行实验,为防止NO与空气中氧气反应,反应前的操作是
②装置B的作用为
③反应一段时间后,取D装置中产物少许,加入稀硫酸,产生无色气体遇到空气变为红棕色。完成反应的化学方程式:
6___________
 4___________
4___________
④根据D装置中产物的判断结果,说明Na2O2与NO反应中Na2O2的作用是
A.氧化剂 B.还原剂 C.即是氧化剂也是还原剂
您最近一年使用:0次
名校
解题方法
5 . 化学实验是研究物质组成和探究物质性质的重要途径。
Ⅰ.某澄清透明溶液(忽略水的电离),可能含有Fe3+、Mg2+、K+、CO 、SO
、SO 、Ba2+、MnO
、Ba2+、MnO 等离子中的几种,且离子的物质的量相等(即离子数目相等),为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如图所示。请你根据上述实验推断:
等离子中的几种,且离子的物质的量相等(即离子数目相等),为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如图所示。请你根据上述实验推断:
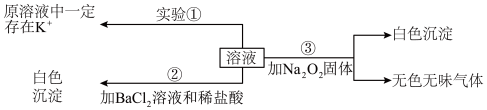
(1)实验①的焰色试验,需要透过_______ ,来观察火焰的颜色。
(2)取100mL溶液进行实验②,经足量盐酸洗涤、干燥后,得沉淀质量为2.33g。该溶液中K+的物质的量浓度为________ 。
(3)实验③产生的无色无味气体为________ ,白色沉淀为_______ (填物质化学式)。原溶液中一定存在的离子有_______ 。
(4)向该溶液中加入硫酸酸化,再通入SO2气体,发生反应使该溶液的颜色发生变化,写出该反应的离子方程式_______ 。
Ⅱ.Na2O2具有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测,Na2O2与H2能发生反应。为了验证此推测结果,该同学设计并进行了如图所示实验。其中装置A用锌和稀盐酸制取氢气。
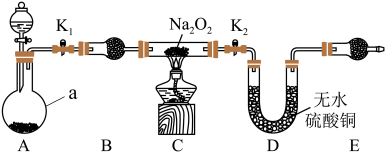
(5)装置B中的试剂是________ 。
(6)下面是实验过程中的重要操作,正确的顺序是_______。
(7)实验过程中观察到淡黄色粉末慢慢变成白色固体,无水硫酸铜未变蓝色。由此可推测出Na2O2与H2反应生成的产物为_______ 。
Ⅰ.某澄清透明溶液(忽略水的电离),可能含有Fe3+、Mg2+、K+、CO
 、SO
、SO 、Ba2+、MnO
、Ba2+、MnO 等离子中的几种,且离子的物质的量相等(即离子数目相等),为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如图所示。请你根据上述实验推断:
等离子中的几种,且离子的物质的量相等(即离子数目相等),为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如图所示。请你根据上述实验推断:
(1)实验①的焰色试验,需要透过
(2)取100mL溶液进行实验②,经足量盐酸洗涤、干燥后,得沉淀质量为2.33g。该溶液中K+的物质的量浓度为
(3)实验③产生的无色无味气体为
(4)向该溶液中加入硫酸酸化,再通入SO2气体,发生反应使该溶液的颜色发生变化,写出该反应的离子方程式
Ⅱ.Na2O2具有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测,Na2O2与H2能发生反应。为了验证此推测结果,该同学设计并进行了如图所示实验。其中装置A用锌和稀盐酸制取氢气。

(5)装置B中的试剂是
(6)下面是实验过程中的重要操作,正确的顺序是_______。
| A.加热至Na2O2逐渐熔化,反应一段时间 | B.用小试管收集气体并检验其纯度 |
| C.打开K1、K2,通入氢气 | D.停止加热,充分冷却,关闭K1、K2 |
(7)实验过程中观察到淡黄色粉末慢慢变成白色固体,无水硫酸铜未变蓝色。由此可推测出Na2O2与H2反应生成的产物为
您最近一年使用:0次
6 . 化学实验中颜色变化丰富多彩。下列说法正确的是
A.向 固体中加入适量水后,滴加 固体中加入适量水后,滴加 溶液,产生浅绿色沉淀 溶液,产生浅绿色沉淀 |
B.用洁净的铂丝蘸取 溶液,在酒精灯外焰上灼烧,火焰呈紫色 溶液,在酒精灯外焰上灼烧,火焰呈紫色 |
| C.向滴有酚酞的水中加入一块绿豆粒大的钾,反应后溶液显红色 |
| D.向溴化钾溶液中滴加几滴新制氯水,溶液变成紫色 |
您最近一年使用:0次
2024-01-30更新
|
77次组卷
|
3卷引用:安徽省阜阳市2023-2024学年高一上学期期末联考化学试卷
7 . 下列“类比”合理的是
A.浓 常温下能溶解 常温下能溶解 ,则浓 ,则浓 常温下也能溶解 常温下也能溶解 |
B. 与 与 反应生成 反应生成 和 和 ,则 ,则 与 与 反应生成 反应生成 和 和 |
C.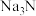 与盐酸反应生成 与盐酸反应生成 和 和 ,则 ,则 与盐酸反应生成 与盐酸反应生成 和 和 |
D. 的溶解度比 的溶解度比 大,则 大,则 的溶解度比 的溶解度比 大 大 |
您最近一年使用:0次
名校
解题方法
8 . 某同学结合所学知识探究 与
与 能否反应,设计装置如下,下列说法正确的是
能否反应,设计装置如下,下列说法正确的是

 与
与 能否反应,设计装置如下,下列说法正确的是
能否反应,设计装置如下,下列说法正确的是
A.装置 也可直接用于 也可直接用于 与浓盐酸反应制取 与浓盐酸反应制取 |
B.装置 气密性检查方法:直接向长颈漏斗中加水,当漏斗中液面高于试管液面且高度不变说明气密性良好 气密性检查方法:直接向长颈漏斗中加水,当漏斗中液面高于试管液面且高度不变说明气密性良好 |
C.装置 中盛放无水氯化钙,其作用是除去 中盛放无水氯化钙,其作用是除去 中挥发出来的少量水蒸气 中挥发出来的少量水蒸气 |
D.装置 加热前,用试管在 加热前,用试管在 中管口末端处收集气体点燃,通过声音判断气体纯度 中管口末端处收集气体点燃,通过声音判断气体纯度 |
您最近一年使用:0次
解题方法
9 . 下列关于钠及其化合物的说法正确的是
A. 和 和 都具有强还原性 都具有强还原性 |
B. 和 和 长期露置于空气中,最终产物不相同 长期露置于空气中,最终产物不相同 |
C.将足量的 和 和 分别加入含有酚酞的水中,最终所得溶液均为红色 分别加入含有酚酞的水中,最终所得溶液均为红色 |
D.将少量 和 和 分别加入 分别加入 溶液中,均产生蓝色沉淀同时放出无色气体 溶液中,均产生蓝色沉淀同时放出无色气体 |
您最近一年使用:0次
2024-01-13更新
|
140次组卷
|
2卷引用:云南省昆明市五华区2023-2024学年高一上学期1月期末化学试题
名校
解题方法
10 . 有人设计出一种在隔绝空气条件下让钠与 溶液反应,观察
溶液反应,观察 颜色的实验。实验时,往
颜色的实验。实验时,往 的大试管中先加
的大试管中先加 煤油,取
煤油,取 粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入
粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入 溶液
溶液 不含
不含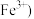 使煤油的液面至橡胶塞,并夹紧弹簧夹
使煤油的液面至橡胶塞,并夹紧弹簧夹 如图所示
如图所示 。下列说法错误的是
。下列说法错误的是

 溶液反应,观察
溶液反应,观察 颜色的实验。实验时,往
颜色的实验。实验时,往 的大试管中先加
的大试管中先加 煤油,取
煤油,取 粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入
粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入 溶液
溶液 不含
不含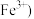 使煤油的液面至橡胶塞,并夹紧弹簧夹
使煤油的液面至橡胶塞,并夹紧弹簧夹 如图所示
如图所示 。下列说法错误的是
。下列说法错误的是

| A.长颈漏斗中的液面上升 |
| B.大试管下层溶液出现白色沉淀,并可持续较长时间 |
| C.用过氧化钠代替钠也可以观察到此现象 |
| D.该反应同时也能说明钠不能与硫酸亚铁溶液发生置换反应 |
您最近一年使用:0次
2023-10-05更新
|
243次组卷
|
4卷引用:北京师范大学附属中学2023-2024学年高一上学期期末考试化学试卷
北京师范大学附属中学2023-2024学年高一上学期期末考试化学试卷安徽省肥东县综合高中2022-2023学年高一上学期11月期中化学试题广东省东莞市东莞中学松山湖学校2023-2024学年高一上学期期中考试化学试卷(已下线)专题03 铁 金属材料-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)



