名校
1 . 类比思想是化学学习中的重要思想,下列各项中由客观事实类比得到的结论正确的是
| 选项 | 客观事实 | 类比结论 |
| A | 电解熔融的 制备镁 制备镁 | 电解熔融的 可制备铝 可制备铝 |
| B |  与 与 溶液反应生成 溶液反应生成 |  与 与 溶液反应可生成 溶液反应可生成 |
| C |  与 与 反应生成 反应生成 和 和 |  与 与 反应生成 反应生成 和 和 |
| D |  可作净水剂 可作净水剂 |  也可作净水剂 也可作净水剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-08更新
|
303次组卷
|
4卷引用:河北省沧州市2022-2023学年高三上学期期末考试化学试题
名校
2 . SO2虽是大气污染物之一,但也是重要的工业原料。某同学在实验室设计了如下实验,对SO2的部分性质进行了探究。
I.二氧化硫的水溶性
(1) SO2易溶于水,溶于水有H2SO3生成。向SO2饱和溶液中加入NaHSO3固体,有气体冒出,原因是_______ (结合有关平衡方程式简要说明)。
II.验证SO2能否与BaCl2溶液反应
某同学设计了如图装置,且所配制的溶液均使用了无氧蒸馏水,检验SO2在无氧干扰时,是否与氯化钡反应生成沉淀。
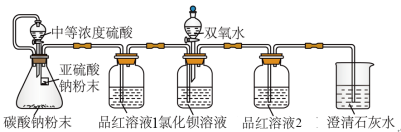
(2)加入碳酸钠粉末的目的是_______ 。
(3)当_______ 时,氯化钡溶液中没有沉淀出现,说明二氧化硫不与氯化钡溶液反应,此时滴加双氧水,出现了白色沉淀。
(4)装置中选用澄清石灰水而不用氢氧化钠溶液的目的是_______ 。
III.二氧化硫的还原性
已知SO2具有还原性,可以还原I2,也可以与Na2O2发生反应。
(5)将SO2通入装有过氧化钠的硬质试管中,将带火星的木条放在试管口处。
①若木条不复燃,则说明SO2与Na2O2反应无O2生成,可能发生反应的化学方程式为_______ 。
②若木条复燃,则说明SO2与Na2O2反应有O2生成,发生反应的化学方程式为2Na2O2+2SO2=2Na2SO3+O2。
(6)将SO2通入装有碘水(含淀粉)的洗气瓶中,若_______ ,说明还原性:SO2>I-,写出该反应的离子方程式:_______ 。
I.二氧化硫的水溶性
(1) SO2易溶于水,溶于水有H2SO3生成。向SO2饱和溶液中加入NaHSO3固体,有气体冒出,原因是
II.验证SO2能否与BaCl2溶液反应
某同学设计了如图装置,且所配制的溶液均使用了无氧蒸馏水,检验SO2在无氧干扰时,是否与氯化钡反应生成沉淀。

(2)加入碳酸钠粉末的目的是
(3)当
(4)装置中选用澄清石灰水而不用氢氧化钠溶液的目的是
III.二氧化硫的还原性
已知SO2具有还原性,可以还原I2,也可以与Na2O2发生反应。
(5)将SO2通入装有过氧化钠的硬质试管中,将带火星的木条放在试管口处。
①若木条不复燃,则说明SO2与Na2O2反应无O2生成,可能发生反应的化学方程式为
②若木条复燃,则说明SO2与Na2O2反应有O2生成,发生反应的化学方程式为2Na2O2+2SO2=2Na2SO3+O2。
(6)将SO2通入装有碘水(含淀粉)的洗气瓶中,若
您最近一年使用:0次
2022-12-31更新
|
305次组卷
|
2卷引用:广东省梅州市名校2022-2023学年高三上学期期末考试化学试题
名校
解题方法
3 . 某种化合物由W、X、Y、Z四种短周期元素组成,结构如图。其中W、Y、Z分别位于三个不同周期,Y核外最外层电子数是W核外最外层电子数的2倍;W、X、Y三种简单离子的核外电子排布相同。下列说法错误的是
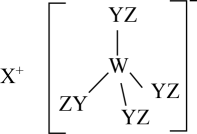

A. 是一种比较好的耐火材料 是一种比较好的耐火材料 |
| B.X与Y;Y与Z均可形成具有漂白性的化合物 |
| C.第一电离能:X>W |
| D.W与X的最高价氧化物的水化物可相互反应 |
您最近一年使用:0次
解题方法
4 . 下列实验操作、现象和结论均正确的是
| 实验操作 | 现象 | 结论 | |
| A | 向某溶液中滴加Ba(NO3)2和HNO3混合溶液 | 生成白色沉淀 | 原溶液中有SO |
| B | 将过量的过氧化钠投入滴有酚酞试液的水中 | 最终得红色溶液 | 过氧化钠与水反应生成碱性物质 |
| C | 将H2在充满Cl2的集气瓶中燃烧 | 集气瓶口上方有白烟生成 | H2、Cl2化合生成HCl |
| D | 向浓度均为0.1mol·L-1NaCl和NaI的混合溶液中滴加少量AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . Na2O2具有强氧化性,可以用来漂白纺织类物品、麦秆、羽毛等,也可做呼吸面具中的供氧剂。
(1)某实验小组通过下列实验探究过氧化钠与水的反应:
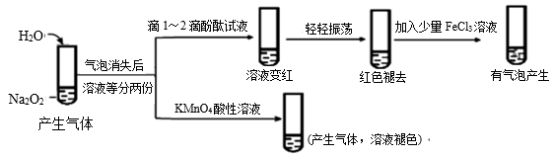
①依据实验现象推测红色褪去的原因是_________________ 。
②加入FeCl3反应的化学方程式为________________________ 。
③用离子方程式解释加入高锰酸钾溶液褪色的原因___________________ 。
(2)实验小组两名同学共同设计如下装置探究过氧化钠与二氧化硫的反应。通入SO2,将带余烬的木条插入试管C中,木条复燃。
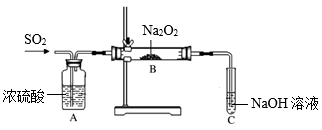
请回答下列问题:
①甲同学认为Na2O2与SO2反应生成了Na2SO3和O2,检验有Na2SO3生成的实验方法是___________ 。
②乙同学认为反应的后B中有Na2SO3还会有Na2SO4。乙同学猜想的理由是__________ 。
③为检验产物中Na2SO4的存在,乙同学设计并实施了如下实验方案:
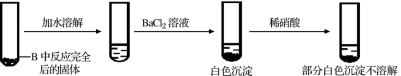
甲同学认为该实验方案的现象不能证明有Na2SO4生成,用反应方程式解释其原因_______ ;改进的方法为______________________ 。
(1)某实验小组通过下列实验探究过氧化钠与水的反应:

①依据实验现象推测红色褪去的原因是
②加入FeCl3反应的化学方程式为
③用离子方程式解释加入高锰酸钾溶液褪色的原因
(2)实验小组两名同学共同设计如下装置探究过氧化钠与二氧化硫的反应。通入SO2,将带余烬的木条插入试管C中,木条复燃。

请回答下列问题:
①甲同学认为Na2O2与SO2反应生成了Na2SO3和O2,检验有Na2SO3生成的实验方法是
②乙同学认为反应的后B中有Na2SO3还会有Na2SO4。乙同学猜想的理由是
③为检验产物中Na2SO4的存在,乙同学设计并实施了如下实验方案:

甲同学认为该实验方案的现象不能证明有Na2SO4生成,用反应方程式解释其原因
您最近一年使用:0次
2021-01-16更新
|
358次组卷
|
3卷引用:河南省新蔡县2021届高三上学期期末调研考试化学试题
河南省新蔡县2021届高三上学期期末调研考试化学试题(已下线)第06讲 钠及其化合物(练) — 2022年高考化学一轮复习讲练测(新教材新高考)山西省临汾市2022-2023学年高一上学期9月月考化学试题
6 . 过氧化钙是一种白色固体,微溶于冷水,不溶于乙醇,化学性质与过氧化钠类似。某学习小组设计在碱性环境中利用CaCl2与H2O2反应制取CaO2·8H2O,装置如下图所示:
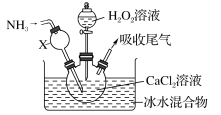
回答下列问题:
(1)小组同学查阅文献得知:该实验用质量分数为20%的H2O2溶液最为适宜。市售H2O2溶液的质量分数为30%。该小组同学用市售H2O2溶液配制约20%的H2O2溶液的过程中,使用的玻璃仪器除玻璃棒、胶头滴管外,还有___________ 。
(2)仪器X的主要作用除导气外,还具有的作用是_________ 。
(3)在冰水浴中进行的原因是_________ 。
(4)实验时,在三颈烧瓶中析出CaO2·8H2O晶体,总反应的离子方程式为_________ 。
(5)反应结束后,经过滤、洗涤、低温烘干获得CaO2·8H2O。下列试剂中,洗涤CaO2·8H2O的最佳选择是_______ 。
A.无水乙醇 B.浓盐酸 C.Na2SO3溶液 D.CaCl2溶液
(6)若CaCl2原料中含有Fe3+杂质,Fe3+催化分解H2O2,会使H2O2的利用率明显降低。反应的机理为:
①Fe3++H2O2===Fe2++H++HOO·
②H2O2+X===Y+Z+W(已配平)
③Fe2++·OH===Fe3++OH-
④H++OH-===H2O
根据上述机理推导步骤②中的化学方程式为____________ 。
(7)如图所示装置,安全漏斗在实验中的作用除了滴加液体外,还有______________ 。
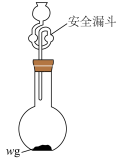

回答下列问题:
(1)小组同学查阅文献得知:该实验用质量分数为20%的H2O2溶液最为适宜。市售H2O2溶液的质量分数为30%。该小组同学用市售H2O2溶液配制约20%的H2O2溶液的过程中,使用的玻璃仪器除玻璃棒、胶头滴管外,还有
(2)仪器X的主要作用除导气外,还具有的作用是
(3)在冰水浴中进行的原因是
(4)实验时,在三颈烧瓶中析出CaO2·8H2O晶体,总反应的离子方程式为
(5)反应结束后,经过滤、洗涤、低温烘干获得CaO2·8H2O。下列试剂中,洗涤CaO2·8H2O的最佳选择是
A.无水乙醇 B.浓盐酸 C.Na2SO3溶液 D.CaCl2溶液
(6)若CaCl2原料中含有Fe3+杂质,Fe3+催化分解H2O2,会使H2O2的利用率明显降低。反应的机理为:
①Fe3++H2O2===Fe2++H++HOO·
②H2O2+X===Y+Z+W(已配平)
③Fe2++·OH===Fe3++OH-
④H++OH-===H2O
根据上述机理推导步骤②中的化学方程式为
(7)如图所示装置,安全漏斗在实验中的作用除了滴加液体外,还有

您最近一年使用:0次
解题方法
7 . 表中陈述I、II均正确,且两者在反应原理上相似的是
| 选项 | 陈述I | 陈述II |
| A | 向酚酞溶液中加Na2O2,溶液先变红后褪色色 | 向石蕊溶液中通入Cl2,溶液先变红后褪色 |
| B | 将SO2和Cl2同时通入BaCl2溶液中,产生白色沉淀 | 将CO2和NH3同时通入CaCl2溶液中,产生白色沉淀 |
| C | 向MgCl2溶液中加入NaOH溶液生成白色沉淀 | 向FeCl3溶液中加入NaOH溶液生成红褐色沉淀 |
| D | Na投入水中产生大量气泡 | Na2CO3投入盐酸中产生大量气泡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 将过氧化钠加入到氯化亚铁溶液中,最终可以观察到的现象是( )
| A.过氧化钠将溶液漂白 | B.生成红褐色沉淀 |
| C.除溶解外无特殊现象产生 | D.生成白色沉淀 |
您最近一年使用:0次
2018-01-08更新
|
330次组卷
|
2卷引用:上海市长宁(嘉定)区2017-2018学年高三第一学期期末教学质量检测化学试卷
名校
9 . Na2O2具有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测Na2O2与H2能发生反应。为了验证此推测结果,该同学设计并进行如下实验。
I.实验探究
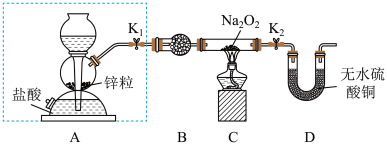
步骤1:按如图所示的装置组装仪器(图中夹持仪器已省略)并检查装置的气密性,然后装入药品。
步骤2:打开K1、K2,在产生的氢气流经装有Na2O2的硬质玻璃管的过程中,未观察到明显现象。
步骤3:进行必要的实验操作,淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝色。
(1)组装好仪器后,要检查装置的气密性。简述检查虚线框内装置气密性的方法:________ 。
(2)B装置中所盛放的试剂是_____ ,其作用是_______ 。
(3)步骤3中的必要操作为打开K1、K2,_______ (请按正确的顺序填入下列步骤的字母)。
A.加热至Na2O2逐渐熔化,反应一段时间
B.用小试管收集气体并检验其纯度
C.关闭K1
D.停止加热,充分冷却
(4)由上述实验可推出Na2O2与H2反应的化学方程式为__________ 。
II.数据处理
(5)实验结束后,该同学欲测定C装置硬质玻璃管内白色固体中未反应完的Na2O2含量。
其操作流程如下:

①测定过程中需要的仪器除固定、夹持仪器外,还有电子天平、烧杯、酒精灯、蒸发皿和____ 。
②在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数_____ (填“偏大”“偏小”或“不变”)
I.实验探究

步骤1:按如图所示的装置组装仪器(图中夹持仪器已省略)并检查装置的气密性,然后装入药品。
步骤2:打开K1、K2,在产生的氢气流经装有Na2O2的硬质玻璃管的过程中,未观察到明显现象。
步骤3:进行必要的实验操作,淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝色。
(1)组装好仪器后,要检查装置的气密性。简述检查虚线框内装置气密性的方法:
(2)B装置中所盛放的试剂是
(3)步骤3中的必要操作为打开K1、K2,
A.加热至Na2O2逐渐熔化,反应一段时间
B.用小试管收集气体并检验其纯度
C.关闭K1
D.停止加热,充分冷却
(4)由上述实验可推出Na2O2与H2反应的化学方程式为
II.数据处理
(5)实验结束后,该同学欲测定C装置硬质玻璃管内白色固体中未反应完的Na2O2含量。
其操作流程如下:

①测定过程中需要的仪器除固定、夹持仪器外,还有电子天平、烧杯、酒精灯、蒸发皿和
②在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数
您最近一年使用:0次
2017-10-30更新
|
1131次组卷
|
9卷引用:河北省承德市各县第一中学2018届高三上学期期末考试化学试题
河北省承德市各县第一中学2018届高三上学期期末考试化学试题江西省百所名校2018届高三第一次联合考试化学试题山西省大同市2020届高三第一次联合考试(县区)化学试题(已下线)第三章 能力提升检测卷(测)——2021年高考化学一轮复习讲练测河北省廊坊市2018-2019学年高二下学期期末考试化学试题甘肃省天水市第一中学2021届高三上学期第一学段考试化学试题(已下线)第06讲 钠及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第1讲 钠及其重要化合物湖南省衡阳市第八中学2017-2018学年高一(理科实验班)上学期第一次月考理综化学试题
名校
解题方法
10 . 把少量过氧化钠投入下列溶液中,一定会有白色沉淀生成的是( )
| A.1mol/L氢氧化钠 | B.饱和碳酸氢钠 |
| C.1mol/L硫酸亚铁 | D.饱和碳酸钠 |
您最近一年使用:0次
2016-12-09更新
|
256次组卷
|
3卷引用:上海市浦东新区2016届高三上学期期末质量抽测化学试题



