2015届广东省清远市高三上学期期末理综化学试卷
广东
高三
期末
2017-07-26
526次
整体难度:
适中
考查范围:
有机化学基础、化学与STSE、认识化学科学、化学反应原理、常见无机物及其应用、化学实验基础、物质结构与性质
2015届广东省清远市高三上学期期末理综化学试卷
广东
高三
期末
2017-07-26
526次
整体难度:
适中
考查范围:
有机化学基础、化学与STSE、认识化学科学、化学反应原理、常见无机物及其应用、化学实验基础、物质结构与性质
一、单选题 添加题型下试题
单选题
|
较易(0.85)
1. 化学在生产和日常生活中有着重要的作用。下列有关说法不正确的是
| A.雾霾天气对人的健康造成危害,“雾”和“霾”的分散质微粒不相同 |
| B.氢氧化铁溶胶、蔗糖溶液、淀粉溶液均具有丁达尔效应 |
| C.“地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |
| D.只要符合限量,“食用色素”、“亚硝酸盐”可以作为某些食品的添加剂 |
【知识点】 油脂的性质 化学科学对人类文明发展的意义解读 食品添加剂解读
您最近一年使用:0次
2016-12-09更新
|
194次组卷
|
2卷引用:2015届广东省清远市高三上学期期末理综化学试卷
单选题
|
适中(0.64)
2. 下列各组离子在水溶液中能大量共存的是
| A.Na+、HCO3—、SO32—、OH— | B.Al3+、H+、SiO32—、I— |
| C.Fe2+、K+、NO3—、SO42— | D.Fe3+、NH4+、ClO—、CO32— |
【知识点】 离子共存
您最近一年使用:0次
单选题
|
适中(0.65)
3. NA为阿伏加德罗常数,下列说法正确的是
| A.同温同压同体积的CO2和SO2所含氧原子数均为2NA |
| B.32gCu与S完全反应转移的电子数为NA(相对原子质量 Cu:64) |
| C.1L 1.0mol·L—1 NH4Cl与2L 0.5mol·L—1 NH4Cl溶液含NH4+数目相同 |
| D.25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH— 数目为0.1NA |
您最近一年使用:0次
2016-12-09更新
|
1113次组卷
|
3卷引用:2014届广东省深圳市高三第二次调研考试理综化学试卷
单选题
|
适中(0.65)
4. 常温下,下列有关物质的量浓度关系正确的是
| A.等物质的量浓度的溶液中,水电离出的c(H+):HCl>CH3COOH |
| B.pH相同的溶液中:c(Na2CO3)<c(NaHCO3) |
| C.在Na2SO3溶液中:c(Na+) = 2c(SO32— ) + c(HSO3— ) + c(OH— ) |
| D.0.1mol·L—1NaHS溶液中:c(Na+) = c(HS-) |
您最近一年使用:0次
单选题
|
适中(0.65)
5. 下列实验现象对应的结论正确的是( )
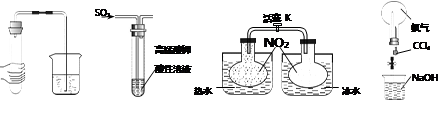
①气密性检查 ②气体性质检验 ③化学平衡的探究 ④喷泉实验
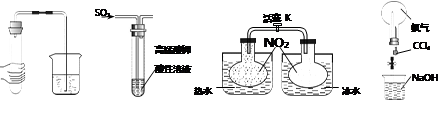
①气密性检查 ②气体性质检验 ③化学平衡的探究 ④喷泉实验
| 选项 | 现象 | 结论 |
| A | ①中导管口冒气泡,手松开无现象 | 气密性良好 |
| B | ②中KMnO4溶液紫红色褪去 | SO2具有漂白性 |
| C | ③中关闭K,气体颜色在热水中比冷水深 | NO2生成N2O4为吸热反应 |
| D | ④中烧瓶中形成喷泉 | Cl2易溶于CCl4 |
| A.A | B.B | C.C | D.D |
【知识点】 氯气 化学平衡的移动及其影响因素 仪器使用与实验安全 综合实验设计与评价解读
您最近一年使用:0次
2014-05-06更新
|
1383次组卷
|
5卷引用:2014届广东省深圳市高三第二次调研考试理综化学试卷
(已下线)2014届广东省深圳市高三第二次调研考试理综化学试卷2015届广东省清远市高三上学期期末理综化学试卷2016届广东省深圳第二外国语学校高三上学期第二次教学质检化学试卷2016届山东省泰安市高三上学期期末考试化学试卷(已下线)2019年3月13日《每日一题》二轮复习 有关气体的制备和性质
单选题
|
较易(0.85)
名校
6. 有关金属的腐蚀与防护的叙述正确的是


| A.金属的化学腐蚀比电化学发生普遍 |
| B.上图装置的原理是“牺牲阳极的阴极保护法” |
| C.金属腐蚀的本质是M-ne-→Mn+而被损耗 |
| D.用铝制铆钉来接铁板,铁板易被腐蚀 |
您最近一年使用:0次
2016-12-09更新
|
376次组卷
|
4卷引用:2015届广东省清远市高三上学期期末理综化学试卷
2015届广东省清远市高三上学期期末理综化学试卷上海市上海交通大学附属中学2018届高三10月月考化学试题(已下线)上海市杨浦区2014届高三三模化学试题(已下线)1.3.2 金属的电化学防护(重点练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)
二、多选题 添加题型下试题
多选题
|
适中(0.65)
7. 下图所示的五种元素中,W、X、Y、Z为短周期元素,X元素的单质是空气中含量最多的成分。下列说法正确的是
| X | Y | ||
| W | Z | ||
| T |
| A.X位于元素周期表中第二周期ⅤA族 |
| B.X、Y、Z三种元素的气态氢化物的稳定性依次减弱 |
| C.由X、Y和氢三种元素形成的化合物中只有共价键 |
| D.元素T与X的原子序数相差25 |
【知识点】 金属与非金属在周期表中位置及其性质递变的规律
您最近一年使用:0次
多选题
|
适中(0.65)
解题方法
8. 表中陈述I、II均正确,且两者在反应原理上相似的是
| 选项 | 陈述I | 陈述II |
| A | 向酚酞溶液中加Na2O2,溶液先变红后褪色色 | 向石蕊溶液中通入Cl2,溶液先变红后褪色 |
| B | 将SO2和Cl2同时通入BaCl2溶液中,产生白色沉淀 | 将CO2和NH3同时通入CaCl2溶液中,产生白色沉淀 |
| C | 向MgCl2溶液中加入NaOH溶液生成白色沉淀 | 向FeCl3溶液中加入NaOH溶液生成红褐色沉淀 |
| D | Na投入水中产生大量气泡 | Na2CO3投入盐酸中产生大量气泡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
三、填空题 添加题型下试题
填空题
|
较难(0.4)
9. 2—甲基—2—丁烯酸甲酯是一种重要的化工原料。下面是该物质的一种合成路线:
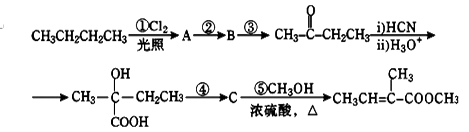
已知:R-CN R-COOH。请回答下列问题:
R-COOH。请回答下列问题:
(1)A是一氯代烷,则其结构简式为_____________ ,反应②的反应条件是_____________ ;
(2)写出反应③的化学方程式:__________________________________________ 。
(3)C的结构简式为______________ ,其所含官能团的名称是________________ 。
(4)步骤④的反应类型是______________ 。
(5)2—甲基—2—丁烯酸甲酯的某种羧酸类链状同分异构体X,分子中含有3个甲基。则X的结构简式为__________________________ 。
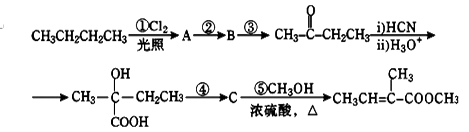
已知:R-CN
 R-COOH。请回答下列问题:
R-COOH。请回答下列问题:(1)A是一氯代烷,则其结构简式为
(2)写出反应③的化学方程式:
(3)C的结构简式为
(4)步骤④的反应类型是
(5)2—甲基—2—丁烯酸甲酯的某种羧酸类链状同分异构体X,分子中含有3个甲基。则X的结构简式为
【知识点】 有机物的合成与推断
您最近一年使用:0次
填空题
|
较难(0.4)
10. 随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%,CO2的排放量也要大幅减少。
Ⅰ.处理NOx的一种方法是利用甲烷催化还原NOx。
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2
③CH4(g)+2NO2 (g)= N2(g) + CO2(g)+2H2O(g) △H3=-867kJ·mol-1
则△H2=_________________ 。
Ⅱ.化石燃料的燃烧、含硫金属矿石的冶炼和硫酸的生产过程中产生的SO2是大气中SO2的主要来源。
(1)将煤转化为水煤气是将煤转化为洁净燃料的方法之一,反应为C(s) + H2O(g) CO(g) + H2(g)
CO(g) + H2(g)
①该反应的化学平衡常数表达式为:K=____________________ 。
②800℃时,将1molCO、3mol H2O、1mol H2充入容积为1L的容器中,发生反应: CO(g) + H2O(g) CO2(g) + H2(g),一定时间后达到平衡时,测得容器中CO2浓度为0.5mol·L-1,则CO的转化率为
CO2(g) + H2(g),一定时间后达到平衡时,测得容器中CO2浓度为0.5mol·L-1,则CO的转化率为_________ ,800℃时该反应的平衡常数为_________ 。
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:

①用离子方程式表示反应器中发生的反应_______________________________________ 。
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是:___________ 。
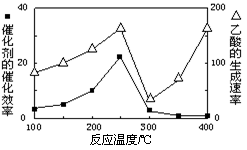
Ⅲ.以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4通过反应CO2(g)+CH4(g) CH3COOH(g)直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率
CH3COOH(g)直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率
如图所示。由下图可以得出的结论是(写两条):_____________________ 、___________________ 。
Ⅰ.处理NOx的一种方法是利用甲烷催化还原NOx。
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2
③CH4(g)+2NO2 (g)= N2(g) + CO2(g)+2H2O(g) △H3=-867kJ·mol-1
则△H2=
Ⅱ.化石燃料的燃烧、含硫金属矿石的冶炼和硫酸的生产过程中产生的SO2是大气中SO2的主要来源。
(1)将煤转化为水煤气是将煤转化为洁净燃料的方法之一,反应为C(s) + H2O(g)
 CO(g) + H2(g)
CO(g) + H2(g)①该反应的化学平衡常数表达式为:K=
②800℃时,将1molCO、3mol H2O、1mol H2充入容积为1L的容器中,发生反应: CO(g) + H2O(g)
 CO2(g) + H2(g),一定时间后达到平衡时,测得容器中CO2浓度为0.5mol·L-1,则CO的转化率为
CO2(g) + H2(g),一定时间后达到平衡时,测得容器中CO2浓度为0.5mol·L-1,则CO的转化率为(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:

①用离子方程式表示反应器中发生的反应
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是:
Ⅲ.以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4通过反应CO2(g)+CH4(g)
 CH3COOH(g)直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率
CH3COOH(g)直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。由下图可以得出的结论是(写两条):

您最近一年使用:0次
四、解答题 添加题型下试题
解答题-工业流程题
|
困难(0.15)
解题方法
11. 金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以钛铁矿(主要成分FeTiO3,含FeO、Al2O3、SiO2等杂质)为主要原料冶炼金属钛,其生产的工艺流程图如下:
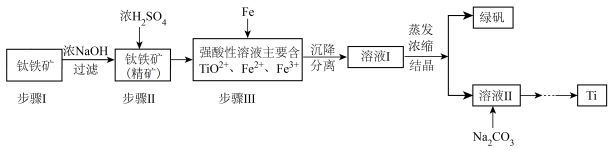
已知:2H2SO4(浓)+ FeTiO3=TiOSO4 + FeSO4 + 2H2O
(1)步骤I中发生反应的离子方程式:____________________ 、_____________________ 。
(2)已知:TiO2+易水解,只能存在于强酸性溶液中。
25 ℃时,难溶电解质溶解度(s)与pH关系如图,TiO(OH)2溶度积Ksp=1×10-29
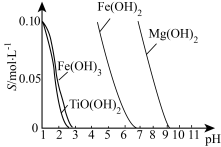
①步骤Ⅲ加入铁屑原因是____________________ 。
②TiO2+水解的离子方程式为______________ 。向溶液II中加入Na2CO3粉末的作用是_______ 。当溶液pH接近_____ 时,TiO(OH)2已沉淀完全。
(3)TiCl4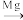 Ti反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于
Ti反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于_______ ℃即可。
(4)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用下图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。写出阳极上所发生的反应式:___________________ 。


已知:2H2SO4(浓)+ FeTiO3=TiOSO4 + FeSO4 + 2H2O
(1)步骤I中发生反应的离子方程式:
(2)已知:TiO2+易水解,只能存在于强酸性溶液中。
25 ℃时,难溶电解质溶解度(s)与pH关系如图,TiO(OH)2溶度积Ksp=1×10-29

①步骤Ⅲ加入铁屑原因是
②TiO2+水解的离子方程式为
(3)TiCl4
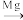 Ti反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于
Ti反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |

您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
解题方法
12. 某小组进行铝热反应实验,装置如图所示。
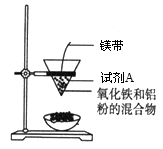
(1)铝热反应原理_________________ (写化学方程式),试剂A为___________ (写化学式)。
(2)对坩埚内的黑色固体物质的组成,小组进行了如下探究
假设I:该黑色物质为铁
假设Ⅱ:该黑色物质为铁与氧化铁的混合物
【设计方案并实验】
【交流评价】
你认为上述结论是否合理?_________ ,理由是_____________________________ 。
(3)取上述实验所得溶液,滴入适量氯水溶液变红色。
①此时涉及的氧化还原反应的离子反应方程式为________________________________ 。
②利用反应体系中存在的平衡:Fe3++3SCN— Fe(SCN)3,小组再将滴入适量氯水的溶液平均分成两份,分别置于两支试管中并编号l、2,进行如下表所示的探究。该实验中,小组主要探究的问题是
Fe(SCN)3,小组再将滴入适量氯水的溶液平均分成两份,分别置于两支试管中并编号l、2,进行如下表所示的探究。该实验中,小组主要探究的问题是____________ ;应重点观察的现象是_____________ ;预计得出的结论是__________ 。

(1)铝热反应原理
(2)对坩埚内的黑色固体物质的组成,小组进行了如下探究
假设I:该黑色物质为铁
假设Ⅱ:该黑色物质为铁与氧化铁的混合物
【设计方案并实验】
| 实 验 步 骤 | 现 象 | 结 论 |
| ①取少量黑色固体于试管中加稀盐酸 | 固体全部溶解,有气泡产生 | 假设I成立,假设Ⅱ不成立 |
| ②滴入几滴0.01mol/LKSCN溶液 | 溶液不变色 |
你认为上述结论是否合理?
(3)取上述实验所得溶液,滴入适量氯水溶液变红色。
①此时涉及的氧化还原反应的离子反应方程式为
②利用反应体系中存在的平衡:Fe3++3SCN—
 Fe(SCN)3,小组再将滴入适量氯水的溶液平均分成两份,分别置于两支试管中并编号l、2,进行如下表所示的探究。该实验中,小组主要探究的问题是
Fe(SCN)3,小组再将滴入适量氯水的溶液平均分成两份,分别置于两支试管中并编号l、2,进行如下表所示的探究。该实验中,小组主要探究的问题是| 实验编号 | 实验步骤 |
| 1 | ①滴加饱和FeCl3溶液4滴,充分振荡 |
| ②滴加几滴NaOH溶液 | |
| 2 | ①滴加4滴1mol/LKSCN溶液 |
| ②滴加几滴NaOH溶液 |
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:有机化学基础、化学与STSE、认识化学科学、化学反应原理、常见无机物及其应用、化学实验基础、物质结构与性质
试卷题型(共 12题)
题型
数量
单选题
6
多选题
2
填空题
2
解答题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 油脂的性质 化学科学对人类文明发展的意义 食品添加剂 | |
| 2 | 0.64 | 离子共存 | |
| 3 | 0.65 | 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 结合物质结构基础知识与NA相关推算 盐类水解规律 | |
| 4 | 0.65 | 水的电离 弱电解质的电离平衡 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 5 | 0.65 | 氯气 化学平衡的移动及其影响因素 仪器使用与实验安全 综合实验设计与评价 | |
| 6 | 0.85 | 金属的电化学腐蚀与防护 金属的化学腐蚀与电化学腐蚀 金属的防护 | |
| 二、多选题 | |||
| 7 | 0.65 | 金属与非金属在周期表中位置及其性质递变的规律 | |
| 8 | 0.65 | 氯气与水的反应 二氧化硫与其他强氧化剂的反应 钠与水反应原理 过氧化钠的强氧化性 | |
| 三、填空题 | |||
| 9 | 0.4 | 有机物的合成与推断 | |
| 10 | 0.4 | 化学反应热的计算 化学平衡 | |
| 四、解答题 | |||
| 11 | 0.15 | 盐类水解在生活、生产中的应用 电解池电极反应式及化学方程式的书写与判断 物质分离、提纯综合应用 物质制备的探究 | 工业流程题 |
| 12 | 0.65 | 铝热反应 铁盐 化学实验探究 物质性质的探究 | 实验探究题 |



