1 . (1)①写出金刚砂的化学式___ ;②写出葡萄糖的结构简式___ 。
(2)CH3ONa是离子化合物,各原子均满足8电子稳定结构(除H以外),CH3ONa的电子式是___ 。
(3)写出向NaHSO3溶液加入少量Na2O2的离子方程式__ 。
(2)CH3ONa是离子化合物,各原子均满足8电子稳定结构(除H以外),CH3ONa的电子式是
(3)写出向NaHSO3溶液加入少量Na2O2的离子方程式
您最近一年使用:0次
名校
2 . 已知钠、氯及其化合物间有如下转化关系,请按要求填空:
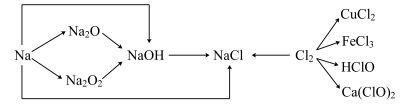
(1)实验室中金属钠通常保存在______ 中,一小块金属钠投入硫酸铜溶液中反应的离子方程式是____________ 。
(2)Na2O2常用于呼吸面具中,有关反应的化学方程式为_____________ ,___________ 。
(3)Na2O2粉末投入到紫色石蕊试液中,观察到的现象是____________ 。
(4)工业上用氯气和石灰乳反应制漂白粉,其化学方程式为__________ 。

(1)实验室中金属钠通常保存在
(2)Na2O2常用于呼吸面具中,有关反应的化学方程式为
(3)Na2O2粉末投入到紫色石蕊试液中,观察到的现象是
(4)工业上用氯气和石灰乳反应制漂白粉,其化学方程式为
您最近一年使用:0次
3 . 现有下列6种物质:①Na2O2 ②CaO ③NO2 ④SO2 ⑤HClO ⑥硫酸铝
回答下列问题:
(1)上述物质中,属于碱性氧化物的是__ ,属于弱电解质的是__ (填标号)。
(2)上述物质中,能与FeCl2溶液发生氧化还原反应且有沉淀产生的是_ 。(填标号)
(3)写出⑥溶于水的电离方程式:__ 。
回答下列问题:
(1)上述物质中,属于碱性氧化物的是
(2)上述物质中,能与FeCl2溶液发生氧化还原反应且有沉淀产生的是
(3)写出⑥溶于水的电离方程式:
您最近一年使用:0次
名校
4 . (1)通常把pH小于_________ 的降雨称为酸雨。
(2)0.6mol H2SO4 的质量是_________ g,含_______ 个分子,该硫酸所含氢元素的质量与_________ g HCl中所含氢元素的质量相同。
(3)“比较”是化学研究物质性质的基本方法之一,请运用比较法解答下列问题:已知在一定条件下,过氧化钠几乎可与所有的常见气态非金属氧化物反应。如:
2Na2O2+2CO2=2Na2CO3+O2, Na2O2+CO=Na2CO3。
①试分别写出Na2O2与SO2、SO3反应的化学方程式。
___________________________ ;__________________ 。
②通过比较可知:在氧化物中,当非金属元素处于______ 价时,其氧化物与过氧化钠反应就有O2生成。
(2)0.6mol H2SO4 的质量是
(3)“比较”是化学研究物质性质的基本方法之一,请运用比较法解答下列问题:已知在一定条件下,过氧化钠几乎可与所有的常见气态非金属氧化物反应。如:
2Na2O2+2CO2=2Na2CO3+O2, Na2O2+CO=Na2CO3。
①试分别写出Na2O2与SO2、SO3反应的化学方程式。
②通过比较可知:在氧化物中,当非金属元素处于
您最近一年使用:0次
2018-04-13更新
|
355次组卷
|
2卷引用:重庆市綦江区2017-2018学年高一上学期期末联考化学试题
5 . (1)标准状况下,44.8L的NH3气体质量为_______ g,其中含____________ 个氮原子,其中含_________ mol 氢原子。
(2)标准状况下,11.2L的H2R气体质量为17g,则H2R的摩尔质量是________ ,等质量的NH3与H2R的物质的量比为_________ ,1.7g氨气与______ mol H2O含有的电子数相等。
(3)过氧化钠几乎可与所有的常见气态非金属氧化物反应。如:
2Na2O2+ 2CO2= 2Na2CO3+ O2; Na2O2+ CO = Na2CO3
试分别写出Na2O2与SO2、SO3反应的化学方程式:
____________________________ 。
__________________________ 。
(4)取黄豆粒大小的一块金属钠,用滤纸擦干其表面的煤油,然后加入到硫酸铜溶液中,观察实验现象并写出相关的化学方程式:
①实验现象__________________________________________________________
②有关的化学方程式是________________________________________________ 。
(2)标准状况下,11.2L的H2R气体质量为17g,则H2R的摩尔质量是
(3)过氧化钠几乎可与所有的常见气态非金属氧化物反应。如:
2Na2O2+ 2CO2= 2Na2CO3+ O2; Na2O2+ CO = Na2CO3
试分别写出Na2O2与SO2、SO3反应的化学方程式:
(4)取黄豆粒大小的一块金属钠,用滤纸擦干其表面的煤油,然后加入到硫酸铜溶液中,观察实验现象并写出相关的化学方程式:
①实验现象
②有关的化学方程式是
您最近一年使用:0次
9-10高一下·河北邯郸·期末
6 . 运用比较方法是化学科学中研究物质性质的基本方法之一,请运用比较法解答下题:过氧化钠几乎可与所有的常见气态非金属氧化物反应。
如:2Na2O2+2CO2=2Na2CO3+O2↑,Na2O2+2CO=Na2CO3。
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式:
_____________________ 。_______________________ 。
(2)通过比较可知,当非金属元素处于______________ 价时,其氧化物与过氧化钠反应有O2生成。
如:2Na2O2+2CO2=2Na2CO3+O2↑,Na2O2+2CO=Na2CO3。
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式:
(2)通过比较可知,当非金属元素处于
您最近一年使用:0次



