解题方法
1 . 某种天然碱样品的化学式可以用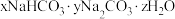 表示(式中x、y、z是最简整数比)。取50g某一浓度的盐酸与3.32g样品充分反应,能生成
表示(式中x、y、z是最简整数比)。取50g某一浓度的盐酸与3.32g样品充分反应,能生成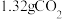 气体。
气体。
(1)若改用1.66g样品与50g这种盐酸反应,能生成
 ?
?(2)另取3.32g样品在300℃下加热至完全分解(已知
 在300℃时不会分解),能产生
在300℃时不会分解),能产生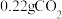 和
和 ,试确定该样品的化学式
,试确定该样品的化学式(3)写出这种天然碱与盐酸完全反应的化学方程式:
 最多,求该盐酸中溶质质量分数
最多,求该盐酸中溶质质量分数
您最近一年使用:0次
23-24高一上·浙江温州·期中
解题方法
2 . 取5.48g Na2CO3和NaHCO3的固体混合物,分成两等份。
(1)将其中一份固体混合物加水溶解配成100mL溶液。当向溶液中加入300mLBa(OH)2溶液时,恰好使生成白色沉淀的量最多,测得反应后溶液的c(OH-)=0.100 mol∙L-1 (混合溶液体积改变忽略不计)。则原混合物中n(Na2CO3):n(NaHCO3)=___________ 。
(2)将另一份固体混合物充分加热。写出加热时发生反应的化学方程式___________ 。充分加热后的固体溶于水配成100mL溶液,则c(Na+)=___________ mol∙L-1。
(1)将其中一份固体混合物加水溶解配成100mL溶液。当向溶液中加入300mLBa(OH)2溶液时,恰好使生成白色沉淀的量最多,测得反应后溶液的c(OH-)=0.100 mol∙L-1 (混合溶液体积改变忽略不计)。则原混合物中n(Na2CO3):n(NaHCO3)=
(2)将另一份固体混合物充分加热。写出加热时发生反应的化学方程式
您最近一年使用:0次
23-24高一上·山东烟台·期中
解题方法
3 . 金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)用空气和 可直接制备
可直接制备 。空气与熔融
。空气与熔融 反应前需依次通过填
反应前需依次通过填_______ 、_______ (填标号)
a.浓硫酸 b.饱和食盐水 c. 溶液 d.
溶液 d. 溶液
溶液
(2)将 和
和 的混合物置于真空密闭容器中加热,充分反应后经检测气体产物为
的混合物置于真空密闭容器中加热,充分反应后经检测气体产物为 和水蒸气,其总质量为33g,冷却至标准状况下的体积为16.8L。则剩余固体的成分为
和水蒸气,其总质量为33g,冷却至标准状况下的体积为16.8L。则剩余固体的成分为_______ ,其物质的量之比为_______ ,原混合物中 的质量为
的质量为_______ 。
(3)为探究 的某些化学性质进行如下实验:向锥形瓶内加入饱和
的某些化学性质进行如下实验:向锥形瓶内加入饱和 溶液,用
溶液,用 传感器测定密闭装置中
传感器测定密闭装置中 分压(
分压( 的分压
的分压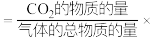 气体总压强),测得
气体总压强),测得 分压与温度的变化关系如图所示。温度在50℃之前,装置中
分压与温度的变化关系如图所示。温度在50℃之前,装置中 分压增大的主要原因是
分压增大的主要原因是_______ ;温度升高到50℃之后,装置中 分压急剧增大的原因是
分压急剧增大的原因是_______ 。

(1)用空气和
 可直接制备
可直接制备 。空气与熔融
。空气与熔融 反应前需依次通过填
反应前需依次通过填a.浓硫酸 b.饱和食盐水 c.
 溶液 d.
溶液 d. 溶液
溶液(2)将
 和
和 的混合物置于真空密闭容器中加热,充分反应后经检测气体产物为
的混合物置于真空密闭容器中加热,充分反应后经检测气体产物为 和水蒸气,其总质量为33g,冷却至标准状况下的体积为16.8L。则剩余固体的成分为
和水蒸气,其总质量为33g,冷却至标准状况下的体积为16.8L。则剩余固体的成分为 的质量为
的质量为(3)为探究
 的某些化学性质进行如下实验:向锥形瓶内加入饱和
的某些化学性质进行如下实验:向锥形瓶内加入饱和 溶液,用
溶液,用 传感器测定密闭装置中
传感器测定密闭装置中 分压(
分压( 的分压
的分压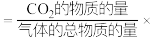 气体总压强),测得
气体总压强),测得 分压与温度的变化关系如图所示。温度在50℃之前,装置中
分压与温度的变化关系如图所示。温度在50℃之前,装置中 分压增大的主要原因是
分压增大的主要原因是 分压急剧增大的原因是
分压急剧增大的原因是
您最近一年使用:0次
23-24高一上·全国·假期作业
解题方法
4 . 已知:①碳酸钠高温下不分解;②碳酸氢钠受热发生分解反应:2NaHCO3 Na2CO3+H2O+CO2↑。充分加热碳酸钠和碳酸氢钠的混合物19 g,完全反应后固体质量减轻了3.1 g,求:
Na2CO3+H2O+CO2↑。充分加热碳酸钠和碳酸氢钠的混合物19 g,完全反应后固体质量减轻了3.1 g,求:
(1)原混合物中碳酸钠的质量是_______ g。
(2)在剩余固体中,加入过量盐酸,反应后放出二氧化碳的体积(标准状况)是_______ L。
 Na2CO3+H2O+CO2↑。充分加热碳酸钠和碳酸氢钠的混合物19 g,完全反应后固体质量减轻了3.1 g,求:
Na2CO3+H2O+CO2↑。充分加热碳酸钠和碳酸氢钠的混合物19 g,完全反应后固体质量减轻了3.1 g,求:(1)原混合物中碳酸钠的质量是
(2)在剩余固体中,加入过量盐酸,反应后放出二氧化碳的体积(标准状况)是
您最近一年使用:0次
名校
5 . 某食品膨松剂作用物质为 ,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
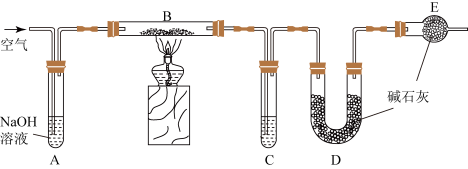
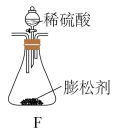
已知:碱石灰是固体氢氧化钠和氧化钙的混合物: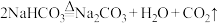 。
。
(1)A装置中 溶液的作用是除去空气中的
溶液的作用是除去空气中的________ ,C装置内所盛试剂是________ ,E装置的作用是________________________ ;
(2)若没有E装置,测定的结果________ (填“偏高”、“偏低”或“无影响”);若没有A装置,B装置左侧用橡皮塞封闭,实验结果将________ (填“偏高”、“偏低”或“无影响”)。
(3)取a克 与
与 混合物进行下列三组实验,其中能测定
混合物进行下列三组实验,其中能测定 质量分数的是
质量分数的是________ (填序号)。
A.充分加热,质量减少b克
B.与足量稀盐酸充分反应,加热、蒸干,灼烧,得b克固体
C.与足量稀硫酸充分反应,逸出气体用氧化钙吸收,增重b克
 ,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。

已知:碱石灰是固体氢氧化钠和氧化钙的混合物:
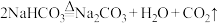 。
。(1)A装置中
 溶液的作用是除去空气中的
溶液的作用是除去空气中的(2)若没有E装置,测定的结果
(3)取a克
 与
与 混合物进行下列三组实验,其中能测定
混合物进行下列三组实验,其中能测定 质量分数的是
质量分数的是A.充分加热,质量减少b克
B.与足量稀盐酸充分反应,加热、蒸干,灼烧,得b克固体
C.与足量稀硫酸充分反应,逸出气体用氧化钙吸收,增重b克
您最近一年使用:0次
22-23高一下·浙江温州·期中
名校
6 . 现有某固体混合物甲,由Na2CO3和NaHCO3混合而成,取2.96g甲溶于水配成25.0mL溶液,往该溶液中加入25.0mLBa(OH)2溶液恰好使生成白色沉淀的量最多,测得反应后溶液中c(OH-)=1.00mol/L(混合溶液体积为50.0mL)。试计算:
(1)原混合物中Na2CO3的物质的量是______ mol。
(2)反应后溶液中Na+的物质的量是______ mol。
(3)上述加入的Ba(OH)2溶液的物质的量浓度为______ 。
(1)原混合物中Na2CO3的物质的量是
(2)反应后溶液中Na+的物质的量是
(3)上述加入的Ba(OH)2溶液的物质的量浓度为
您最近一年使用:0次
21-22高一·浙江杭州·期中
7 . 在80mLNaOH溶液中,通入一定量的CO2得到混合溶液,向所得溶液中逐滴加入盐酸,边滴边振荡,使其充分反应产生CO2的气体的体积与所加盐酸的体积之间关系如图所示,根据图像计算:

(1)混合溶液中溶质是什么?_______ 两者质量比为_______ 。
(2)盐酸滴加到80mL时,溶液中的溶质是什么?_______
(3)原NaOH溶液中NaOH个数与通入CO2气体个数比_______ 。

(1)混合溶液中溶质是什么?
(2)盐酸滴加到80mL时,溶液中的溶质是什么?
(3)原NaOH溶液中NaOH个数与通入CO2气体个数比
您最近一年使用:0次
解题方法
8 . 碳酸钠和碳酸氢钠是用途广泛的化合物。在实验室中,充分加热碳酸钠和碳酸氢钠的混合物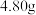 ,完全反应后称得剩余固体质量为
,完全反应后称得剩余固体质量为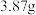 ,求混合物中碳酸氢钠的质量分数
,求混合物中碳酸氢钠的质量分数_______ 。
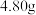 ,完全反应后称得剩余固体质量为
,完全反应后称得剩余固体质量为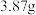 ,求混合物中碳酸氢钠的质量分数
,求混合物中碳酸氢钠的质量分数
您最近一年使用:0次
22-23高一上·全国·课时练习
名校
9 . 向100mLNaOH溶液中缓慢通入一定量的CO2气体,充分反应后,在减压低温下蒸发溶液,得到白色固体。请回答下列问题:
(1)由于CO2通入量不同,所得到的白色固体的组成也不同,试推断有几种可能的组成,并分别列出___________ 。
(2)若通入CO2气体为1.12L(标准状况下),得到5.7g的白色固体。则所用NaOH溶液的物质的量浓度为___________ mol/L。
(1)由于CO2通入量不同,所得到的白色固体的组成也不同,试推断有几种可能的组成,并分别列出
| 1 | 2 | 3 | 4 | |
| 白色固体组成 |
您最近一年使用:0次
21-22高一·全国·假期作业
解题方法
10 . 有碳酸钠、碳酸氢钠的混合物19.0g,把它们加热到质量不再减轻,冷却后称量为15.9g。求:
(1)原混合物中碳酸钠的质量分数___________ 。
(2)将原混合物19.0g完全溶解于蒸馏水水中,配成500mL溶液,则其中钠离子物质的量浓度为___________ 。
(1)原混合物中碳酸钠的质量分数
(2)将原混合物19.0g完全溶解于蒸馏水水中,配成500mL溶液,则其中钠离子物质的量浓度为
您最近一年使用:0次



