名校
解题方法
1 . 某兴趣小组的同学模拟侯德榜制碱法制取纯碱,流程如图:

(1)向饱和NaCl溶液中通入 和氨气时,应先通入
和氨气时,应先通入___________ (填化学式)。操作①的名称为___________ 。
(2)写出反应①的化学方程式:___________ 。
(3)该流程中可循环利用的物质是___________ (填化学式)。
(4)现将 和
和 的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中
的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中 和
和 的物质的量之比为
的物质的量之比为___________ 。
(5)下列选项中哪种方法可以鉴别 溶液和
溶液和 溶液___________。
溶液___________。
(6)下列实验方案中,不能测定出 和
和 的混合物中
的混合物中 质量分数的是_______。
质量分数的是_______。
(7)钠是一种典型的碱金属元素,下列性质的递变规律正确,且能作为碱金属元素金属性递变规律判断依据的是___________(填字母)。

(1)向饱和NaCl溶液中通入
 和氨气时,应先通入
和氨气时,应先通入(2)写出反应①的化学方程式:
(3)该流程中可循环利用的物质是
(4)现将
 和
和 的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中
的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中 和
和 的物质的量之比为
的物质的量之比为(5)下列选项中哪种方法可以鉴别
 溶液和
溶液和 溶液___________。
溶液___________。| A.加入澄清石灰水 | B.加入氢氧化钠溶液 |
| C.加热 | D.逐滴加入稀盐酸 |
(6)下列实验方案中,不能测定出
 和
和 的混合物中
的混合物中 质量分数的是_______。
质量分数的是_______。| A.取ag混合物充分加热,质量减少bg |
| B.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体 |
| C.取ag混合物与足量NaOH溶液充分反应,得到bg溶液 |
| D.取ag混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加bg |
(7)钠是一种典型的碱金属元素,下列性质的递变规律正确,且能作为碱金属元素金属性递变规律判断依据的是___________(填字母)。
| A.Li、Na、K的原子半径和密度都随原子序数的增加而增大 |
B.碱性: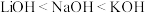 |
C.还原性: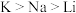 ,故K可以从NaCl溶液中置换出金属钠 ,故K可以从NaCl溶液中置换出金属钠 |
D.熔、沸点: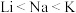 |
您最近一年使用:0次
2023-12-23更新
|
142次组卷
|
3卷引用:湖南省长沙市南雅中学2023-2024学年高一上学期第三次12月月考化学试卷
名校
解题方法
2 . Ⅰ.将 54.8 g Na2CO3和 NaHCO3 的混合物分成等量的两份,一份溶于水后加入足量某浓度的盐酸,收集到气体 V L;另一份直接加热至恒重,生成气体 2.24 L(所有气体体积均在标准状况下测定)。试准确计算出:
(1)原固体混合物中 Na2CO3的物质的量:n(Na2CO3)=__________
(2)V=_____ L。
Ⅱ.研究性学习小组欲用化学方法测量一个不规则容器的体积。把35.1 g NaCl放入500 mL烧杯中,加入150 mL蒸馏水使之完全溶解,将溶解后的溶液全部转移入不规则容器中,用蒸馏水稀释到完全充满容器,从中取出溶液l00 mL,该溶液恰好与2 L 0.100 mol/L AgNO3的溶液完全反应,则不规则容器的体积是_____ mL,不规则容器中NaCl溶液的物质的量浓度是______ mol/L。
(1)原固体混合物中 Na2CO3的物质的量:n(Na2CO3)=
(2)V=
Ⅱ.研究性学习小组欲用化学方法测量一个不规则容器的体积。把35.1 g NaCl放入500 mL烧杯中,加入150 mL蒸馏水使之完全溶解,将溶解后的溶液全部转移入不规则容器中,用蒸馏水稀释到完全充满容器,从中取出溶液l00 mL,该溶液恰好与2 L 0.100 mol/L AgNO3的溶液完全反应,则不规则容器的体积是
您最近一年使用:0次
名校
解题方法
3 . 小苏打样品(主要成分为NaHCO3)中常含有少量氯化钠。某化验员取该样品9.4g加入溶质质量分数为18.25%的稀盐酸20.0g,恰好完全反应,形成无色透明溶液。(NaHCO3+HCl=NaCl+H2O+CO2↑)
求:(1)20.0g18.25%的稀盐酸中溶质HCl的质量。_______
(2)反应后所得溶液中溶质的质量分数。_______
求:(1)20.0g18.25%的稀盐酸中溶质HCl的质量。
(2)反应后所得溶液中溶质的质量分数。
您最近一年使用:0次
解题方法
4 . (1)把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的浓度恰好相等。则已反应的Fe3+和未反应的Fe3+的物质的量之比为_____ 。
(2)把Na2CO3和NaHCO3的混合物29.6g加热到质量不再变化时,得残留固体26.5g;则原混合物中Na2CO3的物质的量为:_____ 。
(2)把Na2CO3和NaHCO3的混合物29.6g加热到质量不再变化时,得残留固体26.5g;则原混合物中Na2CO3的物质的量为:
您最近一年使用:0次
名校
解题方法
5 . 分别取等物质的量浓度的氢氧化钠溶液各100mL,再通入一定量的CO2,随后分别各取20mL溶液,向其中逐滴滴入0.2mol/L的盐酸,在标准状况下产生CO2的体积(y轴)与所加入盐酸的体积(x轴)的关系如图(分A、B两种情况):

(1)在A情况下,溶质是(填化学式)_____________________ ,其物质的量之比为______________
(2)在B情况下,溶质是(填化学式)____________________ 其物质的量之比为______________
(3)原氢氧化钠溶液的物质的量浓度_____________________

(1)在A情况下,溶质是(填化学式)
(2)在B情况下,溶质是(填化学式)
(3)原氢氧化钠溶液的物质的量浓度
您最近一年使用:0次
2018-12-16更新
|
484次组卷
|
5卷引用:湖南省邵阳市邵东县创新实验学校2021届高三上学期第一次月考化学试题
湖南省邵阳市邵东县创新实验学校2021届高三上学期第一次月考化学试题(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第1讲 钠及其氧化物【押题专练】安徽省六安二中2019届高三第一学期第一次诊断性考试理科综合化学试题宁夏固原市隆德县中学2021届高三上学期第二次月考化学试题第三章 金属及其化合物 第12讲 Na2CO3、NaHCO3 碱金属
名校
解题方法
6 . 某化学小组模拟“侯氏制碱法”,以NaCl、NH3、CO2和水等为原料以及下图所示装置制取NaHCO3,反应的化学方程式为NH3+CO2+H2O+NaCl = NaHCO3↓+NH4Cl。然后再将NaHCO3制成Na2CO3。

(1)装置乙的作用是__________ 。为防止污染空气,尾气中含有的_____ 需要进行吸收处理。
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有__________ 。NaHCO3转化为Na2CO3的化学方程式为___________ 。
(3)若在⑵中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1 min的NaHCO3 样品的组成进行了以下探究。
取加热了t1 min的NaHCO3样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中有关离子的物质的量的变化如下图所示。
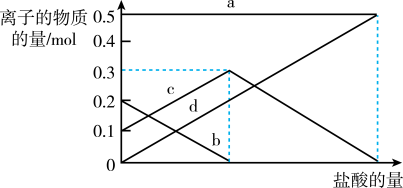
则曲线c对应的溶液中的离子是______ (填离子符号);该样品中NaHCO3和Na2CO3的物质的量之比是_____ 。
(4)若取21.0 g NaHCO3固体,加热了t2 min后,剩余固体的质量为l4.8 g。如果把此剩余固体全部加入到200 mL 2 mol·L-1的盐酸中则充分反应后溶液中H+ 的物质的量浓度为_________ (设溶液体积变化忽略不计)。

(1)装置乙的作用是
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有
(3)若在⑵中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1 min的NaHCO3 样品的组成进行了以下探究。
取加热了t1 min的NaHCO3样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中有关离子的物质的量的变化如下图所示。

则曲线c对应的溶液中的离子是
(4)若取21.0 g NaHCO3固体,加热了t2 min后,剩余固体的质量为l4.8 g。如果把此剩余固体全部加入到200 mL 2 mol·L-1的盐酸中则充分反应后溶液中H+ 的物质的量浓度为
您最近一年使用:0次
11-12高三上·湖南常德·阶段练习
7 . 为了测定K2CO3和NaHCO3混合物的组成,某学生称取了2.22g混合物溶于水配成0.5L溶液,向其中加入0.5 L物质的量浓度为0.06 mol/L的Ba(OH)2溶液,测得沉淀的质量为3.94g。试求:
(1)混合物中K2CO3和NaHCO3的物质的量之比;
(2)取混合后所得溶液体积的1/10,加水配成500mL溶液,所得溶液的pH。
(1)混合物中K2CO3和NaHCO3的物质的量之比;
(2)取混合后所得溶液体积的1/10,加水配成500mL溶液,所得溶液的pH。
您最近一年使用:0次



