名校
解题方法
1 . 下列有关 和
和 性质的说法中正确的是
性质的说法中正确的是
 和
和 性质的说法中正确的是
性质的说法中正确的是A. 和 和 均可用于治疗胃酸过多 均可用于治疗胃酸过多 |
B.可用加热的方法除去 粉末中混有的 粉末中混有的 |
C.等物质的量的 和 和 分别与过量盐酸反应, 分别与过量盐酸反应, 产生 产生 的质量大 的质量大 |
D.向 溶液和 溶液和 溶液中分别加入 溶液中分别加入 溶液,都产生白色沉淀 溶液,都产生白色沉淀 |
您最近一年使用:0次
2022-07-13更新
|
941次组卷
|
5卷引用:作业(九) 碳酸钠和碳酸氢钠 焰色试验
作业(九) 碳酸钠和碳酸氢钠 焰色试验陕西省汉中市6校联考2021-2022学年高一下学期期末考试化学试题(已下线)第二章《 海水中的重要元素----钠和氯》基础过关单元检测-【帮课堂】2022-2023学年高一化学同步精品讲义(人教版2019必修第一册)湖北省襄阳市第一中学2022-2023学年高一上学期10月月考化学试题河北省张家口市宣化第一中学2022-2023学年高一上学期12月月考化学试题
2 . 一定体积的NO2气体依次通过盛有以下物质的容器,饱和NaHCO3溶液→浓H2SO4→固体Na2O2,发生反应的化学方程式是:
(1)___________ ;
(2)___________ ;
(3)___________ ;
(4)___________ 。
(1)
(2)
(3)
(4)
您最近一年使用:0次
3 . 某同学在两个相同的特制容器中分别加入20mL0.4mol·L-1Na2CO3溶液和40mL0.2mol·L-1NaHCO3溶液,再分别用0.4mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如图曲线:
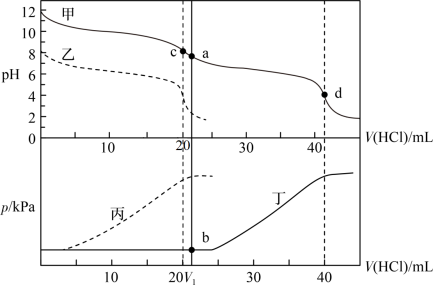
下列说法正确的的是

下列说法正确的的是
| A.图中甲、丁线表示向NaHCO3溶液中滴加盐酸,乙、丙线表示向Na2CO3溶液中滴加盐酸 |
B.当滴加盐酸的体积为V1mL时(a点、b点),所发生的反应用离子方程式表示为:HCO +H+=CO2↑+H2O +H+=CO2↑+H2O |
| C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点 |
D.Na2CO3和NaHCO3溶液中均满足:c(H2CO3)-c(CO )=c(OH-)-c(H+) )=c(OH-)-c(H+) |
您最近一年使用:0次
2022-01-12更新
|
9276次组卷
|
24卷引用:章末检测卷(三) 水溶液中的离子反应与平衡
章末检测卷(三) 水溶液中的离子反应与平衡2022 年1月浙江省普通高校招生选考科目考试化学试题(已下线)卷09 水溶液中的离子平衡-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)回归教材重难点07 图像数据和结果的分析-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)天津市第一中学2021-2022学年高三下学期4月月考化学试题(已下线)2022年浙江1月高考真题变式题(21-25)(已下线)考点28 盐类的水解-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第32练 盐类的水解-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第25讲 盐类水解(练)-2023年高考化学一轮复习讲练测(全国通用)湖南省怀化市沅陵县第一中学2022届高三下学期第四次模拟考试化学试题(已下线)第22讲 水的电离与溶液的pH(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)微专题41 水溶液中的三大守恒和浓度大小比较-备战2023年高考化学一轮复习考点微专题上海市七宝中学2022-2023学年高三上学期9月月考化学试题(已下线)专题06 水溶液中的离子平衡(讲)-2023年高考化学二轮复习讲练测(新高考专用)湖南省株洲南方中学2022-2023学年高二上学期期中考试化学试题(已下线)题型133 酸碱中和滴定实验及误差分析(已下线)专题16 水溶液中的离子平衡(已下线)专题16 水溶液中的离子平衡(已下线)第15练 水溶液中的离子平衡图像分析 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)专题09 水溶液中的离子平衡-2023年高考化学真题题源解密(新高考专用)(已下线)考点28 盐类的水解(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)第三章 水溶液中的离子反应与平衡 第二节 水的电离和溶液的pH 第2课时 酸碱中和滴定(已下线)考点2 水的电离与溶液的pH (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点3 盐类水解(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
名校
解题方法
4 . 一定量CO2通入500mL某浓度的NaOH溶液中得到溶液A,向A溶液中逐滴滴入稀盐酸,加入n(HCl)与生成n(CO2)的关系如图所示。下列有关叙述错误的是
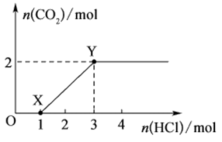

A.X→Y段发生反应的子方程式为HCO +H+=H2O+CO2↑ +H+=H2O+CO2↑ |
| B.原溶液中c(NaOH)=6mol/L |
| C.通入的CO2气体体积为44.8L |
| D.A溶液中含Na2CO3和NaHCO3各1mol |
您最近一年使用:0次
2021-12-17更新
|
649次组卷
|
5卷引用:第二节 金属材料 第2课时 物质的量在化学方程式计算中的应用
解题方法
5 . 为测定某天然碱(xNa2CO3•yNaHCO3•zH2O)的组成.取4.04g天然碱样品,逐滴加入1mol/L的盐酸,产生的CO2体积(标况)与加入盐酸的体积关系如图所示,请回答下列问题:

(1)最终产生的CO2的物质的量为___ mol。
(2)该天然碱的化学式为___ 。

(1)最终产生的CO2的物质的量为
(2)该天然碱的化学式为
您最近一年使用:0次
2021-11-20更新
|
567次组卷
|
2卷引用:第二节 金属材料 第2课时 物质的量在化学方程式计算中的应用
名校
解题方法
6 . 关于Na2CO3和NaHCO3性质的叙述正确的是
| A.在水中的溶解度:Na2CO3<NaHCO3 |
| B.热稳定性:Na2CO3>NaHCO3 |
| C.与酸反应放出气体的速率:Na2CO3>NaHCO3 |
| D.Na2CO3不能转化成NaHCO3,而NaHCO3能转化为Na2CO3 |
您最近一年使用:0次
2021-11-17更新
|
781次组卷
|
21卷引用:2.1.3 碳酸钠和碳酸氢钠-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)
(已下线)2.1.3 碳酸钠和碳酸氢钠-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)2015-2016学年四川省雅安天全中学高一上学期11月月考化学试卷2015-2016学年江苏省海安实验中学高一上学期期中测试化学试卷2015-2016学年安徽省六安一中高一上学期期末化学试卷2015-2016学年甘肃省嘉峪关一中高一上学期期末化学试卷2015-2016学年黑龙江省绥棱一中高二6月月考化学试卷辽宁省辽阳2017-2018学年高一化学期末考试题陕西省西安市第八十三中学2017-2018学年第一学期期末考试高一年级化学试卷安徽省滁州市定远县重点中学2020-2021学年高一10月月考化学试题山西省古县第一中学2020-2021学年高一上学期期中化学试题安徽省六安市舒城育才学校2020-2021学年高一12月月考化学试题吉林省长春市榆树高级中学2020-2021学年高一上学期期末考试化学试题福建省莆田锦江中学2020-2021学年高一上学期期末考试化学试题甘肃省临夏县中学2020-2021学年高一上学期期末考试化学试题河北省石家庄精英中学2018-2019学年高一上学期期末考试化学试题山西省大同市2021-2022学年高一上学期期中化学试题吉林省前郭尔罗斯蒙古族自治县蒙古族中学2021-2022学年高一上学期第二次月考化学试题陕西省西安市西航一中2021-2022学年高一上学期第二次月考化学试题江西省丰城市第九中学2021-2022学年高一上学期期末考试化学试题(已下线)【知识图鉴】单元讲练测必修第一册第二单元02基础练河北省石家庄市西山学校2022-2023学年高一上学期期末考试化学试题
21-22高一·全国·课时练习
解题方法
7 . 某种市售食用碱是纯碱与小苏打的混合物,可大量应用于食品加工,如面条、面包、馒头等,某校化学兴趣小组利用如图所示装置进行实验测定此种食用碱中纯碱的质量分数。

实验步骤:
①检查装置的气密性,称取样品(仅由纯碱与小苏打组成)10g,加到装置B中;
②连接装置,打开弹簧夹,先通一段时间空气后,关闭弹簧夹,打开分液漏斗活塞滴入稀硫酸至不再有气体生成;
③关闭分液漏斗的活塞,打开弹簧夹,继续通入一段时间空气。实验中记录的数据如表所示:
请回答下列问题:
(1)装置a的仪器名称是_____ ,写出稀硫酸与碳酸氢钠反应的化学方程式:_____ 。
(2)实验开始前,先打开弹簧夹,通入一段时间空气,其目的为_____ ,试剂X为_____ (填化学名称)溶液,实验结束后,需要继续通入一段时间的空气,其目的为_____
(3)干燥管II目的作用是_____ ,若缺少干燥管II,会造成测定结果_____ (填“偏大”“不变”或“偏小”)。
(4)有同学认为,表格中三组数据都可以计算该样品中Na2CO3的质量分数,但也有同学认为不能用装置C前后的质量差来计算,其理由是_____ ;通过实验数据计算,食用碱中Na2CO3的质量分数为_____ (保留三位有效数字)。

实验步骤:
①检查装置的气密性,称取样品(仅由纯碱与小苏打组成)10g,加到装置B中;
②连接装置,打开弹簧夹,先通一段时间空气后,关闭弹簧夹,打开分液漏斗活塞滴入稀硫酸至不再有气体生成;
③关闭分液漏斗的活塞,打开弹簧夹,继续通入一段时间空气。实验中记录的数据如表所示:
| 装置B | 装置C | 干燥管1 | |
| 实验前称得的质量/g | 180.0 | 30.0 | 120.4 |
| 实验后称得的质量/g | 174.2 | 31.5 | 124.8 |
(1)装置a的仪器名称是
(2)实验开始前,先打开弹簧夹,通入一段时间空气,其目的为
(3)干燥管II目的作用是
(4)有同学认为,表格中三组数据都可以计算该样品中Na2CO3的质量分数,但也有同学认为不能用装置C前后的质量差来计算,其理由是
您最近一年使用:0次
名校
解题方法
8 . 下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的一组是
①NaHCO3 ②K2CO3 ③A2O3 ④Al(OH)3 ⑤AlCl3
①NaHCO3 ②K2CO3 ③A2O3 ④Al(OH)3 ⑤AlCl3
| A.①② | B.③⑤ | C.③④⑤ | D.①③④ |
您最近一年使用:0次
2021-09-13更新
|
548次组卷
|
5卷引用:5.1.1 元素周期律-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)
(已下线)5.1.1 元素周期律-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)河北省石家庄精英中学2018-2019学年高一上学期期末考试化学试题新疆乌鲁木齐市第八中学2021-2022学年高一上学期第二次月考化学试题辽宁省渤海大学附属高级中学2021-2022学年高一上学期期末质量检测化学试题(已下线)【知识图鉴】单元讲练测必修第一册第三单元03巩固练
21-22高一·全国·课后作业
解题方法
9 . Na2CO3和NaHCO3是重要的化工原料,请回答:
(1)两物质的水溶液分别与足量盐酸混合,反应的化学方程式分别为_______ 、_______ 。
(2)除去Na2CO3固体中少量NaHCO3的方法是_______ ,除去NaHCO3溶液中少量的Na2CO3的方法是_______ 。
(1)两物质的水溶液分别与足量盐酸混合,反应的化学方程式分别为
(2)除去Na2CO3固体中少量NaHCO3的方法是
您最近一年使用:0次
名校
解题方法
10 . 下列物质之间的反应,可以用离子反应方程式2H+ + =H2O+CO2↑表示的是
=H2O+CO2↑表示的是
 =H2O+CO2↑表示的是
=H2O+CO2↑表示的是| A.CaCO3+HCl | B.Na2CO3+HCl |
| C.Na2CO3+CH3COOH | D.NaHCO3+HNO3 |
您最近一年使用:0次
2021-08-21更新
|
318次组卷
|
7卷引用:3.2.2 碳酸钠与碳酸氢钠-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)
(已下线)3.2.2 碳酸钠与碳酸氢钠-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)上海交通大学附属中学2018-2019学年高一第一学期期中考试试卷化学试题福建省师范大学附属中学2019-2020学年高一上学期期末考试化学试题吉林省长春市第七中学2020-2021学年高一上学期第一次月考化学试题(已下线)【浙江新东方】26河北省石家庄市第二十二中学2020-2021学年高一上学期阶段检测化学试题浙江省绍兴鲁迅中学2021-2022学年高一上学期第一次限时训练化学试题



