名校
解题方法
1 . 把18.4g由NaOH和NaHCO3组成的固体混合物在密闭容器中加热到约250摄氏度, 经充分反应后排出气体,冷却后称得固体质量为16.6g,试确定原混合物中NaOH与NaHCO3的物质的量的关系为( )
| A.NaOH<NaHCO3 | B.NaOH>NaHCO3 |
| C.NaOH=NaHCO3 | D.无法确定 |
您最近一年使用:0次
名校
2 . 将一定量的NaHCO3和Na2CO3的混合物放在密闭的容器中加热,充分反应后,测得容器中CO2的体积为1.12 L(标准状况)。反应后的固体与200 mL某浓度的盐酸恰好完全反应生成正盐,同时产生3.36L CO2(标准状况)。则下列说法正确的是
| A.盐酸的物质的量浓度为0.75mol/L | B.盐酸的物质的量浓度为1.5mol/L |
| C.原混合物中NaHCO3的质量为8.4g | D.原混合物中Na2CO3的质量15.9g |
您最近一年使用:0次
名校
3 . 实验室配制460mL0.1mol/LNaOH溶液,回答下列问题:
(1)完成本实验所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、量筒、_____ 、_____ 等。
(2)应用托盘天平称取NaOH固体的质量为_________ 。
(3)下面操作造成所配NaOH溶液浓度偏高的是_________________
A .将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容
B .摇匀后发现液面低于刻度线,滴加蒸馏水至刻度线再摇匀
C .定容时俯视容量瓶的刻度线
D.容量瓶内壁附有水珠而未干燥处理
E. NaOH固体放在烧杯中称量时间过长
(4)取上述体积均为150mL的 A、B 两份NaOH 溶液,分别通入一定量的 CO2 后,再向所得溶液中滴加一定物质的量浓度的盐酸 , 产生 CO2 的体积(标准状况)与所加盐酸的体积关系如图所示。
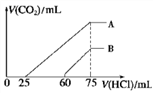
①B 曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为______________ 。
②A 曲线表明,盐酸的浓度为______ mol/L;通入的CO2在标准状况下的体积为______ mL。
(1)完成本实验所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、量筒、
(2)应用托盘天平称取NaOH固体的质量为
(3)下面操作造成所配NaOH溶液浓度偏高的是
A .将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容
B .摇匀后发现液面低于刻度线,滴加蒸馏水至刻度线再摇匀
C .定容时俯视容量瓶的刻度线
D.容量瓶内壁附有水珠而未干燥处理
E. NaOH固体放在烧杯中称量时间过长
(4)取上述体积均为150mL的 A、B 两份NaOH 溶液,分别通入一定量的 CO2 后,再向所得溶液中滴加一定物质的量浓度的盐酸 , 产生 CO2 的体积(标准状况)与所加盐酸的体积关系如图所示。

①B 曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为
②A 曲线表明,盐酸的浓度为
您最近一年使用:0次
名校
4 . Ⅰ.实验室需要配制0.1 mol·L-1NaOH溶液500mL。
(1)根据计算用托盘天平称取的质量为__________ g。在下图所示仪器中,配制上述溶液肯定不需要的是_________ (填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是 _____________ 。

(2)配制时,其正确的操作顺序是(用字母表示,每个操作只用一次)__________ 。
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(3)下面操作造成所配NaOH溶液浓度偏高的是(_____ )
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线.
II.向浓度相等、体积均为100 mL 的 A、B 两份NaOH 溶液中,分别通入一定量的 CO2 后,再向所得溶液中滴加0.1 mol/L 盐酸 , 产生 CO2 的体积(标准状况)与所加盐酸的体积关系如图所示。
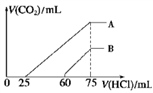
(4)①A 曲线表明,原溶液通入CO2后,所得溶质与盐酸反应产生CO2 的最大体积是_________ mL(标准状况)。
②B 曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为______________ 。
III.某学生用 Na2CO3和 NaHCO3 组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等且不考虑HCl的挥发)
(5)原混合物样品中 n(Na2CO3)∶n(NaHCO3)=____________ , 盐酸的物质的量浓度为________ mol/L ,实验③反应后,至少需继续加入_____ mL的该盐酸溶液才能把混合物全部反应。
(1)根据计算用托盘天平称取的质量为

(2)配制时,其正确的操作顺序是(用字母表示,每个操作只用一次)
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(3)下面操作造成所配NaOH溶液浓度偏高的是(
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线.
II.向浓度相等、体积均为100 mL 的 A、B 两份NaOH 溶液中,分别通入一定量的 CO2 后,再向所得溶液中滴加0.1 mol/L 盐酸 , 产生 CO2 的体积(标准状况)与所加盐酸的体积关系如图所示。

(4)①A 曲线表明,原溶液通入CO2后,所得溶质与盐酸反应产生CO2 的最大体积是
②B 曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为
III.某学生用 Na2CO3和 NaHCO3 组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等且不考虑HCl的挥发)
| 实验序号 | ① | ② | ③ |
| 盐酸体积/mL | 50 | 50 | 50 |
| 固体质量/g | 4.11 | 8.22 | 16.44 |
| 生成气体体积/L(标况) | 1.008 | 2.016 | 2.016 |
(5)原混合物样品中 n(Na2CO3)∶n(NaHCO3)=
您最近一年使用:0次
2017-03-11更新
|
540次组卷
|
2卷引用:2016-2017学年黑龙江省大庆实验中学高一下学期开学考试化学试卷
5 . 在两个烧杯中分别盛有100mL 3.0mol·L-1的盐酸和氢氧化钠溶液,向两个烧杯中分别加入等质量的铝粉,在相同状况下生成的气体的体积比为2∶5,则加入的铝粉的质量为
| A.8.10g | B.5.40g | C.6.75g | D.2.70g |
您最近一年使用:0次
名校
解题方法
6 . 浓度相同的NaOH溶液各100 mL倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量的CO2,充分反应后,再向三份所得溶液中逐滴加入0.2 mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如下图所示。下列判断正确的是(气体体积取标准状况计算)
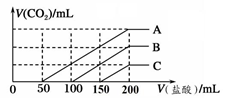

| A.通入CO2后,A烧杯中的溶质成分是Na2CO3 |
| B.B烧杯中通入的CO2体积为448 mL |
| C.原NaOH溶液的浓度为0.2 mol/L |
| D.通入CO2后,C烧杯中溶质成分的物质的量之比为n(NaOH)∶n(Na2CO3)=1∶2 |
您最近一年使用:0次
2016-12-09更新
|
1581次组卷
|
7卷引用:黑龙江省大庆市东风中学2019-2020学年高一上学期期末考试化学试题
黑龙江省大庆市东风中学2019-2020学年高一上学期期末考试化学试题2014-2015湖北省武汉华中师大附高一上学期期末化学试卷福建师大附中2017-2018学年高一上学期期末考试化学试题【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高一上学期第二次月考化学试题山西省太原市山西大学附属中学2019-2020学年高一上学期12月月考化学试题江西省南昌市第二中学2020-2021学年高一上学期第三次月考化学试题(已下线)专题38 CO2与盐或碱溶液反应产物的判断-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
11-12高三·黑龙江大庆·阶段练习
7 . 将15.6g Na2O2和5.4g Al同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入HCl气体6.72L(标准状况),若忽略反应过程中溶液的体积变化,则下列判断正确的是
| A.最终得到7.8g的沉淀 | B.反应过程中得到6.72L(标准状况)的气体 |
| C.最终得到的溶液中c(NaCl)=2.0mo/L | D.最终得到的溶液中c(Na+)=c(Cl—)+c(OH—) |
您最近一年使用:0次
10-11高一上·黑龙江大庆·期中
8 . 向100mLBa(OH)2溶液中加入过量的NaHCO3溶液生成BaCO3沉淀,过滤,将沉淀置于过量盐酸中,在标准状况下收集到4.48L气体。将滤液加水稀释至250mL,取出25mL恰好与20mL盐酸完全反应并收集到1.12L(标准状况下)气体。
(1)Ba(OH)2与过量的NaHCO3溶液反应的化学方程式 。
(2)生成BaCO3沉淀的质量__________g。
(3)100mL Ba(OH)2溶液中溶质Ba(OH)2的物质的量浓度__________mol/L。
(4)最初加入的NaHCO3溶液中含NaHCO3的物质的量__________mol。
(1)Ba(OH)2与过量的NaHCO3溶液反应的化学方程式 。
(2)生成BaCO3沉淀的质量__________g。
(3)100mL Ba(OH)2溶液中溶质Ba(OH)2的物质的量浓度__________mol/L。
(4)最初加入的NaHCO3溶液中含NaHCO3的物质的量__________mol。
您最近一年使用:0次
9-10高一下·广西南宁·期末
9 . 将2.5g碳酸钠、碳酸氢钠和氢氧化钠固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如下图所示:
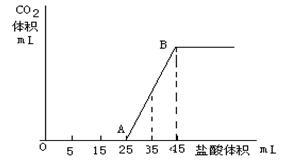
(1)写出OA段所发生反应的离子方程式_________________________
(2)当加入35mL盐酸时,产生二氧化碳的体积为_____ mL(标准状况)
(3)原混合物中Na2CO3的质量分数为_____ 。

(1)写出OA段所发生反应的离子方程式
(2)当加入35mL盐酸时,产生二氧化碳的体积为
(3)原混合物中Na2CO3的质量分数为
您最近一年使用:0次



