解题方法
1 . (1)春秋末期工艺官书《考工记》中记载有“涑帛”的方法,即利用含有碳酸钠的水溶液来洗涤丝帛。请写出碳酸钠水溶液中通入CO2气体的化学方程式___________ 。将54.8g Na2CO3和NaHCO3 的混合物分成等量的两份,一份溶于水后加入足量盐酸,收集到气体V L.另一份直接加热至恒重,生成气体2.24L(所有气体体积均在标准状况下测定),则原固体混合物中Na2CO3的物质的量:n(Na2CO3)=____________ ,气体V=___________ 。
(2)现代社会钠及其化合物用途广泛,回答下列问题:
①过氧化钠是重要的供氧剂,与水反应的离子方程式为_____________ ;
②硫代硫酸钠(Na2S2O3)可用做纸浆漂白时的脱氯剂。Na2S2O3中S的化合价是__________ ,该反应利用了硫代硫酸钠的_________ (填“氧化性”或“还原性“)。
(2)现代社会钠及其化合物用途广泛,回答下列问题:
①过氧化钠是重要的供氧剂,与水反应的离子方程式为
②硫代硫酸钠(Na2S2O3)可用做纸浆漂白时的脱氯剂。Na2S2O3中S的化合价是
您最近一年使用:0次
名校
2 . 由Na2CO3·10H2O与NaHCO3组成的混合物4. 54 g,溶于水配成100 mL溶液,Na+的浓度为0.4 mol·L-1,另取等质量的混合物加强热至质量不变,则剩余固体的质量为
| A.4.24 g | B.3.18 g | C.2.12 g | D.1.06g |
您最近一年使用:0次
2020-11-06更新
|
157次组卷
|
3卷引用:黑龙江省实验中学2020-2021学年高一12月月考化学试题
名校
3 . 现加热5 g碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了0.62 g。则原混合物中碳酸钠的质量分数为
| A.67.6% | B.91.6% | C.66.4% | D.88.2% |
您最近一年使用:0次
14-15高三上·上海虹口·期末
名校
解题方法
4 . 向100mLNaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间的关系如图所示。下列判断正确的是
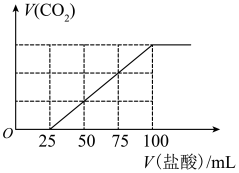

| A.原NaOH溶液的浓度为0.1mol·L-1 |
| B.通入CO2的体积为448mL(标准状况) |
| C.所得溶液的溶质成分的物质的量之比为n(NaOH)∶n(Na2CO3)=1∶3 |
| D.所得溶液的溶质成分的物质的量之比为n(NaHCO3)∶n(Na2CO3)=2∶1 |
您最近一年使用:0次
2020-10-28更新
|
1606次组卷
|
25卷引用:2016届黑龙江省大庆实验中学高三上学期开学考试化学试卷
2016届黑龙江省大庆实验中学高三上学期开学考试化学试卷2016届黑龙江哈尔滨师大附中高三上学期期中考试化学试卷2015-2016学年黑龙江省大庆铁人中学高一上期末化学试卷2017届黑龙江省双鸭山一中高三上学期第一次质检化学试卷【全国百强校】黑龙江省牡丹江市第一高级中学2017-2018学年高二下学期期末考试化学试题【全国百强校】黑龙江省哈尔滨师范大学附属中学2018-2019学年高一下学期开学考试化学试题黑龙江省七台河市勃利县高级中学2021届高三上学期期中考试化学试题(已下线)2014届上海市虹口区高三上学期期末考试(一模)化学试卷(已下线)2015届贵州省贵阳市清华中学高三8月月考理综化学试卷2016届吉林省扶余市第一中学高三上学期第一次月考化学试卷2015-2016学年河南省洛阳市孟津一中高一上期末化学试卷安徽省淮北市第一中学2016-2017学年高二下学期期中考试化学试题2018届高三一轮复习化学:考点17-碳酸钠、碳酸氢钠的性质探究安徽省合肥市第六中学2017-2018学年高一上学期期中考试化学试题江西省上饶市上饶中学2019届高三上学期开学(实验、重点、特长班)检测化学试题吉林省通榆县第一中学2019届高三上学期期中考试化学试题河南省安阳市第三十六中学2018-2019学年高二6月月考化学试题夯基提能2020届高三化学选择题对题专练——化学计算中的常见方法和应用江西省九江市同文中学2019-2020学年度高一下学期期初考试化学试题人教版(2019)高一必修第一册 模块综合测评-B卷高一必修第一册(苏教2019版)专题3 第二单元 金属钠及钠的化合物 课时2 碳酸钠、碳酸氢钠河南省南阳市第一中学校2021届高三第三次月考化学试题黑龙江省哈尔滨市宾县第二中学2021-2022学年高一下学期开学考试化学试题(已下线)专题08 常见无机物及其应用——备战2021年高考化学纠错笔记安徽省芜湖市第一中学2021-2022学年高一上学期第二次月末诊断测试化学试题
名校
5 . 为确定碳酸钠和碳酸氢钠混合样品中碳酸钠的质量分数,可通过加热分解得到的CO2质量进行计算,某同学设计的实验装置示意图如下:
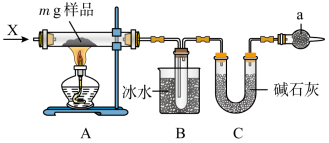
下列说法错误的是

下列说法错误的是
| A.仪器a中试剂的作用是防止外界的水蒸气与二氧化碳进入装置C中 |
| B.装置B中冰水的作用是冷凝反应生成的水 |
| C.样品分解不完全可能使碳酸钠的质量分数偏高 |
| D.产生CO2气体的速率太快,没有被碱石灰完全吸收可能使碳酸钠的质量分数偏低 |
您最近一年使用:0次
2020-08-24更新
|
281次组卷
|
4卷引用:黑龙江省鸡西市第一中学2020-2021学年高一上学期第一次月考化学试题
名校
解题方法
6 . 将标准状况下一定体积的CO2缓缓通入体积为VLNaOH溶液中,充分反应后,在减压低温的条件下蒸发溶液,得到白色固体。
(1)由于CO2通入量不同,所得到的白色固体的组成不同,推断并写出各种可能组成的化学式:(可以不填满,也可以添加序号)
①________ ;②________ ;③________ ;④________ ;⑤________ ;⑥________ 。
(2)按反应的先后顺序,写出各步反应的离子方程式:________ 。
(3)若反应中CO2和NaOH均无剩余,反应后向溶液中加入过量的澄清石灰水生成m1g白色沉淀。
①根据以上数据,能否推理计算出标准状况下CO2的体积?若能,用代数式表示CO2的体积V(CO2)=________ .若不能,理由是________ 。
②根据以上数据,能否推理计算出NaOH溶液的浓度?若能,用代数式表示NaOH溶液的浓度c(NaOH)=________ 。若不能,理由是________ 。
(1)由于CO2通入量不同,所得到的白色固体的组成不同,推断并写出各种可能组成的化学式:(可以不填满,也可以添加序号)
①
(2)按反应的先后顺序,写出各步反应的离子方程式:
(3)若反应中CO2和NaOH均无剩余,反应后向溶液中加入过量的澄清石灰水生成m1g白色沉淀。
①根据以上数据,能否推理计算出标准状况下CO2的体积?若能,用代数式表示CO2的体积V(CO2)=
②根据以上数据,能否推理计算出NaOH溶液的浓度?若能,用代数式表示NaOH溶液的浓度c(NaOH)=
您最近一年使用:0次
名校
7 . 把Na2CO3和NaHCO3的混合物27.4 g加热到质量不再变化时,得残留固体21.2 g.求原混合物中NaHCO3和Na2CO3的质量之比为( )
| A.53:84 | B.84:53 | C.1:1 | D.42:53 |
您最近一年使用:0次
2020-07-09更新
|
197次组卷
|
5卷引用:内蒙古赤峰市宁城县2019-2020学年高一上学期期末考试化学试题
解题方法
8 . 为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1g样品加热,其质量变为w2g,则该样品的纯度(质量分数)是( )
A.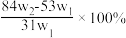 | B.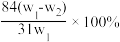 |
C.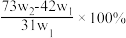 | D.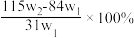 |
您最近一年使用:0次
11-12高三上·湖北襄阳·期中
名校
解题方法
9 . 取等物质的量浓度的 溶液两份A和B,每份10mL,分别向A、B中通入不等量的
溶液两份A和B,每份10mL,分别向A、B中通入不等量的 ,再继续向两溶液中逐滴加入
,再继续向两溶液中逐滴加入 的盐酸,标准状况下产生的
的盐酸,标准状况下产生的 气体体积与所加的盐酸溶液体积之的关系如下图所示,试回答下列问题:
气体体积与所加的盐酸溶液体积之的关系如下图所示,试回答下列问题:
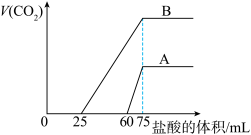
(1)原 溶液的物质的量浓度为
溶液的物质的量浓度为________ 
(2)曲线A表明,原 溶液中通入
溶液中通入 后,所得溶液中的溶质为(写化学式)
后,所得溶液中的溶质为(写化学式)________ ;其物质的量之比为________ ;
(3)曲线B表明,原 溶液中通入
溶液中通入 后,所得溶液加盐酸后产生
后,所得溶液加盐酸后产生 气体体积(标准状况)的最大值为
气体体积(标准状况)的最大值为________ mL。
 溶液两份A和B,每份10mL,分别向A、B中通入不等量的
溶液两份A和B,每份10mL,分别向A、B中通入不等量的 ,再继续向两溶液中逐滴加入
,再继续向两溶液中逐滴加入 的盐酸,标准状况下产生的
的盐酸,标准状况下产生的 气体体积与所加的盐酸溶液体积之的关系如下图所示,试回答下列问题:
气体体积与所加的盐酸溶液体积之的关系如下图所示,试回答下列问题:
(1)原
 溶液的物质的量浓度为
溶液的物质的量浓度为
(2)曲线A表明,原
 溶液中通入
溶液中通入 后,所得溶液中的溶质为(写化学式)
后,所得溶液中的溶质为(写化学式)(3)曲线B表明,原
 溶液中通入
溶液中通入 后,所得溶液加盐酸后产生
后,所得溶液加盐酸后产生 气体体积(标准状况)的最大值为
气体体积(标准状况)的最大值为
您最近一年使用:0次
2020-02-27更新
|
399次组卷
|
10卷引用:黑龙江省齐齐哈尔市第八中学2019届高三9月月考化学试题
黑龙江省齐齐哈尔市第八中学2019届高三9月月考化学试题(已下线)2012届湖北省襄阳市四校高三上学期期中联考化学试卷2016届山东省乳山市第一中学高三上学期10月月考化学试卷2015-2016学年广东省汕头金山中学高一上期末化学试卷2016-2017学年江西省南昌二中高一上第二次考试化学卷湖北省武汉市汉阳一中2018-2019学年高一上学期12月月考化学试题江西省新余市分宜中学2020届高三上学期第一次段考化学试题(已下线)【新东方】2020-44(已下线)专题3.1 金属钠及其化合物 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》天津市耀华中学2021-2022学年高一上学期期中考试化学试题
名校
解题方法
10 . 有Na2CO3和NaHCO3的混合物1.9g,加热灼烧至质量不再减少(反应的化学方程式是:2NaHCO3= Na2CO3+CO2↑+H2O),再与足量盐酸反应生成0.66g气体,试计算原混合物中NaHCO3的质量分数____________ 。
您最近一年使用:0次



