名校
解题方法
1 . 碳酸钠和碳酸氢钠在日常生产生活中有着广泛应用。用如图装置探究二者的稳定性。 和
和 位置互换?
位置互换?_______ (填“能”或“不能”)。能证明 的热稳定性强于
的热稳定性强于 的实验现象是:
的实验现象是:_______
(2)除了热稳定性外,请你再设计一个实验用于鉴别 和
和 :
:_______ 。

 和
和 位置互换?
位置互换? 的热稳定性强于
的热稳定性强于 的实验现象是:
的实验现象是:(2)除了热稳定性外,请你再设计一个实验用于鉴别
 和
和 :
:
您最近一年使用:0次
名校
解题方法
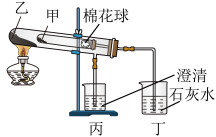
2 . 利用下图进行实验,比较碳酸钠和碳酸氢钠的热稳定性。___________ 。
您最近一年使用:0次
名校
解题方法
3 . 某学习小组研究碳酸钠的性质进行以下实验:
(1)欲检验 中存在钠元素,可使用的方法___________。
中存在钠元素,可使用的方法___________。
(2)欲除去 中少量
中少量 ,可使用的方法___________。
,可使用的方法___________。
(1)欲检验
 中存在钠元素,可使用的方法___________。
中存在钠元素,可使用的方法___________。| A.沉淀法 | B.显色法 | C.焰色反应 | D.气体法 |
 中少量
中少量 ,可使用的方法___________。
,可使用的方法___________。| A.加入过量盐酸 | B.直接加热 | C.加入石灰水 | D.通 过量 过量 |
您最近一年使用:0次
解题方法
4 . 钠元素在自然界中分布很广,储量极为丰富,都以化合态存在,如氯化钠、碳酸钠、硫酸钠等。钠单质和钠的化合物在生产、生活中被广泛应用。请根据钠及其化合物性质按要求完成各题。
(1)钠原子在周期表中的位置为___________ ,钠离子的结构示意图___________ 。
(2)请选择下列物质中合适的物质,按要求填空:
NaOH、 CaCl2 、 SO2 、H2O 、 NH4Cl
只含有离子键的有___________ (填化学式,下同),既含有离子键又含有共价键的有___________ ,只含共价键的有___________ 。
(3)钠的化学性质活泼,暴露在空气中生成___________ 色Na2O,在空气中加热,生成___________ 色的Na2O2,Na2O2可用作呼吸面具、潜水艇的供氧剂,写出Na2O2和CO2反应的化学方程式:___________ 。
(4)钠能在冷水中剧烈反应,该反应的实验现象中描述错误的是____。
(5)下列有关物质的性质描述正确的是____。
(6)Na2CO3和NaHCO3是常见的钠盐,且两者之间可以相互转化,请回答下列问题:
①下列有关碳酸钠和碳酸氢钠的说法正确的是____ 。
A.热稳定性:Na2CO3<NaHCO3
B.溶于水后,碳酸钠溶液呈碱性,碳酸氢钠溶液呈酸性
C.相同条件下,与同种酸反应的剧烈程度:Na2CO3<NaHCO3
D.石碱风化是物理过程
②写出Na2CO3在水溶液中的电离方程式___________ ;
③向Na2CO3溶液中通入CO2可生成NaHCO3,该反应的化学方程式为___________ ;
④加热15.0g碳酸钠和碳酸氢钠的固体混合物至质量不再发生变化,剩余固体的质量为11.9g,则混合物中碳酸氢钠的质量分数为____ 。
A.42% B.44% C.56% D.58%
(1)钠原子在周期表中的位置为
(2)请选择下列物质中合适的物质,按要求填空:
NaOH、 CaCl2 、 SO2 、H2O 、 NH4Cl
只含有离子键的有
(3)钠的化学性质活泼,暴露在空气中生成
(4)钠能在冷水中剧烈反应,该反应的实验现象中描述错误的是____。
| A.钠熔化成银白色小球 | B.钠在水面上迅速游动 |
| C.发出嘶嘶的声响 | D.溶液逐渐变红色 |
| A.钠与氧气反应时的产物主要取决于氧气的用量及纯度 |
| B.钠投入硫酸铜溶液中有气体和蓝色沉淀产生 |
| C.Na2O和Na2O2分别溶于水中,所得的产物相同 |
| D.FeCl3溶液用于铜质印刷线路制作,原因是两者发生置换反应 |
①下列有关碳酸钠和碳酸氢钠的说法正确的是
A.热稳定性:Na2CO3<NaHCO3
B.溶于水后,碳酸钠溶液呈碱性,碳酸氢钠溶液呈酸性
C.相同条件下,与同种酸反应的剧烈程度:Na2CO3<NaHCO3
D.石碱风化是物理过程
②写出Na2CO3在水溶液中的电离方程式
③向Na2CO3溶液中通入CO2可生成NaHCO3,该反应的化学方程式为
④加热15.0g碳酸钠和碳酸氢钠的固体混合物至质量不再发生变化,剩余固体的质量为11.9g,则混合物中碳酸氢钠的质量分数为
A.42% B.44% C.56% D.58%
您最近一年使用:0次
解题方法
5 . Na2CO3可用于纺织、制肥皂、造纸、制玻璃等,NaHCO3可用于制药、焙制糕点等,两者都是白色固体;某实验小组通过以下实验来探究Na2CO3和NaHCO3两种物质的性质。
(1)称取两种固体各 2g,分别放入两个小烧杯中,再各滴加 10mL 蒸馏水,振荡,测量温度变化;待固体充分溶解,并恢复至室温后,向所得溶液中各滴加 2 滴酚酞试液。
①发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得到结论___________ 。
②同学们在两烧杯中还观察到了其它现象。其中,盛放Na2CO3 的烧杯中出现的现象:
I.溶液温度升高;
Ⅱ.滴入酚酞后溶液呈___________ 色。
(2)“套管实验”的实验装置如图所示,请分析实验原理,并回答下列问题:
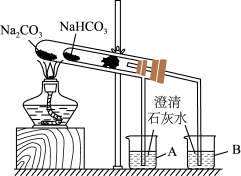
①整个实验过程中,能观察到烧杯 B 中的现象是___________ 。
②写出实验过程中试管中发生反应的化学方程式:___________ 。
③该实验可证明 NaHCO3 的热稳定性___________ (填“强于”“弱于”或“等于”)Na2CO3;证明热稳定性的实验装置中,能否将 NaHCO3、Na2CO3的位置互换?___________ (填“能”或“不能”)。
(3)能用来鉴别 Na2CO3 和 NaHCO3 两种白色固体的实验操作是___________ 。
A.将Na2CO3和NaHCO3 配制成同浓度的溶液,用pH试纸测定pH值并做比较
B.分别加热两种固体样品,看固体是否全部分解挥发
C.分别在这两种物质的溶液中,加入少量NaCl溶液
(1)称取两种固体各 2g,分别放入两个小烧杯中,再各滴加 10mL 蒸馏水,振荡,测量温度变化;待固体充分溶解,并恢复至室温后,向所得溶液中各滴加 2 滴酚酞试液。
①发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得到结论
②同学们在两烧杯中还观察到了其它现象。其中,盛放Na2CO3 的烧杯中出现的现象:
I.溶液温度升高;
Ⅱ.滴入酚酞后溶液呈
(2)“套管实验”的实验装置如图所示,请分析实验原理,并回答下列问题:

①整个实验过程中,能观察到烧杯 B 中的现象是
②写出实验过程中试管中发生反应的化学方程式:
③该实验可证明 NaHCO3 的热稳定性
(3)能用来鉴别 Na2CO3 和 NaHCO3 两种白色固体的实验操作是
A.将Na2CO3和NaHCO3 配制成同浓度的溶液,用pH试纸测定pH值并做比较
B.分别加热两种固体样品,看固体是否全部分解挥发
C.分别在这两种物质的溶液中,加入少量NaCl溶液
您最近一年使用:0次
名校
解题方法
6 .  和
和 是厨房中常见的两种盐。
是厨房中常见的两种盐。
Ⅰ.某学生使用传感器进行如下实验(装置如图1),实验数据如图2:
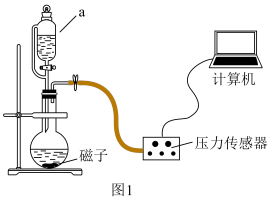

i.向反应器中加入 的
的 溶液,逐滴滴加
溶液,逐滴滴加  的盐酸溶液。
的盐酸溶液。
ii.向反应器中加入 溶液,逐滴滴加一定体积的
溶液,逐滴滴加一定体积的  的盐酸溶液。
的盐酸溶液。
(1)若用无水碳酸钠来配制 的
的 溶液,需在
溶液,需在___________ (填仪器名称)上称取___________  无水碳酸钠。
无水碳酸钠。
(2)配制上述溶液用到的“容量瓶”是___________。
(3)定容操作时:沿着玻璃棒向容量瓶中加水至___________ 处,改用胶头滴管继续滴加水至凹液面最低处与刻度线相平,盖好瓶塞,颠倒摇匀。
(4)实验i中,当碳酸钠溶液与盐酸开始发生反应,压力传感器前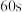 采集的数据如图所示,结合离子方程式用文字表述原因
采集的数据如图所示,结合离子方程式用文字表述原因___________ 。
(5)实验ii为实验i的对照实验,根据图2信息,反应器中加入 溶液,其体积和浓度对应数值最合适的是
溶液,其体积和浓度对应数值最合适的是___________ 。
A.40、0.4 B.20、0.4 C.20、0.2
(6)利用如图3实验比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的为___________ 。

a. B.NaHCO3
B.NaHCO3
Ⅱ.如图4所示,此装置可用来制备 并验证其还原性,填写下列空白:
并验证其还原性,填写下列空白:
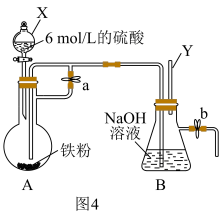
(7)检验反应后圆底烧瓶中是否有 生成所需试剂为
生成所需试剂为___________
(8)实验完毕,B瓶中产生 ,为验证其还原性,打开b处止水夹,充入一段时间空气,此时B瓶中发生的反应为(写化学方程式)
,为验证其还原性,打开b处止水夹,充入一段时间空气,此时B瓶中发生的反应为(写化学方程式)___________ ,现象:___________ 。
 和
和 是厨房中常见的两种盐。
是厨房中常见的两种盐。Ⅰ.某学生使用传感器进行如下实验(装置如图1),实验数据如图2:


i.向反应器中加入
 的
的 溶液,逐滴滴加
溶液,逐滴滴加  的盐酸溶液。
的盐酸溶液。ii.向反应器中加入
 溶液,逐滴滴加一定体积的
溶液,逐滴滴加一定体积的  的盐酸溶液。
的盐酸溶液。(1)若用无水碳酸钠来配制
 的
的 溶液,需在
溶液,需在 无水碳酸钠。
无水碳酸钠。(2)配制上述溶液用到的“容量瓶”是___________。
A. | B. | C.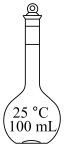 | D.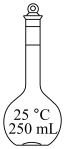 |
(3)定容操作时:沿着玻璃棒向容量瓶中加水至
(4)实验i中,当碳酸钠溶液与盐酸开始发生反应,压力传感器前
 采集的数据如图所示,结合离子方程式用文字表述原因
采集的数据如图所示,结合离子方程式用文字表述原因(5)实验ii为实验i的对照实验,根据图2信息,反应器中加入
 溶液,其体积和浓度对应数值最合适的是
溶液,其体积和浓度对应数值最合适的是A.40、0.4 B.20、0.4 C.20、0.2
(6)利用如图3实验比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的为

a.
 B.NaHCO3
B.NaHCO3Ⅱ.如图4所示,此装置可用来制备
 并验证其还原性,填写下列空白:
并验证其还原性,填写下列空白:
(7)检验反应后圆底烧瓶中是否有
 生成所需试剂为
生成所需试剂为(8)实验完毕,B瓶中产生
 ,为验证其还原性,打开b处止水夹,充入一段时间空气,此时B瓶中发生的反应为(写化学方程式)
,为验证其还原性,打开b处止水夹,充入一段时间空气,此时B瓶中发生的反应为(写化学方程式)
您最近一年使用:0次
7 . 一种碳酸氢钙是一种易溶于水的白色固体,受热易分解。某小组取质量为16.2g的碳酸氢钙样品进行加热分解实验,加热过程中剩余固体的质量随加热时间的变化如图一所示。经查阅资料,他们构建了由碳酸氢钙转化为二氧化碳的不同路径反应转化关系如图二、下列说法不正确的是


| A.图一中,A、C、D三点对应的固体中所含钙元素质量相等 |
| B.图一中,向A点所示固体中加入足量稀盐酸,充分反应生成CO2的质量为2(10.0-x)g |
| C.图二中,等质量的Ca(HCO3)2在反应①、②生成的CO2总量大于反应④生成CO2的量 |
| D.图二中,等质量的Ca(HCO3)2在反应⑤中消耗HCl的量小于在反应④中消耗HCl的量 |
您最近一年使用:0次
名校
解题方法
8 . 某同学为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示。

(1)实验Ⅰ、Ⅱ(盐酸足量且固体质量相同)中能够达到实验目的的是___________ (填装置序号)。
(2)实验Ⅲ、Ⅳ均能鉴别这两种物质,写出所发生的共同反应的化学方程式:___________ 、___________ 。
(3)与实验Ⅲ相比,实验Ⅳ的优点是___________。
(4)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是___________ 。

(1)实验Ⅰ、Ⅱ(盐酸足量且固体质量相同)中能够达到实验目的的是
(2)实验Ⅲ、Ⅳ均能鉴别这两种物质,写出所发生的共同反应的化学方程式:
(3)与实验Ⅲ相比,实验Ⅳ的优点是___________。
| A.Ⅳ比Ⅲ复杂 | B.Ⅳ比Ⅲ安全 |
| C.Ⅳ比Ⅲ操作简便 | D.Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行 |
您最近一年使用:0次
名校
9 . 下列关于碳酸钠和碳酸氢钠的比较中,正确的是
| A.两者在水中的溶解度不同,碳酸氢钠的溶解度大于碳酸钠 |
| B.两者热稳定性不同,碳酸钠的热稳定性小于碳酸氢钠 |
| C.两者与足量盐酸反应,都会产生气泡,现象一定相同 |
| D.两者都能和澄清石灰水反应,现象一样 |
您最近一年使用:0次
2023-06-23更新
|
166次组卷
|
3卷引用:上海市川沙中学2022-2023学年高一下学期期末考试化学试题
10 . 某班级同学设计了以下两组实验。

I.比较Na2CO3和NaHCO3热稳定性。
(1)物质A是_______ (填化学式);能够证明Na2CO3的热稳定性强于NaHCO3的主要证据是 _______ 。
(2)试管B中发生反应的化学方程式是_______ ,烧杯乙中发生反应的离子方程式是_______ 。
II.向浓度相等、体积均为50 mL的A、B两份NaOH溶液中,分别通入一定量的CO2后,再稀释到100 mL。
(3)向NaOH溶液中通入一定量的CO2后,溶液中溶质的主要成分可能是
①_______ ,②_______ ,③_______ ,④_______ 。
(4)在稀释后的溶液中逐滴加入0.10 mol∙L−1的盐酸,产生CO2的体积(标准状况)与所加盐酸的体积关系如下图所示。

①A曲线表明,原溶液通入CO2后,所得溶质与盐酸反应产生CO2的最大体积是_______ mL(标准状况)。
②B曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为_______ ;原NaOH溶液的物质的量浓度为_______ 。

I.比较Na2CO3和NaHCO3热稳定性。
(1)物质A是
(2)试管B中发生反应的化学方程式是
II.向浓度相等、体积均为50 mL的A、B两份NaOH溶液中,分别通入一定量的CO2后,再稀释到100 mL。
(3)向NaOH溶液中通入一定量的CO2后,溶液中溶质的主要成分可能是
①
(4)在稀释后的溶液中逐滴加入0.10 mol∙L−1的盐酸,产生CO2的体积(标准状况)与所加盐酸的体积关系如下图所示。

①A曲线表明,原溶液通入CO2后,所得溶质与盐酸反应产生CO2的最大体积是
②B曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为
您最近一年使用:0次



