解题方法
1 . 为除去括号内的杂质,所选用的试剂或方法正确的是
| A.CO2(HCl):将混合气体通过足量的饱和碳酸钠溶液 |
| B.Na2CO3固体粉末(NaHCO3):加热到固体质量不再减轻为止 |
| C.NaHCO3溶液(Na2CO3):向溶液中加入过量Ca(OH)2溶液,过滤 |
| D.Cl2(HCl):将混合气体通过浓硫酸 |
您最近一年使用:0次
2024-04-07更新
|
69次组卷
|
2卷引用:四川省雅安天立学校腾飞高中2023-2024学年高一上学期11月月考化学试题
解题方法
2 . 下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的有
①Na ②Na2CO3 ③Al2O3 ④NaHSO4 ⑤NaHCO3 ⑥(NH4)2CO3
①Na ②Na2CO3 ③Al2O3 ④NaHSO4 ⑤NaHCO3 ⑥(NH4)2CO3
| A.①③④⑤⑥ | B.①③⑤⑥ | C.②③⑤⑥ | D.①②③⑤ |
您最近一年使用:0次
2024-03-20更新
|
50次组卷
|
2卷引用:四川省雅安市名山区第三中学2023-2024学年高一12月月考化学试题
3 . 类推的思维方法在化学学习与研究中经常使用。下列类推结论中正确的是
| A.BaCl2溶液中通入SO2无沉淀产生,则BaCl2溶液中通入CO2也无沉淀产生 |
B.NaHCO3溶于水电离产生Na+和 ,NaHSO4溶于水电离也产生Na+和 ,NaHSO4溶于水电离也产生Na+和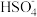 |
| C.Na2O、FeO、Fe2O3等均属于碱性氧化物,金属氧化物都属于碱性氧化物 |
| D.在水中的溶解度Ca(HCO3)2>CaCO3,则溶解度NaHCO3>Na2CO3 |
您最近一年使用:0次
2024-03-12更新
|
78次组卷
|
2卷引用:四川省成都市石室阳安中学2023-2024学年高一上学期12月月考化学试题
名校
4 . 下列说法正确的是
| A.合金因加入其他原子改变了金属原子的层状排列而硬度变大 |
| B.可以通过加热或加入澄清石灰水来鉴别纯碱和小苏打 |
| C.在空气中久置的铝条放入NaOH溶液中,立刻产生大量无色气体,铝条逐渐变细 |
| D.向1L1mol·L-1的醋酸溶液加入1L1mol·L-1氢氧化钠溶液导电能力会减弱 |
您最近一年使用:0次
名校
解题方法
5 . 下列实验过程不能达到实验目的的是
| 编号 | 实验目的 | 实验过程 |
| A | 探究维生素C的还原性 | 向盛有2 mL棕黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 |
| B | 鉴别NaHCO3与Na2CO3 溶液 | 用小试管分别取少量溶液,然后滴加澄清石灰水 |
| C | 比较Fe3+和I2的氧化性强弱 | 向淀粉碘化钾溶液中滴入氯化铁溶液,溶液变蓝色 |
| D | 比较金属镁和铝的活泼性 | 分别向两只盛有等体积等浓度稀硫酸的烧杯中加入打磨过的同样大小的镁片和铝片,比较反应现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 侯德榜发明联合制碱法,其生产流程可简要表示为下图,下列说法错误的是


A.第②步涉及的主要反应为 |
B.流程中若先通入 再通 再通 ,可达到同样效果 ,可达到同样效果 |
| C.实验室进行第③步操作,需要用到的玻璃仪器有漏斗、烧杯、玻璃棒 |
D.用稀盐酸溶液可鉴别 和 和 |
您最近一年使用:0次
名校
解题方法
7 . (Ⅰ)某小组同学依据性质差异,采用比较的方法设计实验鉴别Na2CO3和NaHCO3。
(1)实验Ⅰ中,分别向两支试管中滴加几滴水,A中温度计示数略有降低,B中温度计示数升高。说明固体b与水作用的过程中_______ (填“放出”或“吸收”)热量,可判断固体b为Na2CO3。
(2)实验Ⅱ中,向试管C和D中分别加入5mL水,充分振荡,试管C中固体有剩余,试管D中固体完全溶解。分别向两支试管中滴加2滴酚酞,_______ 试管中红色较浅。
(3)实验Ⅲ中,分别向溶液e和溶液f中逐滴加入稀盐酸,F中开始滴加就可以观察到气泡;E中开始无气泡产生,一段时间后产生气泡。结合离子方程式解释E中开始无气泡产生的原因_______ 。
(Ⅱ)铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。回答下列问题:
(4)可以用电镀法在钢制品上电镀铝,为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应消耗2mol NaOH时,所得气体的物质的量为_______ mol。
(5)如图是从铝土矿(主要成分为Al2O3,还含有少量SiO2、Fe2O3等杂质)中提取Al2O3并生产AlN的工艺流程:

①配料中属于两性氧化物的是_______
②“溶解”时,SiO2与NaOH溶液反应生成的硅酸钠与溶液中偏铝酸钠发生反应:2Na2SiO3+2NaAlO2+2H2O= Na2Al2Si2O8↓+4NaOH ,“赤泥”的主要成分为Na2Al2Si2O8和_______ (写出化学式)。
③ “酸化”时,通入过量CO2与之反应,生成滤液的主要成分是_______ (写化学式)。
实验I | 实验Ⅱ | 实验Ⅲ |
 |  |  |
(2)实验Ⅱ中,向试管C和D中分别加入5mL水,充分振荡,试管C中固体有剩余,试管D中固体完全溶解。分别向两支试管中滴加2滴酚酞,
(3)实验Ⅲ中,分别向溶液e和溶液f中逐滴加入稀盐酸,F中开始滴加就可以观察到气泡;E中开始无气泡产生,一段时间后产生气泡。结合离子方程式解释E中开始无气泡产生的原因
(Ⅱ)铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。回答下列问题:
(4)可以用电镀法在钢制品上电镀铝,为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应消耗2mol NaOH时,所得气体的物质的量为
(5)如图是从铝土矿(主要成分为Al2O3,还含有少量SiO2、Fe2O3等杂质)中提取Al2O3并生产AlN的工艺流程:

①配料中属于两性氧化物的是
②“溶解”时,SiO2与NaOH溶液反应生成的硅酸钠与溶液中偏铝酸钠发生反应:2Na2SiO3+2NaAlO2+2H2O= Na2Al2Si2O8↓+4NaOH ,“赤泥”的主要成分为Na2Al2Si2O8和
③ “酸化”时,通入过量CO2与之反应,生成滤液的主要成分是
您最近一年使用:0次
名校
解题方法
8 . 化学与生产、生活等密切相关,下列说法不正确的是
A. 和 和 的溶液均显碱性,可用作食用碱或工业用碱 的溶液均显碱性,可用作食用碱或工业用碱 |
| B.可以利用放射性同位素释放的射线育种、给金属探伤、诊断和治疗疾病等 |
| C.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁 |
| D.某些喷气式飞机的发动机叶片是由镍钴合金制造,能承受高温 |
您最近一年使用:0次
名校
解题方法
9 . 下列关于Na2CO3、NaHCO3的叙述正确的是
①在酒精灯加热条件下,Na2CO3、NaHCO3固体都能发生分解
②向相同浓度的Na2CO3、NaHCO3溶液中加少量盐酸,产生CO2气体较快的为NaHCO3
③除去NaHCO3固体中的Na2CO3:将固体加热至恒重
④能用澄清石灰水鉴别Na2CO3、NaHCO3溶液
⑤相同温度下,溶解度:Na2CO3<NaHCO3
⑥物质的量相同时,消耗盐酸的量:Na2CO3>NaHCO3
①在酒精灯加热条件下,Na2CO3、NaHCO3固体都能发生分解
②向相同浓度的Na2CO3、NaHCO3溶液中加少量盐酸,产生CO2气体较快的为NaHCO3
③除去NaHCO3固体中的Na2CO3:将固体加热至恒重
④能用澄清石灰水鉴别Na2CO3、NaHCO3溶液
⑤相同温度下,溶解度:Na2CO3<NaHCO3
⑥物质的量相同时,消耗盐酸的量:Na2CO3>NaHCO3
| A.②⑥ | B.①③ | C.④⑤ | D.③⑥ |
您最近一年使用:0次
名校
解题方法
10 . 小组同学进行Na2CO3和NaHCO3性质的探究,实验如下(夹持装置已略去,气密性已检验)。
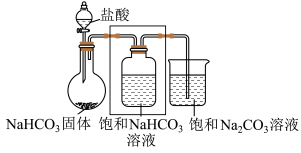
(1)打开分液漏斗活塞放出盐酸,发现流速越来越慢,可能的原因是________ 。
(2) NaHCO3与盐酸反应的化学方程式为________ 。
(3)方框中为洗气装置,请将该装置补充完整________ 。
(4)饱和 NaHCO3溶液的作用是________ 。
(5)反应持续一段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因:________ 。
(6)若向饱和NaHCO3溶液加入少量澄清石灰水的离子方程式_______

(1)打开分液漏斗活塞放出盐酸,发现流速越来越慢,可能的原因是
(2) NaHCO3与盐酸反应的化学方程式为
(3)方框中为洗气装置,请将该装置补充完整
(4)饱和 NaHCO3溶液的作用是
(5)反应持续一段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因:
(6)若向饱和NaHCO3溶液加入少量澄清石灰水的离子方程式
您最近一年使用:0次



