2022高三·全国·专题练习
名校
1 . 为了测定NaCl、Na2CO3•10H2O和NaHCO3的混合物中各组分的含量,某同学设计如图实验:取一定质量的混合物,通过测量反应前后②和③装置质量的变化,测定该混合物中各组分的质量分数。下列说法错误的是
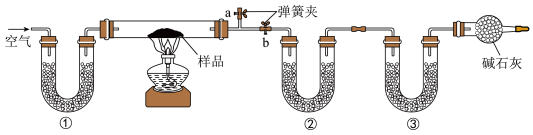

| A.①、②、③中可以依次盛装碱石灰、无水CaCl2、碱石灰 |
| B.若将①装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量偏小 |
| C.硬质玻璃管加热前,应关闭b,打开a,缓缓通入空气,直至a处出来的空气不再使澄清石灰水变浑浊为止 |
| D.实验过程中先停止通入空气,再停止加热 |
您最近一年使用:0次
2022·上海徐汇·一模
解题方法
2 . Na2CO3和NaHCO3是重要的无机化工产品,广泛应用于食品、化工、医药等领域。如图是利用天然碱(主要成分为Na2CO3、NaHCO3和少量NaCl)制备Na2CO3和NaHCO3的工艺流程。
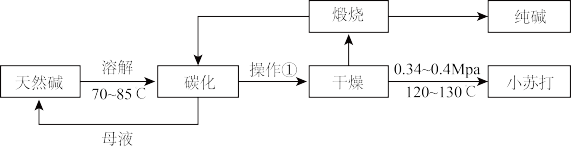
完成下列填空:
(1)操作①为___ 。
(2)碳化装置中反应的离子方程式___ 。
(3)解释选择0.34~0.4MPa干燥的原因___ 。
(4)对比索尔维制碱法,说明利用天然碱制碱的优势___ 。
(5)为了测定产品中小苏打中NaHCO3的含量进行以下实验。
实验步骤:
步骤一:称2.000g小苏打样品,配制小苏打溶液250mL。
步骤二:取20.00mL小苏打溶液置于锥形瓶中,用0.1000mol·L-1盐酸滴定,溶液pH随盐酸体积变化如图所示。

完成下列填空:
①取20.00mL小苏打溶液需要使用的定量仪器名称____ 。
②根据滴定曲线分析,若采用传统滴定法,应选择的指示剂是___ ,此时滴定终点的现象为___ 。
③计算该样品中NaHCO3的质量分数为____ 。

完成下列填空:
(1)操作①为
(2)碳化装置中反应的离子方程式
(3)解释选择0.34~0.4MPa干燥的原因
(4)对比索尔维制碱法,说明利用天然碱制碱的优势
(5)为了测定产品中小苏打中NaHCO3的含量进行以下实验。
实验步骤:
步骤一:称2.000g小苏打样品,配制小苏打溶液250mL。
步骤二:取20.00mL小苏打溶液置于锥形瓶中,用0.1000mol·L-1盐酸滴定,溶液pH随盐酸体积变化如图所示。

完成下列填空:
①取20.00mL小苏打溶液需要使用的定量仪器名称
②根据滴定曲线分析,若采用传统滴定法,应选择的指示剂是
③计算该样品中NaHCO3的质量分数为
您最近一年使用:0次
21-22高一上·广东广州·期末
解题方法
3 . 某同学在实验室对钠的化合物相关样品进行定性、定量研究:
(1)实验1:某纯碱样品只含NaCl杂质,现测定样品中 的含量。称取样品ag,采用如图实验装置进行实验:
的含量。称取样品ag,采用如图实验装置进行实验:

①写出Y形管中稀硫酸与样品发生反应的离子方程式:___________ 。
②试剂X最佳选择是___________ (填标号)。
A.饱和 溶液 B.饱和
溶液 B.饱和 溶液 C.饱和NaCl溶液
溶液 C.饱和NaCl溶液
③读数时,若水准管的液面高于量气管的液面,则样品中 的含量
的含量___________ (填“偏高”、“偏低”或“不影响”)。
④实验结束时,所测得气体体积为V mL。设实验时的气体摩尔体积为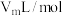 ,则样品中
,则样品中 的质量分数为
的质量分数为___________ 。
(2)实验Ⅱ:碳酸钠和碳酸氢钠稳定性探究。

①上图实验中试剂A和试剂B分别是___________ 、___________ 。
②试管中受热处发生反应的化学方程式:___________ 。
(3)实验Ⅲ:若加热 和
和 的混合物,剩余固体成分会因二者物质的量不同而发生变化。当
的混合物,剩余固体成分会因二者物质的量不同而发生变化。当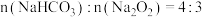 混合后,加热使其充分反应,试管内剩余固体为
混合后,加热使其充分反应,试管内剩余固体为 和NaOH,两者物质的量之比是
和NaOH,两者物质的量之比是___________ 。
(1)实验1:某纯碱样品只含NaCl杂质,现测定样品中
 的含量。称取样品ag,采用如图实验装置进行实验:
的含量。称取样品ag,采用如图实验装置进行实验:
①写出Y形管中稀硫酸与样品发生反应的离子方程式:
②试剂X最佳选择是
A.饱和
 溶液 B.饱和
溶液 B.饱和 溶液 C.饱和NaCl溶液
溶液 C.饱和NaCl溶液③读数时,若水准管的液面高于量气管的液面,则样品中
 的含量
的含量④实验结束时,所测得气体体积为V mL。设实验时的气体摩尔体积为
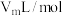 ,则样品中
,则样品中 的质量分数为
的质量分数为(2)实验Ⅱ:碳酸钠和碳酸氢钠稳定性探究。

①上图实验中试剂A和试剂B分别是
②试管中受热处发生反应的化学方程式:
(3)实验Ⅲ:若加热
 和
和 的混合物,剩余固体成分会因二者物质的量不同而发生变化。当
的混合物,剩余固体成分会因二者物质的量不同而发生变化。当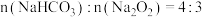 混合后,加热使其充分反应,试管内剩余固体为
混合后,加热使其充分反应,试管内剩余固体为 和NaOH,两者物质的量之比是
和NaOH,两者物质的量之比是
您最近一年使用:0次
2021·河南信阳·模拟预测
名校
4 . 大苏打 、苏打、小苏打被称为“苏氏三兄弟”。它们在生活、生产中有广泛应用。
、苏打、小苏打被称为“苏氏三兄弟”。它们在生活、生产中有广泛应用。
(1)工业上,将 和
和 以
以 的物质的量之比配成溶液。再通入
的物质的量之比配成溶液。再通入 可制取
可制取 ,同时放出
,同时放出 ,写出该反应的化学方程
,写出该反应的化学方程___________ 。 溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的电子式为
溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的电子式为___________ 。
(2) 标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示其原因
标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示其原因___________ 。
(3)下列关于苏打和小苏打的说法正确的是___________ (选填字母序号)。
A.纯碱是一种重要的化工原料,在玻璃、肥皂、造纸等工业中都有重要的应用
B.苏打和小苏打的相互转化属于可逆反应
C.苏打(含氯化钠杂质)可用滴定法测苏打的质量分数,使用石蕊溶液做指示剂更准确
D.牙膏中加入小苏打可以让小苏打颗粒直接摩擦牙齿,帮助清洁牙垢
(4)向 的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入
的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入 的稀盐酸,产生气体体积(标况)如图所示。
的稀盐酸,产生气体体积(标况)如图所示。

请回答下列问题
①通入二氧化碳后形成溶液的溶质成分是___________ (填写化学式)
②滴入 稀盐酸过程中,溶液导电性
稀盐酸过程中,溶液导电性___________ (填“增强”或“减弱”),试解释其原因___________ 。
③原 氢氧化钠溶液的浓度为
氢氧化钠溶液的浓度为___________ 。
 、苏打、小苏打被称为“苏氏三兄弟”。它们在生活、生产中有广泛应用。
、苏打、小苏打被称为“苏氏三兄弟”。它们在生活、生产中有广泛应用。(1)工业上,将
 和
和 以
以 的物质的量之比配成溶液。再通入
的物质的量之比配成溶液。再通入 可制取
可制取 ,同时放出
,同时放出 ,写出该反应的化学方程
,写出该反应的化学方程 溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的电子式为
溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的电子式为(2)
 标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示其原因
标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示其原因(3)下列关于苏打和小苏打的说法正确的是
A.纯碱是一种重要的化工原料,在玻璃、肥皂、造纸等工业中都有重要的应用
B.苏打和小苏打的相互转化属于可逆反应
C.苏打(含氯化钠杂质)可用滴定法测苏打的质量分数,使用石蕊溶液做指示剂更准确
D.牙膏中加入小苏打可以让小苏打颗粒直接摩擦牙齿,帮助清洁牙垢
(4)向
 的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入
的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入 的稀盐酸,产生气体体积(标况)如图所示。
的稀盐酸,产生气体体积(标况)如图所示。
请回答下列问题
①通入二氧化碳后形成溶液的溶质成分是
②滴入
 稀盐酸过程中,溶液导电性
稀盐酸过程中,溶液导电性③原
 氢氧化钠溶液的浓度为
氢氧化钠溶液的浓度为
您最近一年使用:0次
2021-02-09更新
|
1015次组卷
|
7卷引用:专题06 钠及其化合物(限时精练)-2022届高考化学一轮复习热点题型归纳与变式训练
(已下线)专题06 钠及其化合物(限时精练)-2022届高考化学一轮复习热点题型归纳与变式训练(已下线)第07讲 钠及其重要化合物(精练)-2022年高考化学一轮复习讲练测(已下线)第07讲 钠及其重要化合物(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第1讲 钠及其重要化合物河南省信阳市2021届高三上学期第二次教学质量检测化学试题河北省武安市第一中学2021-2022学年高三上学期第五次调研考试化学试题新疆维吾尔自治区伊犁哈萨克自治州新源县第二中学2021-2022学年上学期高三第一次月考化学试题
22-23高一下·湖北·期中
名校
5 . 下列实验方案中,不能测定出 和
和 的混合物中
的混合物中 质量分数的是
质量分数的是
 和
和 的混合物中
的混合物中 质量分数的是
质量分数的是| A.取a g混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加b g |
| B.取a g混合物充分加热,质量减少b g |
| C.取a g混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到b g固体 |
| D.取a g混合物与足量NaOH溶液充分反应,得到b g溶液 |
您最近一年使用:0次
2023-04-16更新
|
174次组卷
|
4卷引用:选择题11-14
20-21高一上·安徽·期中
名校
解题方法
6 . 下列说法正确的是
①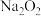 投入到紫色石蕊试液中,溶液先变蓝,后褪色;
投入到紫色石蕊试液中,溶液先变蓝,后褪色;
②质量相等的 与
与 分别与足量相同浓度盐酸完全反应时,产生
分别与足量相同浓度盐酸完全反应时,产生 的物质的量相等;
的物质的量相等;
③取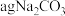 和
和 混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重bg,能测定
混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重bg,能测定 和
和 混合物中
混合物中 质量分数;
质量分数;
④区别 与
与 溶液,可用
溶液,可用 溶液;
溶液;
⑤ 固体可以做干粉灭火剂,金属钠起火可以用它来灭火;
固体可以做干粉灭火剂,金属钠起火可以用它来灭火;
⑥ 粉末中混有
粉末中混有 ,可配制成溶液通入过量的
,可配制成溶液通入过量的 ,再低温结晶提纯得到。
,再低温结晶提纯得到。
①
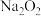 投入到紫色石蕊试液中,溶液先变蓝,后褪色;
投入到紫色石蕊试液中,溶液先变蓝,后褪色;②质量相等的
 与
与 分别与足量相同浓度盐酸完全反应时,产生
分别与足量相同浓度盐酸完全反应时,产生 的物质的量相等;
的物质的量相等;③取
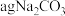 和
和 混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重bg,能测定
混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重bg,能测定 和
和 混合物中
混合物中 质量分数;
质量分数;④区别
 与
与 溶液,可用
溶液,可用 溶液;
溶液;⑤
 固体可以做干粉灭火剂,金属钠起火可以用它来灭火;
固体可以做干粉灭火剂,金属钠起火可以用它来灭火;⑥
 粉末中混有
粉末中混有 ,可配制成溶液通入过量的
,可配制成溶液通入过量的 ,再低温结晶提纯得到。
,再低温结晶提纯得到。| A.②④ | B.②⑤ | C.①⑥ | D.③④ |
您最近一年使用:0次
2022-08-25更新
|
251次组卷
|
15卷引用:衔接点15 钠的化合物-2022年初升高化学无忧衔接?
(已下线)衔接点15 钠的化合物-2022年初升高化学无忧衔接?安徽省蚌埠市第二中学2020-2021学年高一上学期期中考试化学(理科)试题河南省镇平县第一高级中学2020-2021学年高一上学期第二次月考化学试题湖北省沙市中学2021-2022学年高一上学期期中考试化学试题天津市耀华中学2021-2022学年高一上学期期中考试化学试题(已下线)必考点07 钠盐及焰色试验-【对点变式题】2021-2022学年高一化学上学期期中期末必考题精准练(人教版2019)(已下线)第08练 钠及其化合物-2022年【寒假分层作业】高一化学(苏教版2019必修第一册)黑龙江省饶河县高级中学2021-2022学年高一上学期期中考试化学试题江西省宜春市万载中学2021-2022学年高一上学期第三次月考化学试题山东省威海乳山市银滩高级中学2022-2023学年高一10月第二次考试化学试题甘肃省兰州市西北师范大学附属中学2022-2023学年高三上学期期中考试化学试题黑龙江省鹤岗市第一中学2022-2023学年高一上学期11月期中化学试题江西省丰城中学2023-2024学年高三上学期开学考试化学试题新疆维吾尔自治区阿克苏地区第二中学2023-2024学年高三上学期第二次月考化学试题天津市第二十中学2023-2024学年高一上学期期中考试化学试题
21-22高一上·新疆乌鲁木齐·期末
名校
7 . 下列实验方案中,不能测定Na2CO3和NaHCO3混合物中NaHCO3质量分数的方案有
| A.取a克混合物与稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
| B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体 |
| C.取a克混合物与足量Ca(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体 |
| D.取a克混合物充分加热后,固体质量减重bg |
您最近一年使用:0次
20-21高二下·上海·期中
名校
解题方法
8 . 某化学课外活动小组欲制取纯Na2CO3溶液并讨论实验过程中的相关问题。可供选择的试剂有:
A.大理石 B.盐酸 C.氢氧化钠溶液 D.澄清石灰水
三名同学设计的制备纯Na2CO3的溶液的实验方案的反应流程分别如下:
甲:NaOH溶液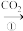 Na2CO3溶液
Na2CO3溶液
乙:NaOH溶液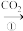 NaHCO3溶液
NaHCO3溶液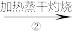 Na2CO3固体
Na2CO3固体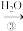 Na2CO3溶液
Na2CO3溶液
丙:NaOH溶液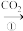 NaHCO3溶液
NaHCO3溶液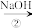 Na2CO3溶液
Na2CO3溶液
(1)请指出甲、乙两方案的主要缺点:
甲方案:___________ ;
乙方案:___________ 。
(2)若采用丙方案制取纯Na2CO3溶液,其实验的关键是:___________ 。
(3)假设反应②所得的Na2CO3固体中混有未分解的NaHCO3,乙同学选择澄清石灰水测定其中NaHCO3的质量分数,乙同学___________ (填“能”或“不能”)达到实验目的:若能,请说明计算所需的数据;若不能,请简要说明理由;___________ 。
(4)已知物质的量浓度均为0.10mol/L的NaHCO3、Na2CO3和Na2S溶液pH如下:
①Na2CO3水溶液呈碱性的原因是___________ (用离子方程式表示)。NaHCO3溶液中滴加酚酞溶液显___________ 色,原因是___________ ;微热溶液颜色变深,可能的原因是___________ (结合离子方程式说明)。
②从表中数据可知,K2CO3溶液中c(CO )
)___________ K2S溶液中的c(S2-)(填“>”“<”或“=”)。
A.大理石 B.盐酸 C.氢氧化钠溶液 D.澄清石灰水
三名同学设计的制备纯Na2CO3的溶液的实验方案的反应流程分别如下:
甲:NaOH溶液
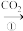 Na2CO3溶液
Na2CO3溶液乙:NaOH溶液
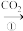 NaHCO3溶液
NaHCO3溶液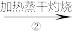 Na2CO3固体
Na2CO3固体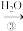 Na2CO3溶液
Na2CO3溶液丙:NaOH溶液
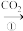 NaHCO3溶液
NaHCO3溶液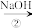 Na2CO3溶液
Na2CO3溶液(1)请指出甲、乙两方案的主要缺点:
甲方案:
乙方案:
(2)若采用丙方案制取纯Na2CO3溶液,其实验的关键是:
(3)假设反应②所得的Na2CO3固体中混有未分解的NaHCO3,乙同学选择澄清石灰水测定其中NaHCO3的质量分数,乙同学
(4)已知物质的量浓度均为0.10mol/L的NaHCO3、Na2CO3和Na2S溶液pH如下:
| 溶液 | NaHCO3 | Na2CO3 | Na2S |
| pH | 8.3 | 11.6 | 12.5 |
①Na2CO3水溶液呈碱性的原因是
②从表中数据可知,K2CO3溶液中c(CO
 )
)
您最近一年使用:0次
19-20高二下·河北邯郸·阶段练习
名校
解题方法
9 . 某校课外小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验。
方案Ⅰ:甲组同学用质量法,按如图所示的实验流程进行实验:

(1)实验时,蒸发结晶操作中,除了铁架台(带铁圈)、酒精灯外,还要用到的仪器是________ 。
(2)有同学认为“加入适量盐酸”不好控制,应改为“加入过量盐酸”,便于操作且不影响测定的准确性,该观点________ (填“正确”或“不正确”),其原因是___________________________ 。
(3)若实验中测得样品质量为46.4g,蒸发后固体质量为40.95g,则碳酸钠的质量分数为________ (保留3位有效数字)。
(4)蒸发结晶过程中若有固体飞溅,测得碳酸钠的质量分数________ (填“偏大”“偏小”或“无影响”)。
方案Ⅱ:乙组同学的主要实验流程如下:

按如图所示装置进行实验:

(5)装置B中的试剂为_______ 在装置C中装碱石灰来吸收净化后的气体,装置D的作用是________________________ 。
(6)有的同学认为为了减小实验误差,在反应前后都通入N2,反应后通入N2的目的是________________________________________________________________________ 。
方案Ⅲ:气体分析法
(7)把一定量样品与足量稀硫酸反应后,用如图装置测量产生CO2气体的体积,B中溶液最好采用________ (填序号)使测量误差较小。

a.饱和碳酸钠溶液 b.饱和碳酸氢钠溶液
c.饱和氢氧化钠溶液 d.饱和硫酸铜溶液
方案Ⅰ:甲组同学用质量法,按如图所示的实验流程进行实验:

(1)实验时,蒸发结晶操作中,除了铁架台(带铁圈)、酒精灯外,还要用到的仪器是
(2)有同学认为“加入适量盐酸”不好控制,应改为“加入过量盐酸”,便于操作且不影响测定的准确性,该观点
(3)若实验中测得样品质量为46.4g,蒸发后固体质量为40.95g,则碳酸钠的质量分数为
(4)蒸发结晶过程中若有固体飞溅,测得碳酸钠的质量分数
方案Ⅱ:乙组同学的主要实验流程如下:

按如图所示装置进行实验:

(5)装置B中的试剂为
(6)有的同学认为为了减小实验误差,在反应前后都通入N2,反应后通入N2的目的是
方案Ⅲ:气体分析法
(7)把一定量样品与足量稀硫酸反应后,用如图装置测量产生CO2气体的体积,B中溶液最好采用

a.饱和碳酸钠溶液 b.饱和碳酸氢钠溶液
c.饱和氢氧化钠溶液 d.饱和硫酸铜溶液
您最近一年使用:0次
解题方法
10 . 某校课外小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验。
方案Ⅰ.甲组同学用沉淀分析法,按如图所示的实验流程进行实验:

 实验时,过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为
实验时,过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为 ______ ;
 检验沉淀B已洗净操作是
检验沉淀B已洗净操作是 ______ ;
 若实验中测得样品质量为mg,沉淀质量为ng,则碳酸钠的质量分数为
若实验中测得样品质量为mg,沉淀质量为ng,则碳酸钠的质量分数为 ______ 。
方案Ⅱ.乙组同学的主要实验 如图
如图

按如图所示装置进行实验:

 该实验中装置B盛放的物质是
该实验中装置B盛放的物质是 ______ ,分液漏斗中 ______  填“能”或“不能”
填“能”或“不能” 用盐酸代替稀硫酸进行实验;
用盐酸代替稀硫酸进行实验;
 在C中装碱石灰来吸收净化后的气体。
在C中装碱石灰来吸收净化后的气体。
 样品中碳酸钠的质量分数越大,则实验中吸收净化后气体的干燥管在充分吸收气体前后的质量差
样品中碳酸钠的质量分数越大,则实验中吸收净化后气体的干燥管在充分吸收气体前后的质量差 ______ (填“越大”、“越小”或“不变化”);
 装置的作用是
装置的作用是 ______ 。
 有的同学认为为了减少实验误差,在反应前后都要通入
有的同学认为为了减少实验误差,在反应前后都要通入 如图
如图 ,反应后通入
,反应后通入 的目的是
的目的是 ______ 。

方案Ⅰ.甲组同学用沉淀分析法,按如图所示的实验流程进行实验:

 实验时,过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为
实验时,过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为  检验沉淀B已洗净操作是
检验沉淀B已洗净操作是  若实验中测得样品质量为mg,沉淀质量为ng,则碳酸钠的质量分数为
若实验中测得样品质量为mg,沉淀质量为ng,则碳酸钠的质量分数为 方案Ⅱ.乙组同学的主要实验
 如图
如图

按如图所示装置进行实验:

 该实验中装置B盛放的物质是
该实验中装置B盛放的物质是  填“能”或“不能”
填“能”或“不能” 用盐酸代替稀硫酸进行实验;
用盐酸代替稀硫酸进行实验; 在C中装碱石灰来吸收净化后的气体。
在C中装碱石灰来吸收净化后的气体。 样品中碳酸钠的质量分数越大,则实验中吸收净化后气体的干燥管在充分吸收气体前后的质量差
样品中碳酸钠的质量分数越大,则实验中吸收净化后气体的干燥管在充分吸收气体前后的质量差  装置的作用是
装置的作用是  有的同学认为为了减少实验误差,在反应前后都要通入
有的同学认为为了减少实验误差,在反应前后都要通入 如图
如图 ,反应后通入
,反应后通入 的目的是
的目的是 
您最近一年使用:0次



