名校
1 . 下列有关物质的性质与用途不具有 对应关系的是
| A.Fe2O3为红棕色粉末,可用于制作红色颜料 |
| B.纳米Fe3O4能与酸反应,可用作铁磁性材料 |
| C.NaHCO3能与酸反应,可用作抗胃酸药 |
| D.Al2O3的熔点很高,可用作耐火材料 |
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题
(1)除去Na2CO3粉末中的NaHCO3固体,用化学方程式表示___________ ;
(2)除去MgO中混有的Al2O3,用离子方程式表示___________ ;
(3)除去FeCl3溶液中的FeCl2,用离子方程式表示___________ 。
(1)除去Na2CO3粉末中的NaHCO3固体,用化学方程式表示
(2)除去MgO中混有的Al2O3,用离子方程式表示
(3)除去FeCl3溶液中的FeCl2,用离子方程式表示
您最近一年使用:0次
名校
解题方法
3 . 金属及其化合物应用广泛,回答下列问题。
(1)运载火箭和载人飞船上使用的铝材属于_______ (填“纯铝”或“铝合金”),生产可用NaOH溶液除去铝材表面的天然氧化膜,反应的离子方程式是_______ 。
(2)服用维生素C可将人体中的Fe3+转化成Fe2+,这说明维生素C具有_______ (填“还原”或“氧化")性。
(3)为消除废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,用离子方程式表示这一处理过程的原理:_______ 、_______ ;处理过程中需定期添加的原料是_______ (填名称)。
(4)在制作印刷电路板的过程中常利用铜与氯化铁溶液的反应,写出反应的离子方程式_______ 。
(5)铁与水蒸气的反应的化学方程式是_______ 。当有16.8g铁粉参加反应时,生成的气体在标准状况下的体积是_______ 。
(6)实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是_______ ,反应化学方程式为_______ 。
(1)运载火箭和载人飞船上使用的铝材属于
(2)服用维生素C可将人体中的Fe3+转化成Fe2+,这说明维生素C具有
(3)为消除废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,用离子方程式表示这一处理过程的原理:
(4)在制作印刷电路板的过程中常利用铜与氯化铁溶液的反应,写出反应的离子方程式
(5)铁与水蒸气的反应的化学方程式是
(6)实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是
您最近一年使用:0次
4 . 下列物质中既能与稀 反应,又能与
反应,又能与 溶液反应的是
溶液反应的是
① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥
 反应,又能与
反应,又能与 溶液反应的是
溶液反应的是①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥
| A.②③④⑥ | B.①②③⑥ | C.①②③⑤⑥ | D.全部 |
您最近一年使用:0次
2023-09-01更新
|
344次组卷
|
2卷引用:天津市耀华中学2023-2024学年高一上学期第二次月考化学试题
解题方法
5 . 下列变化可通过一步化学反应实现的是
| A.Na2O2→Na | B.Al2O3→Al(OH)3 |
| C.CO→Na2CO3 | D.Na2CO3→NaOH |
您最近一年使用:0次
6 . 下列关于除杂试剂的选择不正确 的是(括号中的物质为杂质)
A.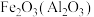 : : 溶液 溶液 | B.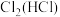 :饱和食盐水 :饱和食盐水 |
C.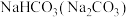 :澄清石灰水 :澄清石灰水 | D.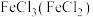 : : |
您最近一年使用:0次
7 . 下列物质属于两性氧化物的是
A. | B. | C. | D. |
您最近一年使用:0次
名校
8 . 混合物的除杂
| 混合物(括号内为杂质) | 除杂试剂 | 发生反应的离子方程式 |
 (Fe3+) (Fe3+) | ① | |
 溶液( 溶液( 溶液) 溶液) | ② | |
 (Cu2+) (Cu2+) | ③ | |
| Fe(Al) | ④ | |
 ( ( ) ) | ⑤ |
您最近一年使用:0次
名校
解题方法
9 . 下列有关物质的性质与用途,不具有对应关系的是
A. 溶液呈酸性,可用于刻蚀铜板 溶液呈酸性,可用于刻蚀铜板 |
B. 的熔点高,常用作耐火、耐高温材料 的熔点高,常用作耐火、耐高温材料 |
C. 与 与 反应,可用于潜艇中的供氧剂 反应,可用于潜艇中的供氧剂 |
D. 具有强氧化性,常作为杀菌、消毒剂 具有强氧化性,常作为杀菌、消毒剂 |
您最近一年使用:0次
2022-12-22更新
|
177次组卷
|
2卷引用:天津市第四十七中学2021-2022学年高一上学期第二次月考化学试题
名校
解题方法
10 . 下列说法正确的是
| A.铝比铁更不容易被腐蚀是因为它的化学性质更不活泼 |
B.可用 溶液除去 溶液除去 粉末中含有的少量 粉末中含有的少量 |
| C.相比纯金属,合金的熔点高、硬度大,在生活生产中应用更广泛 |
D.相同条件下,等质量的铝分别与足量盐酸和 溶液反应,生成 溶液反应,生成 的量不同 的量不同 |
您最近一年使用:0次
2022-12-07更新
|
132次组卷
|
3卷引用:天津市第四十五中学2022-2023学年高一上学期期末考试化学试题



