解题方法
1 . W、X、Y、Z、Q为原子序数依次增大的短周期主族元素,W与Y形成生活中常见的液态化合物,Y的原子序数等于W与X的原子序数之和,Z原子最外层电子数为Y原子最外层电子数的一半,Q的原子半径是第三周期中最小的。下列说法不正确 的是
| A.Y元素与Z元素组成的化合物是两性氧化物 |
| B.由W、X、Y三种元素所组成的化合物可能是酸也可能是碱 |
| C.由Z和Q形成的化合物在熔融状态下能导电 |
| D.简单氢化物的沸点:X<Y |
您最近一年使用:0次
解题方法
2 . 为除去物质中混有的杂质,所选试剂与方法均正确的是
选项 | 物质(杂质) | 除杂试剂 | 方法 |
A |
|
| 点燃 |
B |
|
| 加热 |
C |
| NaOH溶液 | 过滤 |
D | 乙醇( | 无水 | 分液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-06更新
|
765次组卷
|
4卷引用:2024届广东省汕头市高三下学期一模化学试题
2024届广东省汕头市高三下学期一模化学试题(已下线)选择题6-10广东省汕头市2024届高三一化学试题(已下线)压轴题03?物质的制备、检验、分离与提纯(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
名校
解题方法
3 . 工业上以铝土矿(主要成分为 ,含有少量
,含有少量 和
和 )为原料冶炼金属铝,可经过如下过程,其工艺流程示意图如下:
)为原料冶炼金属铝,可经过如下过程,其工艺流程示意图如下:
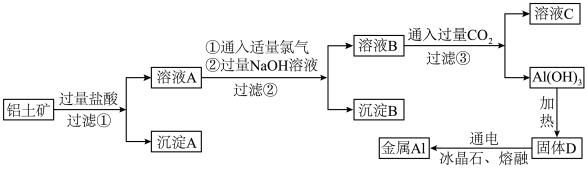
结合上述工艺流程,写出下列反应的化学方程式。
(1)写出得到溶液A,铝土矿中主要成分所发生反应的离子方程式:_______ 。
(2)往溶液 中通入过量
中通入过量 发生反应的离子方程式:
发生反应的离子方程式:_______ 。
(3)沉淀B成分为_______ ,溶液 中
中 与过量
与过量 溶液发生两步反应:
溶液发生两步反应:
①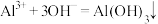
②_______ (写出第2步反应的离子方程)。
(4)溶液C中的溶质主要有_______ 。
(5)已知在熔融状态下, 可被电解(通电分解),得到金属铝,请写出化学方程式:
可被电解(通电分解),得到金属铝,请写出化学方程式:_______ (不用写反应条件)。
 ,含有少量
,含有少量 和
和 )为原料冶炼金属铝,可经过如下过程,其工艺流程示意图如下:
)为原料冶炼金属铝,可经过如下过程,其工艺流程示意图如下:
结合上述工艺流程,写出下列反应的化学方程式。
(1)写出得到溶液A,铝土矿中主要成分所发生反应的离子方程式:
(2)往溶液
 中通入过量
中通入过量 发生反应的离子方程式:
发生反应的离子方程式:(3)沉淀B成分为
 中
中 与过量
与过量 溶液发生两步反应:
溶液发生两步反应:①
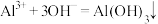
②
(4)溶液C中的溶质主要有
(5)已知在熔融状态下,
 可被电解(通电分解),得到金属铝,请写出化学方程式:
可被电解(通电分解),得到金属铝,请写出化学方程式:
您最近一年使用:0次
4 . 元素周期律是重要的化学学习工具。随着原子序数变化,7种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
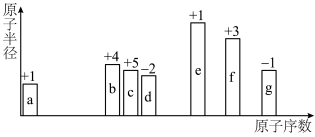
(1)b在元素周期表中的位置是_______ 周期_______ 族。7种元素中金属性最强的是_______ (用元素符号表示,下同),与d处于同一主族的短周期元素是_______ 。
(2)b和c的最高价氧化物的水化物中,酸性较强的是_______ (用化学式表示,下同),c和d的简单氢化物的稳定性较弱的是_______ 。
(3)d和f形成的化合物为_______ (用化学式表示),该化合物在熔融状态下能导电,属于_______ 化合物(填“离子”或“共价”),该化合物与盐酸反应的离子方程式为_______ 。
(4)d、e的单质在加热条件下反应生成的化合物中存在的化学键有_______ 。
(5)用电子式表示由a、c两种元素形成的化合物的形成过程______________ 。

(1)b在元素周期表中的位置是
(2)b和c的最高价氧化物的水化物中,酸性较强的是
(3)d和f形成的化合物为
(4)d、e的单质在加热条件下反应生成的化合物中存在的化学键有
(5)用电子式表示由a、c两种元素形成的化合物的形成过程
您最近一年使用:0次
5 . 世界因多样而精彩,求同是认识物质共性的分类思想,存异是尊重物质客观存在的包容思想。根据下列八种物质回答问题:① Cu ② S ③ CO2 ④ Al2O3 ⑤ Fe2O3 ⑥ Cu2(OH)2CO3 ⑦ 盐酸 ⑧ NaOH
(1)常温常压下,以上八种物质中,能导电的是______ (填写序号)。
(2)我国古代四大发明之一的黑火药是由一硫二硝三木炭的比例混合而成的,爆炸的反应为:S + 2KNO3 + 3C = K2S +______ ↑ + 3CO2↑ 请补齐化学方程式,硝酸钾作为反应的_____ 剂;32g硫粉充分反应,在标况下产生的CO2为______ L。
(3)Al2O3 和Fe2O3同为金属氧化物,均能溶于盐酸中,但Al2O3能溶于NaOH溶液中,而Fe2O3不能,试写出Al2O3与NaOH溶液反应的离子方程式________ 。
(4)铜生锈的产物为碱式碳酸铜Cu2(OH)2CO3,其属于_____ 类(填“酸”、“碱”或“盐”),铜在潮湿的空气中易生锈,试写出铜生锈的化学方程式___________ 。
(1)常温常压下,以上八种物质中,能导电的是
(2)我国古代四大发明之一的黑火药是由一硫二硝三木炭的比例混合而成的,爆炸的反应为:S + 2KNO3 + 3C = K2S +
(3)Al2O3 和Fe2O3同为金属氧化物,均能溶于盐酸中,但Al2O3能溶于NaOH溶液中,而Fe2O3不能,试写出Al2O3与NaOH溶液反应的离子方程式
(4)铜生锈的产物为碱式碳酸铜Cu2(OH)2CO3,其属于
您最近一年使用:0次
解题方法
6 . 下列离子方程式书写正确的是
A.氢氧化钡溶液与硫酸铜溶液混合: |
B.盐酸中加入铝粉: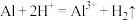 |
C.氧化铝与氢氧化钠溶液混合: |
D.氯化亚铁溶液中滴加氨水: |
您最近一年使用:0次
23-24高三上·贵州·阶段练习
7 . 除去下列括号内的杂质,所选用的试剂或方法正确的是
A.FeSO4 溶液  :加入过量的铁粉,过滤 :加入过量的铁粉,过滤 |
B. :加入过量的NaOH溶液,过滤 :加入过量的NaOH溶液,过滤 |
| C.CO2(CO):通入氧气,点燃 |
D.NaCl溶液(  :加入过量的 BaCl2溶液,过滤 :加入过量的 BaCl2溶液,过滤 |
您最近一年使用:0次
名校
8 . 下列物质中属于碱性氧化物的是
| A.CO2 | B.Na2O2 | C.FeO | D.Al2O3 |
您最近一年使用:0次
2023-10-06更新
|
149次组卷
|
6卷引用:广东省云浮市云安区云安中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
9 . 自然界中的铝元素以化合物的形式存在于各种矿石中、某铝土矿的主要成分是 ,含少量SiO2、Fe2O3等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑其它杂质参与反应):
,含少量SiO2、Fe2O3等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑其它杂质参与反应):
已知: 不溶于水且不与盐酸反应;
不溶于水且不与盐酸反应; 能与NaOH溶液反应,生成可溶性盐。
能与NaOH溶液反应,生成可溶性盐。

请回答下列问题。
(1)步骤①加盐酸前先将铝土矿粉碎的目的是_______ ;所得滤液A中的溶质有_______ 种。
(2)步骤②中所加NaOH溶液须过量的目的是___________ 。
(3)步骤③ 加热分解生成两种氧化物,请写出该反应的化学方程式
加热分解生成两种氧化物,请写出该反应的化学方程式___________ 。
(4)步骤④是通过电解熔融状态的 制备铝。
制备铝。 的熔点是
的熔点是 ,很难达到熔融状态,工业上通过加入冰晶石使其在1000℃左右熔化,请写出这一做法的意义
,很难达到熔融状态,工业上通过加入冰晶石使其在1000℃左右熔化,请写出这一做法的意义___________ 。
氧化亚铜( )可用于电镀工业。干法生产
)可用于电镀工业。干法生产 粉末的主要工艺流程如下:
粉末的主要工艺流程如下:

(5)粉碎机中,发生的变化属于___________ (填“物理变化”或“化学变化”)。
(6) 时,煅烧炉中发生化合反应,该反应的化学方程式为
时,煅烧炉中发生化合反应,该反应的化学方程式为___________ 。
 ,含少量SiO2、Fe2O3等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑其它杂质参与反应):
,含少量SiO2、Fe2O3等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑其它杂质参与反应):已知:
 不溶于水且不与盐酸反应;
不溶于水且不与盐酸反应; 能与NaOH溶液反应,生成可溶性盐。
能与NaOH溶液反应,生成可溶性盐。
请回答下列问题。
(1)步骤①加盐酸前先将铝土矿粉碎的目的是
(2)步骤②中所加NaOH溶液须过量的目的是
(3)步骤③
 加热分解生成两种氧化物,请写出该反应的化学方程式
加热分解生成两种氧化物,请写出该反应的化学方程式(4)步骤④是通过电解熔融状态的
 制备铝。
制备铝。 的熔点是
的熔点是 ,很难达到熔融状态,工业上通过加入冰晶石使其在1000℃左右熔化,请写出这一做法的意义
,很难达到熔融状态,工业上通过加入冰晶石使其在1000℃左右熔化,请写出这一做法的意义氧化亚铜(
 )可用于电镀工业。干法生产
)可用于电镀工业。干法生产 粉末的主要工艺流程如下:
粉末的主要工艺流程如下:
(5)粉碎机中,发生的变化属于
(6)
 时,煅烧炉中发生化合反应,该反应的化学方程式为
时,煅烧炉中发生化合反应,该反应的化学方程式为
您最近一年使用:0次
2023-09-04更新
|
160次组卷
|
2卷引用:广东省揭阳市揭西县2023-2024学年高二上学期1月期末化学试题
10 . 物质的性质决定用途,下列物质的性质与用途无关的是
| 选项 | 物质 | 性质 | 用途 |
| A |  | 熔点高 | 制作耐高温材料 |
| B |  | 极易溶于水 | 作制冷剂 |
| C |  | 燃烧放出的热量多,污染小 | 作燃料 |
| D | 水玻璃 | 硅酸钠不燃不爆 | 作防火剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

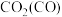

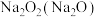
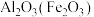
 )
)


