名校
1 . 某废旧金属材料中主要含 、
、 、
、 、
、 、
、 、
、 、
、 和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物:
和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物: 。
。
回答下列问题:
(1)“焙烧”的目的是将金属单质转化为氧化物,并除去_______ 。
(2) 的电子式为
的电子式为_________ ,“碱浸”时发生反应的离子方程式为______ 。
(3)“操作Ⅰ”的名称为________ 。
(4)试剂a为_______ (填化学式),加入试剂a后可能发生的反应为______ (写出其中1个反应的离子方程式即可)。
(5)滤液Ⅱ中可能含有因氧气的作用而产生的少量______ (填离子符号),检验该离子的操作是______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物:
和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物: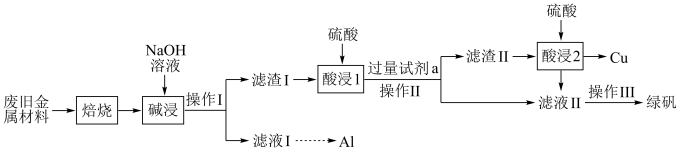
 。
。回答下列问题:
(1)“焙烧”的目的是将金属单质转化为氧化物,并除去
(2)
 的电子式为
的电子式为(3)“操作Ⅰ”的名称为
(4)试剂a为
(5)滤液Ⅱ中可能含有因氧气的作用而产生的少量
您最近一年使用:0次
名校
解题方法
2 . 工业上以铝土矿(主要成分为 ,含有少量
,含有少量 和
和 )为原料冶炼金属铝,可经过如下过程,其工艺流程示意图如下:
)为原料冶炼金属铝,可经过如下过程,其工艺流程示意图如下:
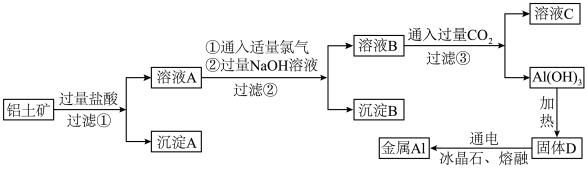
结合上述工艺流程,写出下列反应的化学方程式。
(1)写出得到溶液A,铝土矿中主要成分所发生反应的离子方程式:_______ 。
(2)往溶液 中通入过量
中通入过量 发生反应的离子方程式:
发生反应的离子方程式:_______ 。
(3)沉淀B成分为_______ ,溶液 中
中 与过量
与过量 溶液发生两步反应:
溶液发生两步反应:
①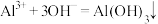
②_______ (写出第2步反应的离子方程)。
(4)溶液C中的溶质主要有_______ 。
(5)已知在熔融状态下, 可被电解(通电分解),得到金属铝,请写出化学方程式:
可被电解(通电分解),得到金属铝,请写出化学方程式:_______ (不用写反应条件)。
 ,含有少量
,含有少量 和
和 )为原料冶炼金属铝,可经过如下过程,其工艺流程示意图如下:
)为原料冶炼金属铝,可经过如下过程,其工艺流程示意图如下:
结合上述工艺流程,写出下列反应的化学方程式。
(1)写出得到溶液A,铝土矿中主要成分所发生反应的离子方程式:
(2)往溶液
 中通入过量
中通入过量 发生反应的离子方程式:
发生反应的离子方程式:(3)沉淀B成分为
 中
中 与过量
与过量 溶液发生两步反应:
溶液发生两步反应:①
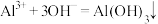
②
(4)溶液C中的溶质主要有
(5)已知在熔融状态下,
 可被电解(通电分解),得到金属铝,请写出化学方程式:
可被电解(通电分解),得到金属铝,请写出化学方程式:
您最近一年使用:0次
3 . 元素周期律是重要的化学学习工具。随着原子序数变化,7种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
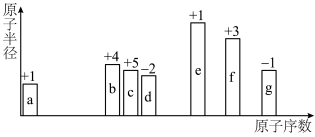
(1)b在元素周期表中的位置是_______ 周期_______ 族。7种元素中金属性最强的是_______ (用元素符号表示,下同),与d处于同一主族的短周期元素是_______ 。
(2)b和c的最高价氧化物的水化物中,酸性较强的是_______ (用化学式表示,下同),c和d的简单氢化物的稳定性较弱的是_______ 。
(3)d和f形成的化合物为_______ (用化学式表示),该化合物在熔融状态下能导电,属于_______ 化合物(填“离子”或“共价”),该化合物与盐酸反应的离子方程式为_______ 。
(4)d、e的单质在加热条件下反应生成的化合物中存在的化学键有_______ 。
(5)用电子式表示由a、c两种元素形成的化合物的形成过程______________ 。

(1)b在元素周期表中的位置是
(2)b和c的最高价氧化物的水化物中,酸性较强的是
(3)d和f形成的化合物为
(4)d、e的单质在加热条件下反应生成的化合物中存在的化学键有
(5)用电子式表示由a、c两种元素形成的化合物的形成过程
您最近一年使用:0次
名校
解题方法
4 . 自然界中的铝元素以化合物的形式存在于各种矿石中、某铝土矿的主要成分是 ,含少量SiO2、Fe2O3等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑其它杂质参与反应):
,含少量SiO2、Fe2O3等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑其它杂质参与反应):
已知: 不溶于水且不与盐酸反应;
不溶于水且不与盐酸反应; 能与NaOH溶液反应,生成可溶性盐。
能与NaOH溶液反应,生成可溶性盐。

请回答下列问题。
(1)步骤①加盐酸前先将铝土矿粉碎的目的是_______ ;所得滤液A中的溶质有_______ 种。
(2)步骤②中所加NaOH溶液须过量的目的是___________ 。
(3)步骤③ 加热分解生成两种氧化物,请写出该反应的化学方程式
加热分解生成两种氧化物,请写出该反应的化学方程式___________ 。
(4)步骤④是通过电解熔融状态的 制备铝。
制备铝。 的熔点是
的熔点是 ,很难达到熔融状态,工业上通过加入冰晶石使其在1000℃左右熔化,请写出这一做法的意义
,很难达到熔融状态,工业上通过加入冰晶石使其在1000℃左右熔化,请写出这一做法的意义___________ 。
氧化亚铜( )可用于电镀工业。干法生产
)可用于电镀工业。干法生产 粉末的主要工艺流程如下:
粉末的主要工艺流程如下:

(5)粉碎机中,发生的变化属于___________ (填“物理变化”或“化学变化”)。
(6) 时,煅烧炉中发生化合反应,该反应的化学方程式为
时,煅烧炉中发生化合反应,该反应的化学方程式为___________ 。
 ,含少量SiO2、Fe2O3等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑其它杂质参与反应):
,含少量SiO2、Fe2O3等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑其它杂质参与反应):已知:
 不溶于水且不与盐酸反应;
不溶于水且不与盐酸反应; 能与NaOH溶液反应,生成可溶性盐。
能与NaOH溶液反应,生成可溶性盐。
请回答下列问题。
(1)步骤①加盐酸前先将铝土矿粉碎的目的是
(2)步骤②中所加NaOH溶液须过量的目的是
(3)步骤③
 加热分解生成两种氧化物,请写出该反应的化学方程式
加热分解生成两种氧化物,请写出该反应的化学方程式(4)步骤④是通过电解熔融状态的
 制备铝。
制备铝。 的熔点是
的熔点是 ,很难达到熔融状态,工业上通过加入冰晶石使其在1000℃左右熔化,请写出这一做法的意义
,很难达到熔融状态,工业上通过加入冰晶石使其在1000℃左右熔化,请写出这一做法的意义氧化亚铜(
 )可用于电镀工业。干法生产
)可用于电镀工业。干法生产 粉末的主要工艺流程如下:
粉末的主要工艺流程如下:
(5)粉碎机中,发生的变化属于
(6)
 时,煅烧炉中发生化合反应,该反应的化学方程式为
时,煅烧炉中发生化合反应,该反应的化学方程式为
您最近一年使用:0次
2023-09-04更新
|
176次组卷
|
2卷引用:广东省揭阳市揭西县2023-2024学年高二上学期1月期末化学试题
名校
解题方法
5 . 石墨在材料领域有重要应用,某初级石墨中含 (7.8%)、
(7.8%)、 (5.1%)和
(5.1%)和 (3.1%)等杂质,提纯与综合利用工艺流程如下:
(3.1%)等杂质,提纯与综合利用工艺流程如下:
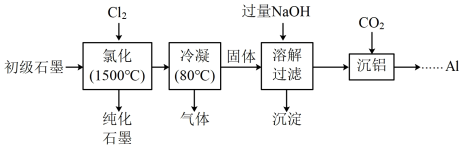
已知:
①氯化后,石墨中氧化物杂质均转变为相应的氯化物;
② 的沸点为57.6℃,金属氯化物的沸点均高于150℃。
的沸点为57.6℃,金属氯化物的沸点均高于150℃。
(1)“氯化”时,先向反应器中通入 一段时间,再加热,主要目的是
一段时间,再加热,主要目的是___________ 。
(2)“冷凝”后,所得“气体”的成分有 和
和___________ (填化学式)。
(3)“溶解过滤”时,加过量NaOH溶液的目的是___________ 。取少量滤液于试管中,___________ (实验操作及现象),证明沉淀已完全。
(4)写出Al的一种用途___________ 。
 (7.8%)、
(7.8%)、 (5.1%)和
(5.1%)和 (3.1%)等杂质,提纯与综合利用工艺流程如下:
(3.1%)等杂质,提纯与综合利用工艺流程如下:
已知:
①氯化后,石墨中氧化物杂质均转变为相应的氯化物;
②
 的沸点为57.6℃,金属氯化物的沸点均高于150℃。
的沸点为57.6℃,金属氯化物的沸点均高于150℃。(1)“氯化”时,先向反应器中通入
 一段时间,再加热,主要目的是
一段时间,再加热,主要目的是(2)“冷凝”后,所得“气体”的成分有
 和
和(3)“溶解过滤”时,加过量NaOH溶液的目的是
(4)写出Al的一种用途
您最近一年使用:0次
名校
6 . 硫酸铝在造纸、水净化、土壤改良中有着广泛的应用,同时还是泡沫灭火器中的试剂。某化工厂利用含铝废料(成分为Al2O3,SiO2及少量FeO∙xFe2O3)制备硫酸铝晶体的工艺流程如下图所示,回答相关问题。

又知生成氢氧化物沉淀的 如下表:
如下表:
(1)料渣I的成分是___________ ,操作 的内容是
的内容是___________ 、洗涤、干燥等。
(2)试剂 最好是
最好是___________ ,a的范围是___________ 。
(3)试剂 是一种液态绿色氧化剂,料液I中反应的离子方程式
是一种液态绿色氧化剂,料液I中反应的离子方程式___________ 。
(4)泡沫灭火器所用试剂为硫酸铝和小苏打,容器构造分为内外两层,内层是塑料容器,外层是钢筒。则硫酸铝溶液应盛放在___________  填“内”或“外”
填“内”或“外” 层容器中,灭火器工作时发生反应的离子方程式为
层容器中,灭火器工作时发生反应的离子方程式为___________ 。

又知生成氢氧化物沉淀的
 如下表:
如下表: |  |  | |
| 开始沉淀时 |  | 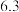 |  |
| 完全沉淀时 | 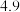 |  |  |
 的内容是
的内容是(2)试剂
 最好是
最好是(3)试剂
 是一种液态绿色氧化剂,料液I中反应的离子方程式
是一种液态绿色氧化剂,料液I中反应的离子方程式(4)泡沫灭火器所用试剂为硫酸铝和小苏打,容器构造分为内外两层,内层是塑料容器,外层是钢筒。则硫酸铝溶液应盛放在
 填“内”或“外”
填“内”或“外” 层容器中,灭火器工作时发生反应的离子方程式为
层容器中,灭火器工作时发生反应的离子方程式为
您最近一年使用:0次
2023-04-02更新
|
165次组卷
|
2卷引用:广东番禺中学2022-2023学年高二下学期科开学考试化学试题
解题方法
7 . 某课外小组研究铝土矿中 Al2O3的含量。查阅资料得知,铝土矿的主要成分是 Al2O3,杂质是 Fe2O3、 SiO2(已知 SiO2性质与 CO2相似,其形成的酸不溶于水)等。从铝土矿中提取 Al2O3 的过程如下:

(1)固体 B 是___________ (填化学式,下同);固体 C 是___________ (填化学式,下同)。
(2)第③步中,生成氢氧化铝的离子方程式是___________ 。
(3)工业上制取 AlCl3常用 Al2O3与碳单质、氯气在高温条件下反应,已知每消耗 0.5molC ,转移 1mol 电子, 则该反应的氧化产物为___________ (填化学式)。

(1)固体 B 是
(2)第③步中,生成氢氧化铝的离子方程式是
(3)工业上制取 AlCl3常用 Al2O3与碳单质、氯气在高温条件下反应,已知每消耗 0.5molC ,转移 1mol 电子, 则该反应的氧化产物为
您最近一年使用:0次
8 . 利用油脂厂废弃的镍( )催化剂(主要含有
)催化剂(主要含有 、
、 、
、 及少量
及少量 、
、 、
、 )制备
)制备 的工艺流程如下:
的工艺流程如下:

回答下列问题:
(1)为加快“碱浸”的速率可采取的措施是___________ (任写一条);“碱浸”中 的作用有:去除油脂、
的作用有:去除油脂、___________ 。
(2)“滤液2”中含金属阳离子,主要有:___________ 。
(3)①“转化”中反应的离子方程式是___________ 。
②“转化”中可替代 的最佳物质是
的最佳物质是___________ (填标号)。
a、 b、
b、 c、
c、
(4)某温度下, 分解得到铁、氧质量比为
分解得到铁、氧质量比为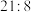 的氧化物,其化学式为
的氧化物,其化学式为___________ 。
 )催化剂(主要含有
)催化剂(主要含有 、
、 、
、 及少量
及少量 、
、 、
、 )制备
)制备 的工艺流程如下:
的工艺流程如下:
回答下列问题:
(1)为加快“碱浸”的速率可采取的措施是
 的作用有:去除油脂、
的作用有:去除油脂、(2)“滤液2”中含金属阳离子,主要有:
(3)①“转化”中反应的离子方程式是
②“转化”中可替代
 的最佳物质是
的最佳物质是a、
 b、
b、 c、
c、
(4)某温度下,
 分解得到铁、氧质量比为
分解得到铁、氧质量比为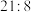 的氧化物,其化学式为
的氧化物,其化学式为
您最近一年使用:0次
解题方法
9 . 2021年,氮化镓等第三代半导体材料的发展被正式列入“十四五规划”,镓及其化合物在国防技术、航空航天技术等领域扮演者着重要的角色,从炼铝废渣(主要含 、
、 、
、 )中提取镓并制备氮化镓的工艺流程如下:
)中提取镓并制备氮化镓的工艺流程如下:

回答下列问题:
(1)Ga与Al同主族,化学性质相似,写出“碱浸”过程中 与NaOH反应的化学方程式:
与NaOH反应的化学方程式:___________ 。
(2)“操作①”所需的玻璃实验仪器有:烧杯、___________ 。
(3)“碱浸”时液固比对镓的浸出率的影响如下图所示,则最适宜的液固比为___________ ,请解释原因___________ 。

(4)“滤渣①”的成分是:___________ ;(写化学式)“流出液”中含有金属元素的离子主要有 、
、___________ 。
(5)“电解”时阴极析出金属镓,请写出阴极反应式___________ ;具体操作时阴极常伴随有气体产生,该气体可能为___________ 。
(6)取a克GaN样品溶于足量的热NaOH溶液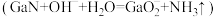 中,用
中,用 溶液将产生的
溶液将产生的 完全吸收,用c mol∙L−1的盐酸滴定,消耗盐酸V mL,则样品的纯度是
完全吸收,用c mol∙L−1的盐酸滴定,消耗盐酸V mL,则样品的纯度是___________ 。(已知: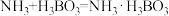 ;
;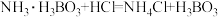 )
)
 、
、 、
、 )中提取镓并制备氮化镓的工艺流程如下:
)中提取镓并制备氮化镓的工艺流程如下:
回答下列问题:
(1)Ga与Al同主族,化学性质相似,写出“碱浸”过程中
 与NaOH反应的化学方程式:
与NaOH反应的化学方程式:(2)“操作①”所需的玻璃实验仪器有:烧杯、
(3)“碱浸”时液固比对镓的浸出率的影响如下图所示,则最适宜的液固比为

(4)“滤渣①”的成分是:
 、
、(5)“电解”时阴极析出金属镓,请写出阴极反应式
(6)取a克GaN样品溶于足量的热NaOH溶液
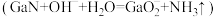 中,用
中,用 溶液将产生的
溶液将产生的 完全吸收,用c mol∙L−1的盐酸滴定,消耗盐酸V mL,则样品的纯度是
完全吸收,用c mol∙L−1的盐酸滴定,消耗盐酸V mL,则样品的纯度是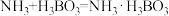 ;
;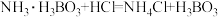 )
)
您最近一年使用:0次
2022-01-09更新
|
401次组卷
|
2卷引用:广东省汕头市2021-2022学年高三上学期期末教学质量监测化学试题
解题方法
10 . 表是元素周期表的一部分,针对表中的①-⑩元素按要求回答下列问题:
(1)在①-⑩元素中,化学性质最不活泼的元素是________ (填元素符号),化学性质最活泼的金属元素是________ (填元素符号)。
(2)在最高价氧化物对应水化物中,酸性最强的化合物的化学式是________ ,碱性最强的化合物的化学式是________ 。
(3)氧化物属于两性氧化物的元素是________ (填元素符号),写出该元素的最高价氧化物与NaOH溶液反应的离子方程式________
(4)比较元素的气态氢化物的稳定性:②_________ ③;最高价氧化物对应水化物的酸性强弱:②_________ ⑥。
(5)⑥的最高价氧化物与烧碱溶液反应的化学方程式为________
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(1)在①-⑩元素中,化学性质最不活泼的元素是
(2)在最高价氧化物对应水化物中,酸性最强的化合物的化学式是
(3)氧化物属于两性氧化物的元素是
(4)比较元素的气态氢化物的稳定性:②
(5)⑥的最高价氧化物与烧碱溶液反应的化学方程式为
您最近一年使用:0次



