石墨在材料领域有重要应用,某初级石墨中含 (7.8%)、
(7.8%)、 (5.1%)和
(5.1%)和 (3.1%)等杂质,提纯与综合利用工艺流程如下:
(3.1%)等杂质,提纯与综合利用工艺流程如下:
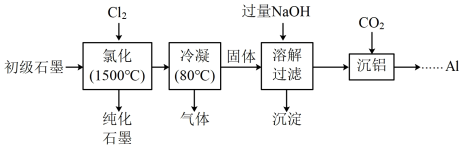
已知:
①氯化后,石墨中氧化物杂质均转变为相应的氯化物;
② 的沸点为57.6℃,金属氯化物的沸点均高于150℃。
的沸点为57.6℃,金属氯化物的沸点均高于150℃。
(1)“氯化”时,先向反应器中通入 一段时间,再加热,主要目的是
一段时间,再加热,主要目的是___________ 。
(2)“冷凝”后,所得“气体”的成分有 和
和___________ (填化学式)。
(3)“溶解过滤”时,加过量NaOH溶液的目的是___________ 。取少量滤液于试管中,___________ (实验操作及现象),证明沉淀已完全。
(4)写出Al的一种用途___________ 。
 (7.8%)、
(7.8%)、 (5.1%)和
(5.1%)和 (3.1%)等杂质,提纯与综合利用工艺流程如下:
(3.1%)等杂质,提纯与综合利用工艺流程如下:
已知:
①氯化后,石墨中氧化物杂质均转变为相应的氯化物;
②
 的沸点为57.6℃,金属氯化物的沸点均高于150℃。
的沸点为57.6℃,金属氯化物的沸点均高于150℃。(1)“氯化”时,先向反应器中通入
 一段时间,再加热,主要目的是
一段时间,再加热,主要目的是(2)“冷凝”后,所得“气体”的成分有
 和
和(3)“溶解过滤”时,加过量NaOH溶液的目的是
(4)写出Al的一种用途
更新时间:2023-05-08 21:08:57
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】工业上以铝土矿(主要成分为 ,含有少量
,含有少量 和
和 )为原料冶炼金属铝,可经过如下过程,其工艺流程示意图如下:
)为原料冶炼金属铝,可经过如下过程,其工艺流程示意图如下:
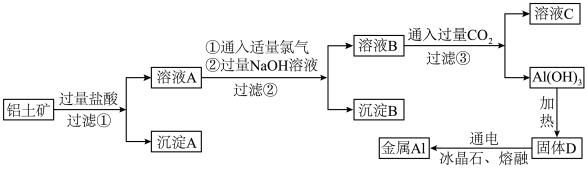
结合上述工艺流程,写出下列反应的化学方程式。
(1)写出得到溶液A,铝土矿中主要成分所发生反应的离子方程式:_______ 。
(2)往溶液 中通入过量
中通入过量 发生反应的离子方程式:
发生反应的离子方程式:_______ 。
(3)沉淀B成分为_______ ,溶液 中
中 与过量
与过量 溶液发生两步反应:
溶液发生两步反应:
①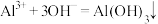
②_______ (写出第2步反应的离子方程)。
(4)溶液C中的溶质主要有_______ 。
(5)已知在熔融状态下, 可被电解(通电分解),得到金属铝,请写出化学方程式:
可被电解(通电分解),得到金属铝,请写出化学方程式:_______ (不用写反应条件)。
 ,含有少量
,含有少量 和
和 )为原料冶炼金属铝,可经过如下过程,其工艺流程示意图如下:
)为原料冶炼金属铝,可经过如下过程,其工艺流程示意图如下:
结合上述工艺流程,写出下列反应的化学方程式。
(1)写出得到溶液A,铝土矿中主要成分所发生反应的离子方程式:
(2)往溶液
 中通入过量
中通入过量 发生反应的离子方程式:
发生反应的离子方程式:(3)沉淀B成分为
 中
中 与过量
与过量 溶液发生两步反应:
溶液发生两步反应:①
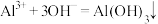
②
(4)溶液C中的溶质主要有
(5)已知在熔融状态下,
 可被电解(通电分解),得到金属铝,请写出化学方程式:
可被电解(通电分解),得到金属铝,请写出化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料.工业上提取氧化铝的工艺流程如下:
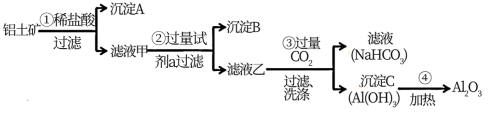
(1)沉淀A、B的成分分别是_______ 、_______ ;
(2)步骤②中的试剂a是_______ ;
(3)试写出步骤③中发生反应的离子方式_______ ;
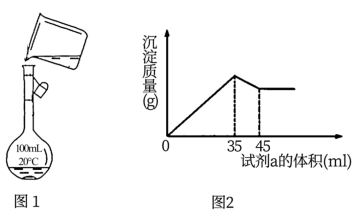
(4)在实验室模拟上述实验过程中,需要用到一定浓度的盐酸溶液.在配制250mL该盐酸溶液时,某同学转移溶液的操作如图1所示,图中的主要错误是:①_______ ;②_______ 。
(5)准确称取6g铝土矿样品,加入100mL盐酸溶液,充分反应后向滤液中加入10mol•L﹣1试剂a的溶液,产生沉淀的质量与加入试剂a的体积关系如图2所示,则所用盐酸溶液的物质的量浓度为_______ ,样品中Al2O3的百分含量为_______ 。

(1)沉淀A、B的成分分别是
(2)步骤②中的试剂a是
(3)试写出步骤③中发生反应的离子方式
(4)在实验室模拟上述实验过程中,需要用到一定浓度的盐酸溶液.在配制250mL该盐酸溶液时,某同学转移溶液的操作如图1所示,图中的主要错误是:①
(5)准确称取6g铝土矿样品,加入100mL盐酸溶液,充分反应后向滤液中加入10mol•L﹣1试剂a的溶液,产生沉淀的质量与加入试剂a的体积关系如图2所示,则所用盐酸溶液的物质的量浓度为

您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】某课外小组研究铝土矿中Al2O3的含量.查阅资料得知,铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:
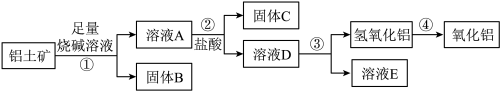
(1)提取前将铝土矿“粉碎”目的是__________ 。
(2)固体B的主要用途有________________ (写出一条即可)。
(3)第①步,向铝土矿中加入足量烧碱溶液,充分反应,发生反应的离子方程式有:_____________ (至少写一个)。
(4)第②步中加入过量盐酸的目的是____________________ ;实验室配制200mL 8mol/L的盐酸需要的玻璃仪器有__________________ 。
(5)能否把第③步中的氨水换成氢氧化钠__________ ,理由___________ 。

(1)提取前将铝土矿“粉碎”目的是
(2)固体B的主要用途有
(3)第①步,向铝土矿中加入足量烧碱溶液,充分反应,发生反应的离子方程式有:
(4)第②步中加入过量盐酸的目的是
(5)能否把第③步中的氨水换成氢氧化钠
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐1】氧缺位体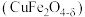 是热化学循环分解水制氢的氧化物体系。一种以黄铜矿(主要成分是
是热化学循环分解水制氢的氧化物体系。一种以黄铜矿(主要成分是 ,含
,含 、
、 等杂质)为原料制备
等杂质)为原料制备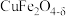 的流程如下:
的流程如下:

已知:①
②已知几种金属离子沉淀的 如表所示:
如表所示:
请回答下列问题:
(1)“焙烧”中生成了 、
、 ,写出“焙烧”中主要化学方程式:
,写出“焙烧”中主要化学方程式:_______ ,“焙烧”产生的 在有氧环境下利用石灰石浆液吸收可转变为
在有氧环境下利用石灰石浆液吸收可转变为_______ (填化学式)。
(2)“调 ”范围为
”范围为_______ ,从滤渣2中提取 的操作包括加入过量
的操作包括加入过量 溶液、过滤、向滤液通入过量的气体R,过滤、灼烧,气体R是
溶液、过滤、向滤液通入过量的气体R,过滤、灼烧,气体R是_______ (填化学式)
(3)“氧化”中 的作用是
的作用是_______ (用离子方程式表示)。
(4)“煅烧”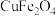 的化学方程式为
的化学方程式为_______ ,氧缺位值( )越大,活性越
)越大,活性越_______ (填“高”或“低”),与水反应制备 越容易。
越容易。
(5)钾、铁、硒形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示。已知:a、b、c的单位为 ,
, 为阿伏加德罗常数的数值,该晶体密度为
为阿伏加德罗常数的数值,该晶体密度为_______  (只列计算式)。
(只列计算式)。

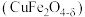 是热化学循环分解水制氢的氧化物体系。一种以黄铜矿(主要成分是
是热化学循环分解水制氢的氧化物体系。一种以黄铜矿(主要成分是 ,含
,含 、
、 等杂质)为原料制备
等杂质)为原料制备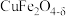 的流程如下:
的流程如下:
已知:①

②已知几种金属离子沉淀的
 如表所示:
如表所示:| 金属氢氧化物 |  |  |  |  |
开始沉淀的 | 2.7 | 7.6 | 4.0 | 6.4 |
完全沉淀的 | 3.7 | 9.6 | 5.2 | 7.6 |
(1)“焙烧”中生成了
 、
、 ,写出“焙烧”中主要化学方程式:
,写出“焙烧”中主要化学方程式: 在有氧环境下利用石灰石浆液吸收可转变为
在有氧环境下利用石灰石浆液吸收可转变为(2)“调
 ”范围为
”范围为 的操作包括加入过量
的操作包括加入过量 溶液、过滤、向滤液通入过量的气体R,过滤、灼烧,气体R是
溶液、过滤、向滤液通入过量的气体R,过滤、灼烧,气体R是(3)“氧化”中
 的作用是
的作用是(4)“煅烧”
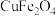 的化学方程式为
的化学方程式为 )越大,活性越
)越大,活性越 越容易。
越容易。(5)钾、铁、硒形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示。已知:a、b、c的单位为
 ,
, 为阿伏加德罗常数的数值,该晶体密度为
为阿伏加德罗常数的数值,该晶体密度为 (只列计算式)。
(只列计算式)。
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】孔雀石主要成分为Cu(OH)2CO3,还含有少量Fe2O3、SiO2等杂质。某学习小组探究孔雀石综合利用的流程如下:
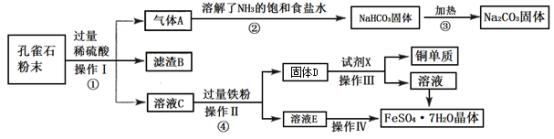
回答下列问题:
(1)步骤①中将孔雀石磨成粉末的目的是________________ ;操作I需要用到的玻璃仪器有________________ 。
(2)滤渣B的主要成分为_______ ;溶液C中的溶质有:CuSO4、________________ 。
(3)步骤②中发生反应的化学方程式为________________
(4)试剂X为________________ ;操作IV的步骤为________________ 、________________ 、过滤。

回答下列问题:
(1)步骤①中将孔雀石磨成粉末的目的是
(2)滤渣B的主要成分为
(3)步骤②中发生反应的化学方程式为
(4)试剂X为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】工业上用FeCl3溶液做印刷电路铜板的腐蚀液。化学小组设计如下流程对腐蚀废液(阳离子主要有H+、Fe3+、Fe2+和Cu2+)进行处理,实现FeCl3溶液再生并回收Cu。
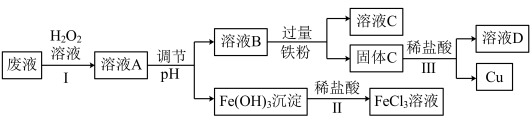
(1)FeCl3溶液腐蚀印刷电路铜板的化学方程式为:_____________ ;
(2)步骤Ⅰ的目的是将Fe2+转化为Fe3+,发生反应的离子方程式为__________ ;
(3)步骤Ⅱ中发生反应的化学方程式为_____________ ;
(4)调节pH的目的是为了使溶液A中的Fe3+全部转化为Fe(OH)3沉淀,如何证明溶液B中没有Fe3+剩余?_____________ ;
(5)固体C中的成分为________________ (填化学式);
(6)步骤Ⅲ中发生反应的离子方程式为___________ ,分离的操作名称为_______ 。

(1)FeCl3溶液腐蚀印刷电路铜板的化学方程式为:
(2)步骤Ⅰ的目的是将Fe2+转化为Fe3+,发生反应的离子方程式为
(3)步骤Ⅱ中发生反应的化学方程式为
(4)调节pH的目的是为了使溶液A中的Fe3+全部转化为Fe(OH)3沉淀,如何证明溶液B中没有Fe3+剩余?
(5)固体C中的成分为
(6)步骤Ⅲ中发生反应的离子方程式为
您最近一年使用:0次
【推荐1】某化工厂以软锰矿、闪锌矿(除主要成分为MnO2、ZnS外还含有少量的FeS、CuS、Al2O3等物质)为原料制取Zn和MnO2.
(1)在一定条件下,将这两种矿粉在硫酸溶液中相互作用,配平如下的化学方程式:MnO2+FeS+H2SO4=MnSO4+Fe2(SO4)3+S+H2O_____
(2)将所得含有Mn2+、Fe3+、Cu2+、Al3+、Zn2+的酸性溶液按如图甲的工业流程进行操作处理得溶液(Ⅳ),电解溶液(Ⅳ)即得MnO2和Zn.
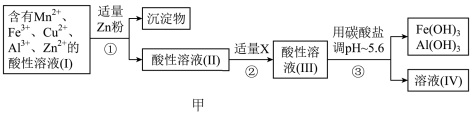
a、操作①中加Zn粉后发生反应的离子方程式为______ .
b、操作②中加入适量X的作用是什么______ ;X的首选物的化学式是: ______ .
c、操作③中所加碳酸盐的化学式是______ .
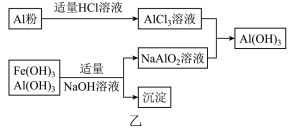
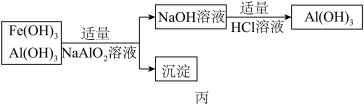
(3)为了从上述流程中产生的Fe(OH)3、Al(OH)3沉淀混合物中回收Al(OH)3,工厂设计了如图乙的有关流程图.
a、AlCl3溶液和NaAlO2溶液反应生成Al(OH)3的离子方程式为______ .若总共得到nmol Al(OH)3,则消耗的NaOH和HCl的理论量(mol)分别为 ______ 、 ______ .
b、若使用如图丙流程回收处理,请比较两个流程消耗酸碱的用量?______ .
(1)在一定条件下,将这两种矿粉在硫酸溶液中相互作用,配平如下的化学方程式:MnO2+FeS+H2SO4=MnSO4+Fe2(SO4)3+S+H2O
(2)将所得含有Mn2+、Fe3+、Cu2+、Al3+、Zn2+的酸性溶液按如图甲的工业流程进行操作处理得溶液(Ⅳ),电解溶液(Ⅳ)即得MnO2和Zn.



a、操作①中加Zn粉后发生反应的离子方程式为
b、操作②中加入适量X的作用是什么
c、操作③中所加碳酸盐的化学式是
(3)为了从上述流程中产生的Fe(OH)3、Al(OH)3沉淀混合物中回收Al(OH)3,工厂设计了如图乙的有关流程图.
a、AlCl3溶液和NaAlO2溶液反应生成Al(OH)3的离子方程式为
b、若使用如图丙流程回收处理,请比较两个流程消耗酸碱的用量?
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
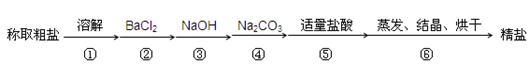
(1)按照该同学设计的实验步骤,并不能得到精盐,原因在于步骤中少了一个操作,该操作是_______ ,应加在_____ 和____ 之间。
(2)判断BaCl2已过量的方法是( )
(3)写出④中相应的离子方程式__________________ ,______________ 。
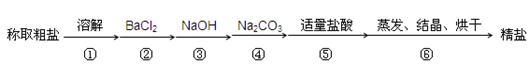
(1)按照该同学设计的实验步骤,并不能得到精盐,原因在于步骤中少了一个操作,该操作是
(2)判断BaCl2已过量的方法是
| A.取②后的上层清液少许放入试管中,再滴入几滴Na2SO4溶液,若溶液未变浑浊,则证明BaCl2已过量。 |
| B.取②后的上层清液少许放入试管中,再滴入几滴BaCl2溶液,若溶液未变浑浊,则证明BaCl2已过量。 |
| C.取②后的上层清液少许放入试管中,再滴入几滴AgNO3溶液,若溶液变浑浊,则证明BaCl2已过量。 |
| D.取②后的上层清液少许放入试管中,再滴入几滴BaCl2溶液,若溶液变浑浊,则证明BaCl2已过量。 |
(3)写出④中相应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】为了除掉粗盐中的Ca2+、Mg2+、SO 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(所加的试剂BaCl2、Na2CO3、NaOH均稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(所加的试剂BaCl2、Na2CO3、NaOH均稍过量):
称取粗盐





 精盐。
精盐。
(1)实验中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明这三种情况下使用玻璃棒的作用,溶解时________ ;过滤时_______ ;蒸发时________ 。
(2)②③④步操作中所加入的试剂各是什么?_______________ 。
(3)判断BaCl2已过量的方法是_____________________ 。
 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(所加的试剂BaCl2、Na2CO3、NaOH均稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(所加的试剂BaCl2、Na2CO3、NaOH均稍过量):称取粗盐






 精盐。
精盐。(1)实验中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明这三种情况下使用玻璃棒的作用,溶解时
(2)②③④步操作中所加入的试剂各是什么?
(3)判断BaCl2已过量的方法是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有CaCl2、MgCl2、Na2SO4以及泥沙等杂质,以下是制备精盐的实验方案,步骤如图:

(1)在第①步粗盐溶解操作中要用到玻璃棒搅拌,其目的是_________________ ;
(2)第②步操作的目的是除去粗盐中的______________ ;( 填化学式,下同)
(3)第④步操作的目的是除去粗盐中的_____________ 、______________ ;,写出相应的离子反应方程式:_______________________ ;_________________________ ;

(1)在第①步粗盐溶解操作中要用到玻璃棒搅拌,其目的是
(2)第②步操作的目的是除去粗盐中的
(3)第④步操作的目的是除去粗盐中的
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】工业上以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(MnCO3)。其工业流程如下:
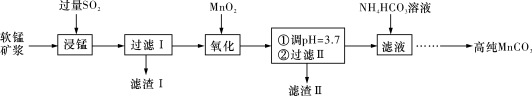
(1)过滤Ⅰ所得滤液中主要存在的两种金属阳离子为____ 和_____ (填离子符号)。
(2)写出氧化过程中MnO2与SO2反应的化学方程式:____________ 。
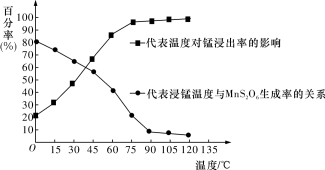
(3)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示,为减少MnS2O6的生成,“浸锰”的适宜温度是___________ 。
(4)向过滤Ⅱ所得的滤液中加入NH4HCO3溶液时温度控制在30-35℃,温度不宜太高的原因是___ 。
(5)加入NH4HCO3溶液后,生成MnCO3沉淀,同时还有气体生成,写出反应的离子方程式:_______ 。

(1)过滤Ⅰ所得滤液中主要存在的两种金属阳离子为
(2)写出氧化过程中MnO2与SO2反应的化学方程式:
(3)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示,为减少MnS2O6的生成,“浸锰”的适宜温度是

(4)向过滤Ⅱ所得的滤液中加入NH4HCO3溶液时温度控制在30-35℃,温度不宜太高的原因是
(5)加入NH4HCO3溶液后,生成MnCO3沉淀,同时还有气体生成,写出反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】富马酸亚铁(C4H2O4Fe)常用于治疗缺铁性贫血,也可作食品营养强化剂,它可由糠醛(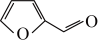 )和硫酸亚铁制备。
)和硫酸亚铁制备。
已知: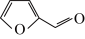
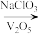 HOOCCH=CHCOOH+CO2↑
HOOCCH=CHCOOH+CO2↑
回答下列问题:
I.制备富马酸(实验装置如图所示,夹持装置已略去)
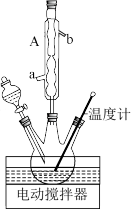
(1)将45.0g氯酸钠、0.2g五氧化二钒置于三颈烧瓶中,加入适量蒸馏水,滴加糠醛并加热至90~100℃,维持此温度3~4h。装置图中仪器A的名称是__________ ,冷凝水应从_____ 口流入,_____ 口流出。(用图中字母a、b表示)
(2)冰水冷却使产品结晶,并通过______________ 操作可以得到富马酸粗品。
(3)用1mol/LHCl溶液对富马酸粗品进行重结晶,得到纯富马酸。该操作中用1mol/LHCl溶液的原因是________________________ (用离子方程式和适当的文字解释)。
II.合成富马酸亚铁
(4)取一定量的富马酸溶于适量水中,加入碳酸钠并加热、搅拌,调节pH为6.5~6.7,产生大量气泡。写出发生反应的化学方程式____________________________________ 。
(5)将硫酸亚铁溶液和适量的Na2SO3溶液缓慢加入上述反应液中,维持温度在100℃并充分搅拌3~4h。该操作过程中加入适量的Na2SO3溶液,其目的是_______________ 。
(6)过滤、洗涤、干燥得到产品。洗涤过程中证明富马酸亚铁产品已洗涤干净的实验方法是___________ 。
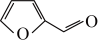 )和硫酸亚铁制备。
)和硫酸亚铁制备。已知:
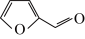
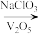 HOOCCH=CHCOOH+CO2↑
HOOCCH=CHCOOH+CO2↑ 回答下列问题:
I.制备富马酸(实验装置如图所示,夹持装置已略去)

(1)将45.0g氯酸钠、0.2g五氧化二钒置于三颈烧瓶中,加入适量蒸馏水,滴加糠醛并加热至90~100℃,维持此温度3~4h。装置图中仪器A的名称是
(2)冰水冷却使产品结晶,并通过
(3)用1mol/LHCl溶液对富马酸粗品进行重结晶,得到纯富马酸。该操作中用1mol/LHCl溶液的原因是
II.合成富马酸亚铁
(4)取一定量的富马酸溶于适量水中,加入碳酸钠并加热、搅拌,调节pH为6.5~6.7,产生大量气泡。写出发生反应的化学方程式
(5)将硫酸亚铁溶液和适量的Na2SO3溶液缓慢加入上述反应液中,维持温度在100℃并充分搅拌3~4h。该操作过程中加入适量的Na2SO3溶液,其目的是
(6)过滤、洗涤、干燥得到产品。洗涤过程中证明富马酸亚铁产品已洗涤干净的实验方法是
您最近一年使用:0次



