解题方法
1 . 利用铝锂钴废料(主要成分为Co3O4,还含有少量铝箔、LiCoO2等杂质,Co3O4具有较强氧化性)制备CoO的工艺流程如图所示。
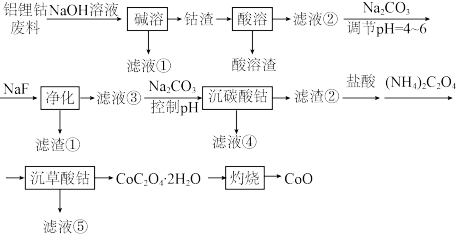
已知:I.不同浸出剂“酸溶”结果
II.Al3+在pH为5.2时沉淀完全。
III.LiF的Ksp为1.8×10-3。
回答下列问题:
(1)“碱溶”时为提高浸出率可采取的措施是_______ (写出一种即可),并写出主要的离子方程式:_______ 。
(2)“酸溶”时最佳的浸出剂应该选择_______ ,并说明理由:_______ 。
(3)“净化”时,加NaF目的是将Li+转化为沉淀,当滤液③中c(F-)=4.0×10-3mol·L-1时计算“净化”后残余c(Li+)=_______ mol·L-1。
(4)写出滤渣②“酸溶”后与草酸铵反应的离子方程式_______ 。

已知:I.不同浸出剂“酸溶”结果
浸出剂 | 浸出液化学成分/(g·L-1) | 钴浸出率/% | |
Co | Al | ||
HCl | 80.84 | 5.68 | 98.4 |
H2SO4+Na2S2O3 | 84.91 | 5.96 | 98.0 |
III.LiF的Ksp为1.8×10-3。
回答下列问题:
(1)“碱溶”时为提高浸出率可采取的措施是
(2)“酸溶”时最佳的浸出剂应该选择
(3)“净化”时,加NaF目的是将Li+转化为沉淀,当滤液③中c(F-)=4.0×10-3mol·L-1时计算“净化”后残余c(Li+)=
(4)写出滤渣②“酸溶”后与草酸铵反应的离子方程式
您最近一年使用:0次
2022-06-29更新
|
369次组卷
|
3卷引用:2022年海南省高考真题变式题15-19
2021·全国·模拟预测
解题方法
2 . 利用钒钛磁铁矿冶炼后产生的钒渣(主要含FeO·V2O3、Al2O3、SiO2及少量可溶性磷酸盐)生产V2O5的工艺流程如下,回答下列问题:

已知:①V2O5、Al2O3、SiO2可与Na2CO3、NaCl组成的混合钠盐在高温下反应,并转化为NaVO3、NaAlO2、Na2SiO3等可溶性钠盐。
②
(1)为提高钒渣的焙烧效率,可采取的措施是___________ (任写一种),实验室中“焙烧”用到的仪器是___________ 。
(2)焙烧Ⅰ包括氧化和钠化成盐两个过程,氧化的目的是获得V2O5,写出氧化过程中O2氧化FeO·V2O3的化学方程式___________ ;
(3)分析“浸取”所得废渣Ⅰ的主要成分是___________ ;
(4)精制I中“加盐酸调pH=1~1.6”有两种作用,一是将溶液中的___________ (填化学式,下同)转为沉淀除去,二是将溶液中的___________ 转为可与氨水生成沉淀除去的离子。
(5)沉钒所得 沉淀需进行洗涤,洗涤时除去的阴离子主要是
沉淀需进行洗涤,洗涤时除去的阴离子主要是___________ (写化学式),如何检验沉淀已经洗涤干净___________ 。
(6)在500℃时焙烧脱氨制得产品V2O5,反应方程式___________ 。

已知:①V2O5、Al2O3、SiO2可与Na2CO3、NaCl组成的混合钠盐在高温下反应,并转化为NaVO3、NaAlO2、Na2SiO3等可溶性钠盐。
②

(1)为提高钒渣的焙烧效率,可采取的措施是
(2)焙烧Ⅰ包括氧化和钠化成盐两个过程,氧化的目的是获得V2O5,写出氧化过程中O2氧化FeO·V2O3的化学方程式
(3)分析“浸取”所得废渣Ⅰ的主要成分是
(4)精制I中“加盐酸调pH=1~1.6”有两种作用,一是将溶液中的
(5)沉钒所得
 沉淀需进行洗涤,洗涤时除去的阴离子主要是
沉淀需进行洗涤,洗涤时除去的阴离子主要是(6)在500℃时焙烧脱氨制得产品V2O5,反应方程式
您最近一年使用:0次
名校
解题方法
3 . 铍作为一种新兴材料日益被重视,有“超级金属、尖端金属、空间金属”之称。工业上常用绿柱石(主要成分为3BeO·Al2O3·6SiO2,还含有铁等杂质)冶炼铍,一种简化的工艺流程如下:

按元素周期表的对角线规则Be和Al性质相似;几种金属阳离子的氢氧化物沉淀时的pH如下表。
(1)步骤②中将熔块粉碎的目的是___________ 。
(2)步骤③加入H2O2时发生反应的离子方程式为___________ ,从滤液1中得到沉淀的合理pH为___________ (填字母)。
A.3.3~3.7 B.3.7~5.0 C.5.0~5.2 D.5.2~6.5
(3)步骤④不宜使用NaOH溶液来沉淀Be2+的原因是___________ 。从溶液中得到(NH4)2BeF4的实验操作是___________ 、___________ 、过滤、洗涤、干燥。
(4)步骤⑦需要隔绝空气的环境,其原因是___________ 。
(5)若绿柱石中BeO的含量为a%,上述过程生产Be的产率为b%。则1 t该绿柱石理论上能生产含铍量2%的镀铜合金___________ t。

按元素周期表的对角线规则Be和Al性质相似;几种金属阳离子的氢氧化物沉淀时的pH如下表。
| Fe3+ | Al3+ | Fe2+ | Be2+ | |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 5.2 |
| 沉淀完全时 | 3.7 | 5.0 | 9.7 | 8.8 |
(1)步骤②中将熔块粉碎的目的是
(2)步骤③加入H2O2时发生反应的离子方程式为
A.3.3~3.7 B.3.7~5.0 C.5.0~5.2 D.5.2~6.5
(3)步骤④不宜使用NaOH溶液来沉淀Be2+的原因是
(4)步骤⑦需要隔绝空气的环境,其原因是
(5)若绿柱石中BeO的含量为a%,上述过程生产Be的产率为b%。则1 t该绿柱石理论上能生产含铍量2%的镀铜合金
您最近一年使用:0次
2021-10-15更新
|
597次组卷
|
5卷引用:2020年海南卷化学高考真题变式题9-14
(已下线)2020年海南卷化学高考真题变式题9-14(已下线)2020年海南卷化学高考真题变式题15-19黑龙江嫩江市高级中学2021-2022学年高三上学期9月月考化学试题(已下线)2022年新高考化学时事热点情境化考题---化工流程重庆市万州第二高级中学2023届高三下学期第二次诊断测试化学试题
名校
解题方法
4 . 二氧化锆(ZrO2)是重要的耐高温材料,可用作陶瓷遮光剂和良好的催化剂。天然锆英石(ZrSiO4)含有FeO、Al2O3、SiO2等杂质,工业以锆英石为原料制备ZrO2的工艺流程如图:
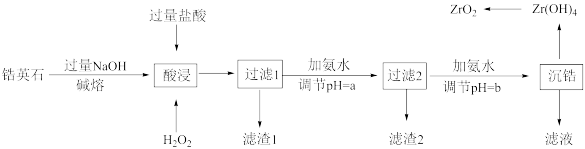
已知:
①高温时锆英石能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+。
②部分离子在实验条件下开始沉淀和完全沉淀时的pH如下表:
结合上面信息回答:
(1)ZrSiO4中Zr的化合价为____ 。滤渣1的主要成分的名称为____ 。
(2)“酸浸”过程中所加的H2O2可用____ 代替。该过程中生成Al3+的离子方程式为____ 。
(3)第一次加氨水调节pH的范围为______ 。
A.3.2~3.3 B.3.3~5.2 C.5.2~6.2 D.6.2~8.0
(4)写出沉锆反应过程中的离子方程式________ 。
(5)向“滤液”中加碳酸钙粉并加热,会放出二氧化碳和_______ 两种气体。

已知:
①高温时锆英石能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+。
②部分离子在实验条件下开始沉淀和完全沉淀时的pH如下表:
| 离子 | Fe3+ | Al3+ | ZrO2+ | Fe2+ |
| 开始沉淀时pH | 1.9 | 3.3 | 6.2 | 7.6 |
| 完全沉淀时pH | 3.2 | 5.2 | 8.0 | 9.7 |
(1)ZrSiO4中Zr的化合价为
(2)“酸浸”过程中所加的H2O2可用
(3)第一次加氨水调节pH的范围为
A.3.2~3.3 B.3.3~5.2 C.5.2~6.2 D.6.2~8.0
(4)写出沉锆反应过程中的离子方程式
(5)向“滤液”中加碳酸钙粉并加热,会放出二氧化碳和
您最近一年使用:0次



