1 . 利用电石渣[主要成分为 ,含少量
,含少量 、
、 、
、 等杂质]制备碳酸钙,同时获得氧化铝,工艺流程如图。下列说法错误的是
等杂质]制备碳酸钙,同时获得氧化铝,工艺流程如图。下列说法错误的是
 ,含少量
,含少量 、
、 、
、 等杂质]制备碳酸钙,同时获得氧化铝,工艺流程如图。下列说法错误的是
等杂质]制备碳酸钙,同时获得氧化铝,工艺流程如图。下列说法错误的是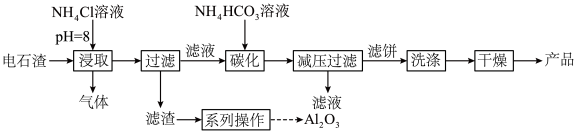
| A.“气体”为NH3 |
B.“碳化”反应为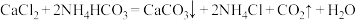 |
| C.“浸取”和“碳化”为了加快反应速率,需在高温下进行 |
D.“滤渣”主要成分为 、 、 |
您最近一年使用:0次
2 . 工业上利用石煤矿粉(主要含V2O3及少量Al2O3、SiO2)为原料生产V2O5,工艺流程如下:

已知:“水溶”、“转沉”、“转化”、“沉钒”后,所得含钒物质依次为NaVO3、Ca3(VO4)2、(NH4)3VO4、NH4VO3。
下列说法正确的是

已知:“水溶”、“转沉”、“转化”、“沉钒”后,所得含钒物质依次为NaVO3、Ca3(VO4)2、(NH4)3VO4、NH4VO3。
下列说法正确的是
A.“焙烧”时V2O3发生的方程式为:V2O3+O2 V2O5 V2O5 |
| B.滤液1的成分为Na[Al(OH)4] |
| C.“转化”时滤渣II经高温煅烧后水浸所得物质可导入到“转沉”操作单元中重复使用 |
D.“沉钒”需要加入过量NH4Cl,其中一个原因是调节pH,将VO 转化为VO 转化为VO |
您最近一年使用:0次
名校
3 . 工业上以铬铁矿(主要成分为FeCr2O4,含有MgO、Al2O3等杂质)为主要原料制备K2Cr2O7的工艺流程如图(部分操作和条件略):

已知:
①100g水中溶解度数据如表所示。
②Cr2O +H2O
+H2O 2CrO
2CrO +2H+
+2H+
下列说法错误的是

已知:
①100g水中溶解度数据如表所示。
| 物质 | 20℃ | 40℃ | 50℃ | 80℃ | 100℃ |
| K2Cr2O7/g | 12.0 | 29.0 | 37.0 | 73.0 | 102.0 |
| Na2SO4/g | 19.5 | 48.8 | 46.2 | 43.7 | 42.5 |
 +H2O
+H2O 2CrO
2CrO +2H+
+2H+下列说法错误的是
| A.“高温煅烧”中Na2O2做氧化剂 |
| B.“调pH”时应加过量硫酸以保证除杂效果 |
| C.“沉铬”时应蒸发浓缩、冷却至40℃后过滤得K2Cr2O7晶体 |
| D.“沉铬”后滤液可回到“水浸”过程循环利用 |
您最近一年使用:0次
2022-02-25更新
|
280次组卷
|
4卷引用:山东省枣庄市2022-2023学年高三下学期二模考试化学试题变式题(不定项选择题)
(已下线)山东省枣庄市2022-2023学年高三下学期二模考试化学试题变式题(不定项选择题)山东省烟台第二中学2021-2022学年高三下学期开年摸底联考化学试题 山东省济宁市泗水县2022-2023学年高三上学期期中考试化学试题湖南省百师联盟2021-2022学年高三下学期开年摸底联考化学试题
名校
解题方法
4 . 铂是一种稀有的贵金属,在一些废板卡、含铂废合金、镀铂、涂铂的废料以及含铂废催化剂含有一定量的铂,以下是某工厂回收铂的工艺流程,已知含铂(Pt)废渣的主要成分为Al2O3,少量SnO2、SiO2和Pt。
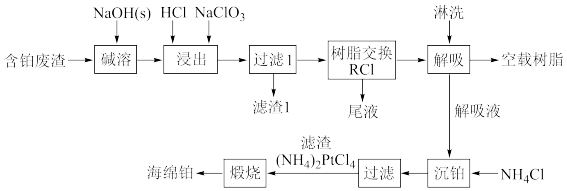
氯铂酸铵[(NH4)2PtCl6],黄色,难溶于水,易溶于盐酸并生成H2PtCl6。
回答下列问题:
(1)“碱溶”时,使用的坩埚的材质是_______ (填标号)。试写出一种金属铂在中学化学中的应用_______ 。
A.陶瓷 B.石英 C.铝 D.铁
(2)“浸出”时,铂生成PtCl ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
(3)“滤渣1”的主要成分为H2SnO3和_______ ,若“滤渣1”中含有少量的铂,可将其返回_______ (填工序名称)。
(4)“树脂交换”时,被阴离子交换树脂RCl吸附的铂的存在形式是_______ (填化学式),尾液中溶质的主要成分为_______ (填化学式)。
(5)滤渣氯铂酸铵[(NH4)2PtCl6]表面有大量氯化铵等可溶性的盐,在煅烧操作之前要将沉淀表面的杂质洗去,洗涤沉淀方法是_______ 。
(6)“煅烧”时温度控制在750℃,除生成Pt外,还有NH3、HCl等生成,写出该反应的化学方程式:_______ 。

氯铂酸铵[(NH4)2PtCl6],黄色,难溶于水,易溶于盐酸并生成H2PtCl6。
回答下列问题:
(1)“碱溶”时,使用的坩埚的材质是
A.陶瓷 B.石英 C.铝 D.铁
(2)“浸出”时,铂生成PtCl
 ,该反应的离子方程式为
,该反应的离子方程式为(3)“滤渣1”的主要成分为H2SnO3和
(4)“树脂交换”时,被阴离子交换树脂RCl吸附的铂的存在形式是
(5)滤渣氯铂酸铵[(NH4)2PtCl6]表面有大量氯化铵等可溶性的盐,在煅烧操作之前要将沉淀表面的杂质洗去,洗涤沉淀方法是
(6)“煅烧”时温度控制在750℃,除生成Pt外,还有NH3、HCl等生成,写出该反应的化学方程式:
您最近一年使用:0次
名校
解题方法
5 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属 、
、 、
、 及其氧化物,还有少量其他不溶性物质。采用如下所示工艺流程回收其中的镍制备硫酸镍晶体
及其氧化物,还有少量其他不溶性物质。采用如下所示工艺流程回收其中的镍制备硫酸镍晶体 :
:

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“碱浸”中 的两个作用分别是
的两个作用分别是_______ 。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式:_______ 。
(2)“滤液②”中含有的金属离子是_______ 。
(3)“转化”中可替代 的物质是
的物质是_______ 。若工艺流程改为先“调 ”后“转化”,即
”后“转化”,即

“滤液③”中可能含有的杂质离子为_______ 。
(4)利用上述表格数据,计算 的
的
_______ (列出计算式)。如果“转化”后的溶液中 浓度为
浓度为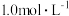 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是_______ 。
(5)硫酸镍在强碱溶液中用 氧化,可沉淀出用作镍镉电池正极材料的
氧化,可沉淀出用作镍镉电池正极材料的 。写出该反应的离子方程式:
。写出该反应的离子方程式:_______ 。
 、
、 、
、 及其氧化物,还有少量其他不溶性物质。采用如下所示工艺流程回收其中的镍制备硫酸镍晶体
及其氧化物,还有少量其他不溶性物质。采用如下所示工艺流程回收其中的镍制备硫酸镍晶体 :
:
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 |  |  |  |  |
开始沉淀时(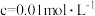 )的 )的 | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时(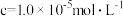 )的 )的 | 8.8 | 4.7 | 3.2 | 9.0 |
(1)“碱浸”中
 的两个作用分别是
的两个作用分别是(2)“滤液②”中含有的金属离子是
(3)“转化”中可替代
 的物质是
的物质是 ”后“转化”,即
”后“转化”,即
“滤液③”中可能含有的杂质离子为
(4)利用上述表格数据,计算
 的
的
 浓度为
浓度为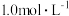 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是(5)硫酸镍在强碱溶液中用
 氧化,可沉淀出用作镍镉电池正极材料的
氧化,可沉淀出用作镍镉电池正极材料的 。写出该反应的离子方程式:
。写出该反应的离子方程式:
您最近一年使用:0次
2021-09-29更新
|
465次组卷
|
3卷引用:2020年山东卷化学高考真题变式题16-20
解题方法
6 . 一种综合利用铜矿(主要为CuS,含少量FeS、SiO2)、软锰矿(主要为MnO2,含少量Fe2O3、Al2O3)制取MnCO3、CuO的工艺流程如图:
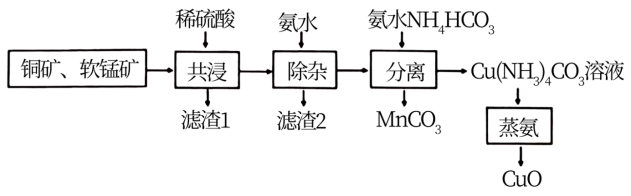
该工艺条件下,溶液中金属离子开始沉淀和沉淀完全的pH如表所示:
(1)“共浸”时,为提高浸取率,可采取的措施为___ 。(填一种方法即可)
(2)滤渣1含有S,为回收S,可先加入CS2,待固液分离后,再___ 得到S。
(3)“共浸”时,发生主要反应的离子方程式为___ 。
(4)该工艺“除杂”中,杂质离子沉淀的先后顺序为___ (填离子符号);“除杂”时控制pH为4.7~4.8,此时溶液中c(Fe3+):c(Al3+)=__ 。
(5)得到MnCO3的离子方程式为___ 。
(6)“蒸氨”是将氨从其盐及固液混合物中蒸出,相应的化学方程式为___ 。

该工艺条件下,溶液中金属离子开始沉淀和沉淀完全的pH如表所示:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ | Cu2+ |
| 开始沉淀pH | 1.9 | 7.0 | 3.0 | 8.1 | 4.8 |
| 沉淀完全(c=1.0×10-5mol·L-1)的pH | 3.2 | 9.0 | 4.7 | 10.1 | 6.7 |
(2)滤渣1含有S,为回收S,可先加入CS2,待固液分离后,再
(3)“共浸”时,发生主要反应的离子方程式为
(4)该工艺“除杂”中,杂质离子沉淀的先后顺序为
(5)得到MnCO3的离子方程式为
(6)“蒸氨”是将氨从其盐及固液混合物中蒸出,相应的化学方程式为
您最近一年使用:0次
7 . 钛铁矿(FeTiO3)中往往含有Fe2O3、MgO、CaO、Al2O3、SiO2等杂质。一种硫酸法制取白色颜料钛白粉(TiO2)生产工艺如下:
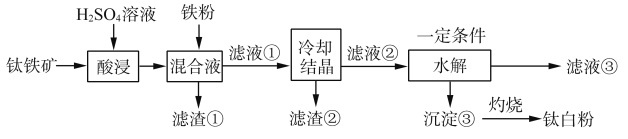 +
+
已知:①酸浸后,钛主要以TiOSO4形式存在;
②强电解质TiOSO4在溶液中仅能电离出 和一种阳离子。
和一种阳离子。
③H2TiO3不溶于水和稀酸。
(1)为提高酸浸速率,一般采取的措施是___________ 。(写两条)
(2)滤渣①的主要成分是___________ 。
(3)酸浸过程中,写出含钛化合物发生反应的化学方程式___________ 。
(4)加入铁粉的目的是还原体系中的Fe3+。为探究最佳反应条件,某实验室做如下尝试。

①在其它条件不变的情况下,体系中Fe(Ⅲ)含量随pH变化如图1,试分析在pH介于4~6之间时,Fe(Ⅲ)含量基本保持不变的原因:___________ 。
②保持其它条件不变的情况下,体系中Fe(Ⅲ)含量随温度变化如图2,55℃后,Fe(Ⅲ)含量增大的原因是___________ 。
(5)水解过程中得到沉淀③的化学式为___________ 。
 +
+已知:①酸浸后,钛主要以TiOSO4形式存在;
②强电解质TiOSO4在溶液中仅能电离出
 和一种阳离子。
和一种阳离子。③H2TiO3不溶于水和稀酸。
(1)为提高酸浸速率,一般采取的措施是
(2)滤渣①的主要成分是
(3)酸浸过程中,写出含钛化合物发生反应的化学方程式
(4)加入铁粉的目的是还原体系中的Fe3+。为探究最佳反应条件,某实验室做如下尝试。

①在其它条件不变的情况下,体系中Fe(Ⅲ)含量随pH变化如图1,试分析在pH介于4~6之间时,Fe(Ⅲ)含量基本保持不变的原因:
②保持其它条件不变的情况下,体系中Fe(Ⅲ)含量随温度变化如图2,55℃后,Fe(Ⅲ)含量增大的原因是
(5)水解过程中得到沉淀③的化学式为
您最近一年使用:0次
解题方法
8 . 实验室以铬铁矿(主要成分是 ,还含有少量
,还含有少量 、
、 等杂质)为原料制备重铬酸钾晶体(
等杂质)为原料制备重铬酸钾晶体( 相对分子质量为294)的流程如下:
相对分子质量为294)的流程如下:

已知:①
② 时,
时, 含量极小
含量极小
请回答下列问题:
(1)① 中各元素化合价均为整数,则
中各元素化合价均为整数,则 为
为_______ 价,将它用氧化物的形式表示为_______ 。
②“操作1”的反应条件是高温,写出主要的化学反应化学方程式_______ 。
③“操作1”中的反应,在常温下的反应速率较慢,为使反应速率增大,除升高温度外,还可采取的措施为_______ 、_______ (写出两条)。
(2)固体X中主要含有_______ (填写化学式),固体Y中主要含有_______ (填写化学式)。
(3) 在pH为3.7时可完全转化为
在pH为3.7时可完全转化为 。在上述流程中所得
。在上述流程中所得 溶液中含有少量
溶液中含有少量 。请结合下图有关物质的溶解度曲线,设计由
。请结合下图有关物质的溶解度曲线,设计由 溶液制备
溶液制备 固体的实验方案:
固体的实验方案:_______ (实验中须选用的试剂:硫酸、 溶液、
溶液、 固体、蒸馏水)。
固体、蒸馏水)。

(4)某工厂用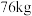 铬铁矿粉(含
铬铁矿粉(含 )制备
)制备 ,最终得到产品
,最终得到产品 ,则产率为
,则产率为___ 。
 ,还含有少量
,还含有少量 、
、 等杂质)为原料制备重铬酸钾晶体(
等杂质)为原料制备重铬酸钾晶体( 相对分子质量为294)的流程如下:
相对分子质量为294)的流程如下:
已知:①

②
 时,
时, 含量极小
含量极小请回答下列问题:
(1)①
 中各元素化合价均为整数,则
中各元素化合价均为整数,则 为
为②“操作1”的反应条件是高温,写出主要的化学反应化学方程式
③“操作1”中的反应,在常温下的反应速率较慢,为使反应速率增大,除升高温度外,还可采取的措施为
(2)固体X中主要含有
(3)
 在pH为3.7时可完全转化为
在pH为3.7时可完全转化为 。在上述流程中所得
。在上述流程中所得 溶液中含有少量
溶液中含有少量 。请结合下图有关物质的溶解度曲线,设计由
。请结合下图有关物质的溶解度曲线,设计由 溶液制备
溶液制备 固体的实验方案:
固体的实验方案: 溶液、
溶液、 固体、蒸馏水)。
固体、蒸馏水)。
(4)某工厂用
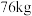 铬铁矿粉(含
铬铁矿粉(含 )制备
)制备 ,最终得到产品
,最终得到产品 ,则产率为
,则产率为
您最近一年使用:0次
解题方法
9 . 利用蒽醌法生产双氧水时的废镍催化剂(含Ni、Al蒽醌及氢蒽醌等有机物和少量Fe杂质)制备 的工艺流程如下:
的工艺流程如下:

回答下列问题:
(1)“焙烧”的主要目的是_______ 。
(2)“碱溶”时发生反应的化学方程式为_______ 。
(3)为了尽可能多地获得 ,“除铁”所用的试剂为
,“除铁”所用的试剂为_______ (填化学式)。
(4)若“除铁”时,溶液中 ,调节pH值使
,调节pH值使 恰好沉淀完全[即溶液中
恰好沉淀完全[即溶液中
 ],此时是否有
],此时是否有 沉淀生成:
沉淀生成:_______ {通过列式计算说明。已知: 、
、 }。
}。
(5)“酸化”使溶液 的目的是
的目的是_______ ,“酸化”后从溶液中得到硫酸镍晶体,包含的操作是_______ 、过滤(水洗)及干燥。
(6)重量法测定产品中 的质量分数,步骤如下:
的质量分数,步骤如下:
称取2.0g 样品于烧杯中,加入1mL盐酸,再加蒸馏水并加热至样品全部溶解,冷却至室温,然后转移至100mL的容量瓶中,用蒸馏水稀释至刻度、摇匀。用移液管移取10mL样品液于锥形瓶中,加入蒸馏水、5mL氯化铵溶液、5mL酒石酸溶液(消除
样品于烧杯中,加入1mL盐酸,再加蒸馏水并加热至样品全部溶解,冷却至室温,然后转移至100mL的容量瓶中,用蒸馏水稀释至刻度、摇匀。用移液管移取10mL样品液于锥形瓶中,加入蒸馏水、5mL氯化铵溶液、5mL酒石酸溶液(消除 干扰),盖上表面皿,加热至沸腾。冷却至70~80
干扰),盖上表面皿,加热至沸腾。冷却至70~80 时,在不断搅拌下缓慢加入稍过量的二甲基乙二醛肟溶液,充分反应后生成二甲基乙二醛肟镍沉淀(化学式为
时,在不断搅拌下缓慢加入稍过量的二甲基乙二醛肟溶液,充分反应后生成二甲基乙二醛肟镍沉淀(化学式为 ,式量为173),经过滤乙醇洗涤,于105~110
,式量为173),经过滤乙醇洗涤,于105~110 干燥至恒定,称量固体质量为m g。产品中
干燥至恒定,称量固体质量为m g。产品中 的质量分数为
的质量分数为_______ (用含m的代数式表示)。
 的工艺流程如下:
的工艺流程如下:
回答下列问题:
(1)“焙烧”的主要目的是
(2)“碱溶”时发生反应的化学方程式为
(3)为了尽可能多地获得
 ,“除铁”所用的试剂为
,“除铁”所用的试剂为(4)若“除铁”时,溶液中
 ,调节pH值使
,调节pH值使 恰好沉淀完全[即溶液中
恰好沉淀完全[即溶液中
 ],此时是否有
],此时是否有 沉淀生成:
沉淀生成: 、
、 }。
}。(5)“酸化”使溶液
 的目的是
的目的是(6)重量法测定产品中
 的质量分数,步骤如下:
的质量分数,步骤如下:称取2.0g
 样品于烧杯中,加入1mL盐酸,再加蒸馏水并加热至样品全部溶解,冷却至室温,然后转移至100mL的容量瓶中,用蒸馏水稀释至刻度、摇匀。用移液管移取10mL样品液于锥形瓶中,加入蒸馏水、5mL氯化铵溶液、5mL酒石酸溶液(消除
样品于烧杯中,加入1mL盐酸,再加蒸馏水并加热至样品全部溶解,冷却至室温,然后转移至100mL的容量瓶中,用蒸馏水稀释至刻度、摇匀。用移液管移取10mL样品液于锥形瓶中,加入蒸馏水、5mL氯化铵溶液、5mL酒石酸溶液(消除 干扰),盖上表面皿,加热至沸腾。冷却至70~80
干扰),盖上表面皿,加热至沸腾。冷却至70~80 时,在不断搅拌下缓慢加入稍过量的二甲基乙二醛肟溶液,充分反应后生成二甲基乙二醛肟镍沉淀(化学式为
时,在不断搅拌下缓慢加入稍过量的二甲基乙二醛肟溶液,充分反应后生成二甲基乙二醛肟镍沉淀(化学式为 ,式量为173),经过滤乙醇洗涤,于105~110
,式量为173),经过滤乙醇洗涤,于105~110 干燥至恒定,称量固体质量为m g。产品中
干燥至恒定,称量固体质量为m g。产品中 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
10 . 以某冶金工业产生的废渣(含Cr2O3、SiO2及少量的Al2O3)为原料,根据下列流程可制备K2Cr2O7。
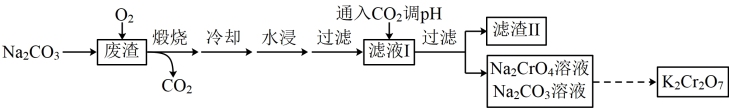
下列说法正确的是

下列说法正确的是
| A.煅烧时没有发生氧化还原反应 |
| B.滤渣Ⅱ中主要成分是Al(OH)3 |
| C.可循环使用的物质是CO2和Na2CO3 |
| D.由Na2CrO4转化为K2Cr2O7的过程中需加入KOH |
您最近一年使用:0次
2021-03-04更新
|
1841次组卷
|
13卷引用:热点8 无机化工流程分析(选择题)-2021年高考化学【热点·重点·难点】专练(山东专用)
(已下线)热点8 无机化工流程分析(选择题)-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)押山东卷第09题 化工生产流程选择题-备战2021年高考化学临考题号押题(山东卷)山东省聊城市第一中学2021届高三下学期开学模拟考试化学试题(已下线)热点5 常见元素及其化合物的性质与相互转化-2021年高考化学专练【热点·重点·难点】(新高考)山东省济南市平阴县第一中学2021届高三下学期3月月考化学试题(已下线)难点1 化工流程微设计-2021年高考化学【热点·重点·难点】专练(新高考)(已下线)考向06 钠及其重要化合物-备战2022年高考化学一轮复习考点微专题(已下线)专题06 金属及其化合物-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题14 无机综合运用(选择题)-2022年高考化学二轮复习重点专题常考点突破练巩固训练7湖南省2021年普通高中学业水平选择考适应性测试化学试题江苏省南京师范大学附属中学2021-2022学年高三下学期开学考试化学试题 江苏省苏州市重点中学2022-2023学年高三上学期10月月考化学试题



