名校
解题方法
1 . 部分含铁物质价类二维图如图所示。下列说法错误的是


| A.a可与e反应生成b |
| B.b既可被氧化,也可被还原 |
| C.e溶液中加入铁粉有浅绿色沉淀生成 |
| D.可存在b→c→d→e→b的循环转化关系 |
您最近一年使用:0次
2023-11-25更新
|
422次组卷
|
5卷引用:北京市海淀区第二十中学2022-2023学年高一上学期11月月考化学试题
解题方法
2 . 室温下,向新制酸化的和未酸化的0.1 mol·L-1的FeSO4溶液中通入氧气且搅拌时,pH变化曲线如图。

已知:Fe(OH)3的 ;Fe(OH)2的
;Fe(OH)2的 ;Fe3+开始沉淀时的pH≈1.5;Fe2+开始沉淀时的pH≈6.3
;Fe3+开始沉淀时的pH≈1.5;Fe2+开始沉淀时的pH≈6.3
下列说法不正确 的是

已知:Fe(OH)3的
 ;Fe(OH)2的
;Fe(OH)2的 ;Fe3+开始沉淀时的pH≈1.5;Fe2+开始沉淀时的pH≈6.3
;Fe3+开始沉淀时的pH≈1.5;Fe2+开始沉淀时的pH≈6.3下列说法
| A.M点对应的溶液中Fe2+水解程度小于P点对应的溶液中Fe2+水解程度 |
B.导致M点→N点pH升高的反应为: |
C.导致P点→Q点pH降低的反应为: |
| D.O点和Q点后,Fe2+全部转化为Fe(OH)3,不再发生Fe2+的氧化反应 |
您最近一年使用:0次
名校
解题方法
3 . 某溶液中含大量Fe2+、Mg2+、Fe3+、Na+、Cl-、SO 离子,其中加入足量的Na2O2固体后,再加入足量的盐酸溶解沉淀,最后溶液中的离子数目与反应前相比保持不变的是
离子,其中加入足量的Na2O2固体后,再加入足量的盐酸溶解沉淀,最后溶液中的离子数目与反应前相比保持不变的是
 离子,其中加入足量的Na2O2固体后,再加入足量的盐酸溶解沉淀,最后溶液中的离子数目与反应前相比保持不变的是
离子,其中加入足量的Na2O2固体后,再加入足量的盐酸溶解沉淀,最后溶液中的离子数目与反应前相比保持不变的是| A.Na+、Fe2+ | B.Mg2+、SO | C.Fe3+、SO | D.Mg2+、Cl- |
您最近一年使用:0次
2023-01-17更新
|
472次组卷
|
2卷引用:北京师范大学附属中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
4 . 长期放置的FeSO4溶液易被氧化而变质。某兴趣小组分别对新制和久置的两瓶FeSO4溶液进行了如表实验。
I.分别取2mL新制的FeSO4溶液于三支试管中,进行如图实验。
(1)方案i中,现象a是立即产生白色沉淀,白色沉淀逐渐变为灰绿色,最终变为红褐色。白色沉淀的化学式是____ ,最终变为红褐色的化学方程式是____ 。
(2)方案iii的实验现象是____ ,写出氯水参与反应的的离子方程式:____ 。
II.久置的FeSO4溶液。
(3)将上述实验v中的实验操作和现象补充完整____ 。
(4)若要使部分变质的FeSO4复原,发生反应的离子反应方程式是____ 。
(5)小组同学查阅资料得知,“维生素C可将Fe3+转化为Fe2+”。为了验证维生素C的作用,设计了如表实验vi。
由实验vi能否得出“维生素C可将Fe3+转化为Fe2+”的结论?请说明理由____ 。
I.分别取2mL新制的FeSO4溶液于三支试管中,进行如图实验。
 | 实验 | 试剂X | 实验现象 |
| 实验i | 1mL1mol/LNaOH溶液 | 现象a | |
| 实验ii | 5滴酸性KMnO4溶液 | 现象b:紫色褪去 | |
| 实验iii | 依次加入5滴KSCN溶液、5滴氯水 | 现象c |
(2)方案iii的实验现象是
II.久置的FeSO4溶液。
| 实验操作 | 实验现象 | 实验结论 | |
| 实验iv | 取少量久置的FeSO4溶液于试管中,向其中滴加5滴KSCN溶液 | 溶液变红 | FeSO4溶液部分变质 |
| 实验v | |||
(4)若要使部分变质的FeSO4复原,发生反应的离子反应方程式是
(5)小组同学查阅资料得知,“维生素C可将Fe3+转化为Fe2+”。为了验证维生素C的作用,设计了如表实验vi。
| 实验操作 | 实验现象 | |
| 实验vi | 取一定量Fe2(SO4)3溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性KMnO4溶液 | 紫色褪去 |
您最近一年使用:0次
2022-09-01更新
|
510次组卷
|
5卷引用:北京市大兴区2021~2022学年高一上学期期末检测化学试题
5 . 下列有关物质检验的实验结论正确的是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有 |
| B | 向某溶液中加入2滴KSCN溶液,溶液不显红色。 再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有 |
| C | 向某溶液中加入硝酸银溶液,有白色沉淀生成 | 该溶液中一定含有 |
| D | 某溶液的焰色反应呈黄色 | 该溶液一定为钠盐溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-03更新
|
886次组卷
|
6卷引用:北京市汇文中学2021-2022学年高一上学期期末考试化学试卷
名校
解题方法
6 . 用废铁屑制备磁性胶体粒子,制备过程如下:
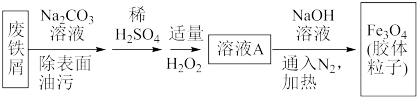
下列说法不正确 的是
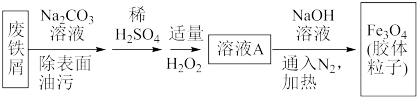
下列说法
| A.加稀H2SO4是为了使铁溶解生成FeSO4 |
| B.通入N2是为了防止空气中的O2氧化Fe2+ |
| C.加适量的H2O2是为了将部分Fe2+氧化为Fe3+ |
| D.溶液A中Fe2+和Fe3+的浓度比为2∶1 |
您最近一年使用:0次
2023-01-07更新
|
411次组卷
|
3卷引用:北京市第八中学2022-2023学年高一上学期期末考试化学试题
7 . 某同学探究Fe2+还原性的实验记录如下:
下列说法错误的是
| ① | ② | ③ |
 | 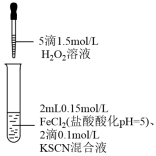 | 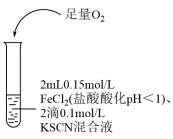 |
溶液变红,大约10秒左右红色褪去,有气体生成(经检验为O2)。取褪色后溶液,滴加盐酸和BaCl2溶液,产生白色沉淀。 | 溶液变红且不褪色,有气体生成(经检验为O2),经检验有丁达尔效应。 | 溶液变红且不褪色,滴加盐酸和BaCl2溶液,无白色沉淀,经检验无丁达尔效应。 |
| A.对比①②,可以判定酸性越强,H2O2的氧化能力越强 |
| B.①中发生的氧化还原反应只有两种 |
| C.②中红色溶液中含有Fe(OH)3胶体 |
| D.③中发生的氧化还原反应为4Fe2++O2+4H+=4Fe3++2H2O |
您最近一年使用:0次
2021-10-09更新
|
1284次组卷
|
11卷引用:北京市海淀区第二十中学2022-2023学年高一上学期11月月考化学试题
北京市海淀区第二十中学2022-2023学年高一上学期11月月考化学试题山东省滨州市2021届高三上学期期末考试化学试题(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(浙江专用)山东省六校(泰安一中、菏泽一中、章丘四中、东营一中、济宁一中、聊城一中、胜利一中)2022届高三“山东学情”10月联考化学试题A卷山东省六校(泰安一中、菏泽一中、章丘四中、东营一中、济宁一中、聊城一中、胜利一中)2022届高三“山东学情”10月联考化学试题B卷(已下线)解密11 化学实验(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)江西省景德镇市第一中学2021-2022学年高二上学期期末(重点班)化学试题湖南省永州市2023届高考第一次适应性考试化学试题湖南省宁远县第一中学2022-2023学年高二上学期第一次适应性考试化学试题(已下线)专题24 实验分析设计型选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
8 . 对某盐溶液进行下列操作,结论正确的是
A.加入少量盐酸溶液,生成白色沉淀,则原溶液中一定有AlO |
B.加入过量盐酸,生成能使澄清石灰水变浑浊的气体,则原溶液中一定有CO |
| C.加入过量新制氯水溶液再加入KSCN溶液,溶液变为红色,则原溶液中一定有Fe2+ |
D.加入过量浓NaOH溶液,微热,生成能使红色石蕊试纸变蓝的气体,则原溶液中一定有NH |
您最近一年使用:0次
名校
9 . 下列物质在生活中的应用与氧化还原反应无关的是
| A.CaO用作衣物防潮剂 |
| B.还原Fe粉用作食品脱氧剂 |
C. 补血剂与维生素C配合使用效果更佳 补血剂与维生素C配合使用效果更佳 |
D.用硅藻土中浸润的 吸收水果散发的乙烯 吸收水果散发的乙烯 |
您最近一年使用:0次
2021-04-09更新
|
1026次组卷
|
9卷引用:北京市海淀区2021届高三一模化学试题
北京市海淀区2021届高三一模化学试题北京市第二十二中学2021-2022学年高三上学期10月月考化学试题福建省厦门英才学校2021届高三4模考试化学试题(已下线)第三章能力提升检测卷-2022年高考化学一轮复习讲练测(已下线)专题05 氧化还原反应-2022年高考化学二轮复习重点专题常考点突破练天津市新华中学2021-2022学年高三下学期 统练2 化学试题进阶训练4天津市宁河区芦台第一中学2022-2023学年高三上学期1月期末考试化学试题陕西省咸阳市武功县普集高级中学2022-2023学年高三上学期11月期中化学试题
名校
解题方法
10 . 某学习小组通过下列装置探究MnO2与FeCl3·6H2O能否反应产生Cl2。
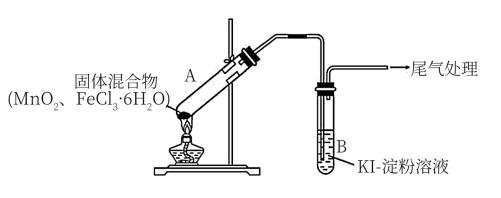
实验操作和现象:
(1)推测现象ⅰ中的白雾中含有的物质是___________ 。
(2)分析现象ⅱ,该小组探究黄色气体的成分,实验如下:
a.加热FeCl3·6H2O,产生白雾和黄色气体。
b.用KSCN溶液检验现象ⅱ和a中的黄色气体,溶液均变红。通过该实验说明现象ⅱ中黄色气体含有___________ 。
(3)除了氯气可使B中溶液变蓝外,推测还可能的原因是:
①实验b检出的气体使之变蓝,反应的离子方程式是___________ 。实验证实推测成立。
②溶液变蓝的另外一种原因是:在酸性条件下,装置中的空气使之变蓝。通过进一步实验确认了这种可能性,其实验方案是___________ 。
(4)为进一步确认黄色气体中是否含有Cl2。
查阅资料:酸性条件下,O2不能氧化Br−。小组同学提出两种方案,均证实了Cl2的存在。
方案1:在A、B间增加盛有某种试剂的洗气瓶C。
方案2:将B中KI—淀粉溶液替换为NaBr溶液;检验Fe2+。
现象如下:
①方案1的C中盛放的试剂是___________ ,其作用是___________ 。
②方案2中检验Fe2+的原因是___________ 。
③综合方案1、2的现象,说明选择NaBr溶液的依据是___________ 。

实验操作和现象:
| 操作 | 现象 |
| 点燃酒精灯,加热 | i.A中部分固体溶解,上方出现白雾 ii.稍后,产生黄色气体,管壁附着黄色液滴 iii.B中溶液变蓝 |
(2)分析现象ⅱ,该小组探究黄色气体的成分,实验如下:
a.加热FeCl3·6H2O,产生白雾和黄色气体。
b.用KSCN溶液检验现象ⅱ和a中的黄色气体,溶液均变红。通过该实验说明现象ⅱ中黄色气体含有
(3)除了氯气可使B中溶液变蓝外,推测还可能的原因是:
①实验b检出的气体使之变蓝,反应的离子方程式是
②溶液变蓝的另外一种原因是:在酸性条件下,装置中的空气使之变蓝。通过进一步实验确认了这种可能性,其实验方案是
(4)为进一步确认黄色气体中是否含有Cl2。
查阅资料:酸性条件下,O2不能氧化Br−。小组同学提出两种方案,均证实了Cl2的存在。
方案1:在A、B间增加盛有某种试剂的洗气瓶C。
方案2:将B中KI—淀粉溶液替换为NaBr溶液;检验Fe2+。
现象如下:
| 方案1 | B中溶液变为蓝色 |
| 方案2 | B中溶液呈浅橙红色;未检出Fe2+ |
②方案2中检验Fe2+的原因是
③综合方案1、2的现象,说明选择NaBr溶液的依据是
您最近一年使用:0次
2021-10-01更新
|
885次组卷
|
4卷引用:北京一零一中学2020-2021学年高一下学期期末考试化学试题
北京一零一中学2020-2021学年高一下学期期末考试化学试题上海行知中学2021-2022学年高二上学期期中考试化学试题(已下线)3.1.2 不同价态铁元素之间的转化-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)山东省临沂第一中学2021-2022学年高一上学期第四次月考化学试题



