名校
1 . 下列离子方程式书写正确的是
A. 溶液中滴加少量稀硫酸: 溶液中滴加少量稀硫酸: |
B. 溶液中滴入 溶液中滴入 溶液: 溶液: |
C.用稀盐酸除去水垢中的 : : |
D.用 溶液刻蚀铜电路板: 溶液刻蚀铜电路板: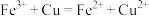 |
您最近一年使用:0次
名校
2 . 下列实验目的、方案设计和现象、结论都正确的是
| 选项 | 实验目的 | 方案设计和现象 | 结论 |
| A | 探究钠在空气中久置后所得固体成分 | 取少量固体,加入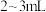 蒸馏水,有气体产生 蒸馏水,有气体产生 | 固体中一定含 |
| B | 比较 、 、 和 和 的氧化性 的氧化性 | 向酸性 溶液中滴入 溶液中滴入 溶液,紫红色溶液变浅并伴有黄绿色气体产生 溶液,紫红色溶液变浅并伴有黄绿色气体产生 | 氧化性: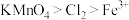 |
| C | 检验某溶液中是否含有 | 取少量待检液于试管中,滴加新制氯水后滴加 溶液,溶液变为红色 溶液,溶液变为红色 | 该溶液含有 |
| D | 验证某固体是 还是 还是 | 室温下取少量固体于试管中,插入温度计,加几滴水,温度升高 | 该固体是 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 下列离子能大量共存,且加入试剂后发生反应的离子方程式正确的是
| 选项 | 离子 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
| A | K+、Fe2+、ClO-、 | 少量CO2 | CO2+2ClO-+H2O= +2HClO +2HClO |
| B | Fe2+、 、 、 | 少量NaHSO4溶液 |  +H+=SO2↑+H2O +H+=SO2↑+H2O |
| C |  、Fe2+、 、Fe2+、 | 少量Ba(OH)2溶液 | 2 + + +Ba2++2OH-=BaSO4↓+2NH3·H2O +Ba2++2OH-=BaSO4↓+2NH3·H2O |
| D | Fe3+、Cl-、 、Cu2+ 、Cu2+ | 少量铁粉 | 2Fe3++Fe=3Fe2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 下列除杂所选用的试剂或方法正确的是
A.除去 溶液中 溶液中 加入过量的 加入过量的 粉,过滤 粉,过滤 |
B.除去 溶液中的少量 溶液中的少量 :加入适量 :加入适量 溶液,过滤 溶液,过滤 |
C.除去 中的少量 中的少量 :通过灼热的铜网,收集气体 :通过灼热的铜网,收集气体 |
D.除去 中的少量 中的少量 :通入饱和食盐水中,洗气 :通入饱和食盐水中,洗气 |
您最近一年使用:0次
5 . 下列相关实验操作、实验现象描述或实验目的表达正确的是
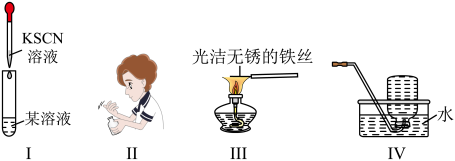
A.图Ⅰ中:证明某溶液中是否含有 | B.图Ⅱ中:闻 的气味 的气味 |
| C.图Ⅲ中:焰色试验检验固体中是否含有钾元素 | D.图Ⅳ中:实验室收集 |
您最近一年使用:0次
2024-01-26更新
|
72次组卷
|
2卷引用:广西钦州市第四中学2023-2024学年高一上学期1月考试化学试卷
名校
6 . 铁是人体不可缺少的微量元素,硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
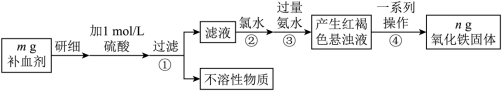
(1)实验中配制480 mL 1 mol/L的硫酸溶液,量取18.4 mol/L的浓硫酸_____ mL。
(2)步骤②加入过量氯水后发生反应的离子方程式为_______ 。
(3)步骤④中一系列操作步骤为______ 、洗涤、灼烧、冷却、称量。
(4)若实验无损耗,则该补血剂含铁元素的质量分数为_______ 。
(5)某同学发现部分补血剂药片表面发黄,取样品研细,溶于1 mol/L的硫酸溶液,过滤。取滤液加________ 溶液(填写化学式),溶液变红说明该补血剂已部分变质。
(6)下列检验(5)中滤液中是否有Fe2+应选用的试剂是___________。

(1)实验中配制480 mL 1 mol/L的硫酸溶液,量取18.4 mol/L的浓硫酸
(2)步骤②加入过量氯水后发生反应的离子方程式为
(3)步骤④中一系列操作步骤为
(4)若实验无损耗,则该补血剂含铁元素的质量分数为
(5)某同学发现部分补血剂药片表面发黄,取样品研细,溶于1 mol/L的硫酸溶液,过滤。取滤液加
(6)下列检验(5)中滤液中是否有Fe2+应选用的试剂是___________。
| A.氯水 | B.酸性KMnO4溶液 | C.铁粉 | D.FeCl3溶液 |
您最近一年使用:0次
解题方法
7 . 室温下,下列各组离子在指定溶液中能大量共存的是
A. 溶液: 溶液: 、 、 、 、 |
B.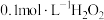 溶液: 溶液: 、 、 、 、 |
C. 溶液: 溶液: 、 、 、 、 |
D. 溶液: 溶液: 、 、 、 、 |
您最近一年使用:0次
8 . 下列关于铁及其化合物的性质与用途均正确且具有对应关系的是
A. 常温下与浓硝酸发生钝化作用,可用铁制容器盛放浓硝酸 常温下与浓硝酸发生钝化作用,可用铁制容器盛放浓硝酸 |
B. 为碱性氧化物,可与水反应生成 为碱性氧化物,可与水反应生成 可用于制作红色涂料 可用于制作红色涂料 |
C. 为紫黑色固体,可用于杀菌消毒 为紫黑色固体,可用于杀菌消毒 |
D. 溶液与 溶液与 溶液反应生成血红色沉淀,可用于检验三价铁离子 溶液反应生成血红色沉淀,可用于检验三价铁离子 |
您最近一年使用:0次
名校
9 . 铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
(1)现有铁和铜的混合物,可以通过______把他们分开。
(2)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式:_______ 。反应后的废液中含有Fe3+,可以用______ 检验。
(3)现将反应后的废液采用以下流程进行回收再生,根据流程图完成下列填空。
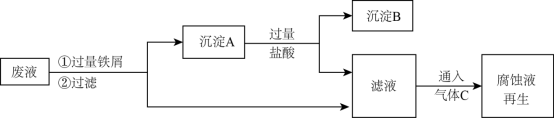
沉淀A中含有的单质:______ ,黄绿色气体C可以把滤液转化成FeCl3腐蚀液,写出反应过程中的离子方程式_______ 。
(4)取“滤液”少许于试管中,然后滴加氢氧化钠溶液,产生白色沉淀,______ (补全实验现象),此过程涉及氧化还原反应的化学方程式是_______ 。
(5)把铁皮插入到的硫酸铜和硫酸的混合溶液中,一段后取出,溶液的质量不变,则参加反应的H+与Cu2+物质的量之比为:______ 。
(1)现有铁和铜的混合物,可以通过______把他们分开。
| A.盐酸 | B.Fe3O4 | C.稀硝酸 | D.Fe2O3 |
(3)现将反应后的废液采用以下流程进行回收再生,根据流程图完成下列填空。

沉淀A中含有的单质:
(4)取“滤液”少许于试管中,然后滴加氢氧化钠溶液,产生白色沉淀,
(5)把铁皮插入到的硫酸铜和硫酸的混合溶液中,一段后取出,溶液的质量不变,则参加反应的H+与Cu2+物质的量之比为:
您最近一年使用:0次
名校
10 . 下列有关“实验操作”、“现象”及“实验结论”都正确的是
| 选项 | 实验操作 | 现象 | 实验结论 |
| A | 取少量某溶液,滴加 溶液 溶液 | 产生白色沉淀 | 说明溶液中含 |
| B | 用足量的盐酸溶解铁与水蒸气反应后的固体,再向溶液中滴加 溶液 溶液 | 溶液不变红 | 铁与水蒸气反应生成的产物中不含 价的铁 价的铁 |
| C | 取氯化镁和氯化铝溶液于两支试管,分别向其中加入过量的氢氧化钠溶液, | 观察到氯化镁的试管中出现白色沉淀,氯化铝的试管中先出现白色沉淀,后溶解 | 说明镁的金属性强于铝 |
| D | 将湿润的有色布条放入充满氯气的集气瓶中 | 布条褪色 | 氯气具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-20更新
|
209次组卷
|
4卷引用: 浙江省湖州市第二中学2023-2024学年高一上学期12月月考化学试题
浙江省湖州市第二中学2023-2024学年高一上学期12月月考化学试题 (已下线)专题01 硫及其化合物(考点清单)(讲+练)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)安徽省桐城中学2023-2024学年高一下学期开学检测化学试题浙江省淳安县汾口中学2023-2024学年高一上学期期末模拟(1月月考)化学试题



