名校
解题方法
1 . 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向X溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,溶液变为红色 | X溶液中一定含有Fe2+ |
| B | 向3mL KI溶液中滴加几滴溴水,振荡,再滴加1mL淀粉溶液,溶液显蓝色 | Br2的氧化性比I2强 |
| C | 向浓度均为0.05mol·L-1的NaI、NaCl混合溶液中滴加少量AgNO3溶液,有黄色沉淀生成 | Ksp(AgI)> Ksp(AgCl) |
| D | 用pH试纸测得:CH3COONa溶液的pH约为9,NaNO2溶液的pH约为8 | HNO2电离出H+的能力比CH3COOH强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 下列物质的实验中不能 达到实验目的的是
选项 | 实验目的 | 实验方法 |
A | 除去CO2中的SO2 | 通过酸性高锰酸钾溶液 |
B | 检验FeCl2溶液是否被氧化 | 取少量液体滴加KSCN溶液 |
C | 检验淀粉是否水解 | 先加氢氧化钠溶液,再加新制氢氧化铜悬浊液煮沸 |
D | 除去FeCl3溶液中的FeCl2 | 加入足量的铁屑后过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 工业上制一元弱酸——硼酸( )常采用硼镁矿(含
)常采用硼镁矿(含 、
、 及少量
及少量 、
、 经
经 溶液溶浸后通过一系列反应制得。下列有关反应及离子方程式均正确的是
溶液溶浸后通过一系列反应制得。下列有关反应及离子方程式均正确的是
 )常采用硼镁矿(含
)常采用硼镁矿(含 、
、 及少量
及少量 、
、 经
经 溶液溶浸后通过一系列反应制得。下列有关反应及离子方程式均正确的是
溶液溶浸后通过一系列反应制得。下列有关反应及离子方程式均正确的是A.已知硼酸是一元弱酸,其电离方程式为: |
B.用KSCN溶液检验溶浸后溶液是否含有 : : |
C. 溶于 溶于 溶液: 溶液: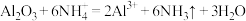 |
D. 溶于 溶于 溶液: 溶液: |
您最近一年使用:0次
名校
4 . 由下列实验操作及现象所得结论或解释正确的是
| 选项 | 实验操作 | 现象 | 结论或解释 |
| A | 向5mL0.1mol·L-1KI溶液中加入10mL0.01mol·L-1FeCl3溶液,充分反应后滴加KSCN溶液 | 溶液变红 | I-与Fe3+的反应是可逆反应 |
| B | 常温下,测定等浓度NaHCO3溶液和NaHSO3溶液的pH | 前者大于后者 | 非金属性S>C |
| C | 将某溶液滴在KI一淀粉试纸上 | 试纸变蓝 | 原溶液中一定含有Cl2 |
| D | 向蛋白质溶液中加入醋酸铅溶液 | 产生白色沉淀 | 蛋白质发生了盐析 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-04更新
|
360次组卷
|
4卷引用:宁夏吴忠市2023届高考模拟联考理科综合化学试题
宁夏吴忠市2023届高考模拟联考理科综合化学试题2024届甘肃省平凉市静宁县高三第四次摸底考试模拟预测化学试题(已下线)考点巩固卷12 化学实验基础(一)(3大考点67题)-2024年高考化学一轮复习考点通关卷(新高考通用)新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高三上学期12月月考化学试卷
解题方法
5 . 下列由实验现象所得结论错误的是
| A.向5mL0.2mol/L的FeCl3溶液中加入几滴同浓度的KI溶液,再加入几滴KSCN溶液,溶液显血红色,则FeCl3与KI的反应是可逆反应 |
| B.二氧化硅虽然能与氢氧化钠、氢氟酸反应,但它不是两性氧化物 |
| C.将淀粉与稀硫酸混合,加热一段时间后,取冷却后少量溶液加入适量NaOH溶液调至弱碱性,再加入银氨溶液水浴加热,试管壁上出现光亮镜面,蔗糖发生了水解反应。 |
| D.向NaClO溶液中滴加酚酞试剂,先变红后褪色,可以证明NaClO在溶液中发生了水解反应 |
您最近一年使用:0次
6 . 化学与日常生活息息相关,下列说法错误的是
| A.食醋除去水垢中的碳酸钙 | B.乙二醇可用于生产汽车防冻液 |
| C.纯铁器皿比生铁器皿更容易锈蚀 | D.氯化铁用于电子元件的五金蚀刻 |
您最近一年使用:0次
7 . 有一种优良的磁性合金材料,经查阅相关资料得知:主要成分是Al—Cu—Mg—Fe—Si合金……。现取几小块合金碎片,进行如下探究性实验,其中现象、结论均正确的是
| 选项 | 实验方案 | 现象 | 结论 |
| A | 加入过量盐酸充分反应 | 有少量固体不溶 | 含有金属铜 |
| B | 加入过量NaOH溶液充分反应 | 有无色气体产生 | 含有金属铝 |
| C | 加入盐酸溶解后,取上层清液,滴入少许NaOH溶液 | 产生白色沉淀 | 含有金属镁 |
| D | 加入稀硝酸溶解后,取上层清液,加入KSCN溶液 | 溶液呈红色 | 含有铁元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-05-18更新
|
294次组卷
|
3卷引用:宁夏银川一中等17校2021届高三下学期5月联考理综化学试题
8 . 甘氨酸亚铁[(NH2CH2COO)2Fe]是一种补铁强化剂。某学习小组利用FeCO3与甘氨酸(NH2CH2COOH)制备甘氨酸亚铁,实验装置如图所示。

有关物质性质如下表
实验过程:
I.合成:装置C中盛有31.8 g FeCO3和200 mL 2.0 mol·L-1甘氨酸溶液和适量柠檬酸。实验时,先打开仪器a的活塞,待装置C中空气排净后,加热并不断搅拌,并通过仪器b向C中加入适量氢氧化钠溶液调节pH到6左右,使反应物充分反应。
II.分离:反应结束后,过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
回答下列问题:
(1)装置B盛装的试剂为___________ ;仪器b比a的优点是___________ 。
(2)若想证明C装置中空气排净,则D中通常盛装的试剂为___________ 。
(3)合成过程加入柠檬酸的作用是促进FeCO3溶解和___________ 。
(4)加入氢氧化钠溶液调节pH若大于6,甘氨酸亚铁产量下降。原因可用离子方程式表示为___________ 。
(5)检验产品中是否含有Fe3+的最佳试剂是___________ 。
(6)本实验制得24.5 g甘氨酸亚铁,则其产率是___________ %。

有关物质性质如下表
| 甘氨酸 | 柠檬酸 | 甘氨酸亚铁 |
| 易溶于水,微溶于乙醇 | 易溶于水和乙醇 | 易溶于水,难溶于乙醇 |
| 两性化合物 | 强酸性、强还原性 |
I.合成:装置C中盛有31.8 g FeCO3和200 mL 2.0 mol·L-1甘氨酸溶液和适量柠檬酸。实验时,先打开仪器a的活塞,待装置C中空气排净后,加热并不断搅拌,并通过仪器b向C中加入适量氢氧化钠溶液调节pH到6左右,使反应物充分反应。
II.分离:反应结束后,过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
回答下列问题:
(1)装置B盛装的试剂为
(2)若想证明C装置中空气排净,则D中通常盛装的试剂为
(3)合成过程加入柠檬酸的作用是促进FeCO3溶解和
(4)加入氢氧化钠溶液调节pH若大于6,甘氨酸亚铁产量下降。原因可用离子方程式表示为
(5)检验产品中是否含有Fe3+的最佳试剂是
(6)本实验制得24.5 g甘氨酸亚铁,则其产率是
您最近一年使用:0次
解题方法
9 . 硫酸镍(NiSO4)主要用于电镀工业,是电镀镍和化学镍的主要镍盐。某矿渣的主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,从该矿渣中回收NiSO4的工艺流程如下:

(1)“焙烧”时发生多个反应,其中NiFe2O4生成NiSO4、Fe2(SO4)3,发生该反应的化学方程式为___________ 。
(2)“浸泡”时用“95℃热水”的目的是___________ ,“浸泡”过程中Fe2(SO4)3生成FeO(OH)的离子方程式为___________ 。
(3)“浸渣”的成分除Fe2O3、FeO(OH)外还含有___________ (填化学式),为检验浸出液中是否含有Fe3+,可选用的化学试剂是___________ 。
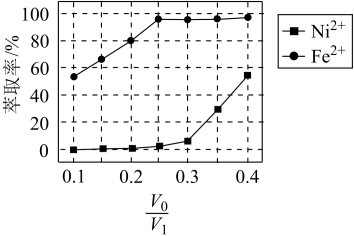
(4)“萃取"过程中发生反应Fe2+(水相)+2RH(有机相) FeR(有机相)+2H+(水相)。萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如下图所示,V0/VA的最佳取值为
FeR(有机相)+2H+(水相)。萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如下图所示,V0/VA的最佳取值为___________ ;在___________ (填“强碱性”“强酸性”或“中性”)介质中“反萃取”能使有机相再生而循环利用。

(1)“焙烧”时发生多个反应,其中NiFe2O4生成NiSO4、Fe2(SO4)3,发生该反应的化学方程式为
(2)“浸泡”时用“95℃热水”的目的是
(3)“浸渣”的成分除Fe2O3、FeO(OH)外还含有
(4)“萃取"过程中发生反应Fe2+(水相)+2RH(有机相)
 FeR(有机相)+2H+(水相)。萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如下图所示,V0/VA的最佳取值为
FeR(有机相)+2H+(水相)。萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如下图所示,V0/VA的最佳取值为
您最近一年使用:0次
名校
解题方法
10 . 下列反应的离子方程式正确的是
| A.Fe2O3溶于HI溶液中:Fe2O3 + 6H+ = 2Fe3+ + 3H2O |
B.向饱和苯酚钠溶液中通入少量CO2:C6H5O- + CO2 + H2O = C6H5OH↓+HCO |
C.用足量NaOH浓溶液吸收NO2尾气:3NO2+2OH-=2NO +NO↑+H2O +NO↑+H2O |
| D.Cl2与热的NaOH溶液反应制取NaClO3:Cl2 +2OH- = Cl- + ClO- + 2H2O |
您最近一年使用:0次



