1 . 分析以下几个反应(未配平),填空:
①Fe2++Zn→Zn2++Fe
②Fe2++Cl2→Fe3++Cl—
③Fe3++Fe→Fe2+
(1)Fe2+体现氧化性的是___________ (填反应的序号)。
(2)写出反应①对应的一个化学反应方程式___________ 。
(3)反应②中每1molCl2完全反应转移电子为___________ mol。
(4)对反应③进行配平,并用单线桥标注电子转移的方向和数目。______
___________Fe3++___________Fe=___________Fe2+
①Fe2++Zn→Zn2++Fe
②Fe2++Cl2→Fe3++Cl—
③Fe3++Fe→Fe2+
(1)Fe2+体现氧化性的是
(2)写出反应①对应的一个化学反应方程式
(3)反应②中每1molCl2完全反应转移电子为
(4)对反应③进行配平,并用单线桥标注电子转移的方向和数目。
___________Fe3++___________Fe=___________Fe2+
您最近一年使用:0次
解题方法
2 . 把铁片放入下列溶液中,铁片溶解,溶液质量增加的是
| A.Na2SO4溶液 | B.CuSO4溶液 | C.AgNO3溶液 | D.Fe2(SO4)3溶液 |
您最近一年使用:0次
2024-01-23更新
|
50次组卷
|
2卷引用:湖南省邵阳市2023-2024学年高一上学期1月期末联考化学试题
名校
解题方法
3 . 如图为铁元素的价类二维图,“→”表示物质间的转化关系。下列说法正确的是
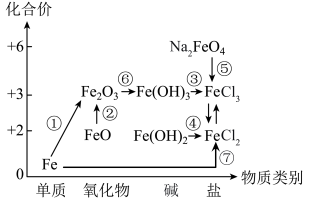

| A.红热的铁与水蒸气反应可实现①的转化 |
| B.FeO在空气中受热进行转化② |
| C.转化⑦的反应类型可以是化合反应 |
D. 溶于稀硝酸可实现转化④ 溶于稀硝酸可实现转化④ |
您最近一年使用:0次
名校
解题方法
4 . 5.76g某部分氧化的Fe、Cu合金样品(氧化产物为 、CuO),经如下处理,下列说法正确的是
、CuO),经如下处理,下列说法正确的是

 、CuO),经如下处理,下列说法正确的是
、CuO),经如下处理,下列说法正确的是
| A.V=448 |
| B.样品中Fe元素的质量为2.14g |
| C.未氧化前Fe元素的质量分数约为38.89% |
| D.样品中CuO的质量为3.52g |
您最近一年使用:0次
名校
解题方法
5 . 下列离子方程式书写不正确的是
A.铁与氯化铁溶液反应: |
B.钠与水反应: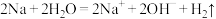 |
C.氯气与水反应: |
D.碳酸氢钠溶液与稀盐酸反应: |
您最近一年使用:0次
名校
6 . 利用废旧铁铜粉可以制备补血剂原料碳酸亚铁和杀菌剂胆矾。流程如下图所示:
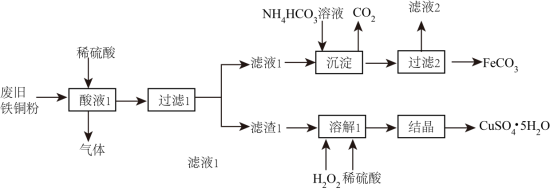
回答下列问题:
(1)“滤液1”中一定含有的金属阳离子___________ (填离子符号),写出检验该金属阳离子的方法___________ 。
(2)过滤用到的玻璃仪器是___________ 。
(3)“溶解1”过程温度不宜过高的原因是___________ 。
(4)向纯净的碳酸亚铁固体中加入足量乳酸溶液,在70℃下搅拌使其充分反应,可得到补铁剂乳酸亚铁。为防止乳酸亚铁变质,在反应体系中应加入少量铁粉,用离子方程式解释使用铁粉的原因___________ 。
(5)“结晶”的具体操作是___________ ,冷却结晶,过滤,洗涤,干燥。
(6)向 固体中加入蒸馏水,固体未见明显减少;一段时间后,难溶物上方出现红褐色氢氧化物并有气泡产生。试写出所发生的化学方程式
固体中加入蒸馏水,固体未见明显减少;一段时间后,难溶物上方出现红褐色氢氧化物并有气泡产生。试写出所发生的化学方程式___________ 。

回答下列问题:
(1)“滤液1”中一定含有的金属阳离子
(2)过滤用到的玻璃仪器是
(3)“溶解1”过程温度不宜过高的原因是
(4)向纯净的碳酸亚铁固体中加入足量乳酸溶液,在70℃下搅拌使其充分反应,可得到补铁剂乳酸亚铁。为防止乳酸亚铁变质,在反应体系中应加入少量铁粉,用离子方程式解释使用铁粉的原因
(5)“结晶”的具体操作是
(6)向
 固体中加入蒸馏水,固体未见明显减少;一段时间后,难溶物上方出现红褐色氢氧化物并有气泡产生。试写出所发生的化学方程式
固体中加入蒸馏水,固体未见明显减少;一段时间后,难溶物上方出现红褐色氢氧化物并有气泡产生。试写出所发生的化学方程式
您最近一年使用:0次
名校
7 . 下列表示对应化学反应的离子方程式正确的是
A.铝表面的保护膜与NaOH溶液反应: |
B.向氯化铁溶液中加入铁粉: |
C. 粉末与水反应: 粉末与水反应: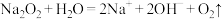 |
D. 溶于稀硝酸: 溶于稀硝酸: |
您最近一年使用:0次
2024-01-18更新
|
132次组卷
|
3卷引用:云南省红河哈尼族彝族自治州2023-2024学年高一上学期1月期末化学试题
名校
解题方法
8 . 现将有铜的印刷线路板浸入120mL氯化铁浓溶液中,有9.6g铜被腐蚀掉。取出印刷线路板,向溶液中加入8.4g铁粉,经充分反应,溶液中还存在4.8g不溶解的物质。(设溶液体积不变,且不考虑金属离子水解)。请回答下列问题:
(1)充分反应后,溶液中存在4.8g不溶物的成分为___________ (用化学式表示)。
(2)充分反应后溶液中一定不存在的金属离子为___________ 。
(3)比较 、
、 、
、 的氧化性大小:
的氧化性大小:___________ 。
(4)试计算最后溶液中 离子的物质的量浓度
离子的物质的量浓度___________ mol/L。
(1)充分反应后,溶液中存在4.8g不溶物的成分为
(2)充分反应后溶液中一定不存在的金属离子为
(3)比较
 、
、 、
、 的氧化性大小:
的氧化性大小:(4)试计算最后溶液中
 离子的物质的量浓度
离子的物质的量浓度
您最近一年使用:0次
名校
9 . 下列除去杂质的方法中,正确的是
| 选项 | 物质 | 杂质 | 除去杂质的方法 |
| A |  溶液 溶液 |  | 加入足量的铁粉、过滤 |
| B |  |  | 通入过量 、点燃 、点燃 |
| C |  溶液 溶液 |  | 加入足量的钢粉、过滤 |
| D |  固体 固体 |  | 加入足量 溶液、过滤、洗涤、干燥 溶液、过滤、洗涤、干燥 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . Ⅰ.钠、铝、铁是三种重要的金属,它们的单质及其化合物在生活生产中有重要的作用。请回答下列问题:
(1)钠着火不能用二氧化碳来灭火,已知钠在足量二氧化碳中燃烧生成炭黑和一种白色固体。根据实验现象写出方程式:_______ ,该反应中氧化剂和还原剂的物质的量之比为______ 。
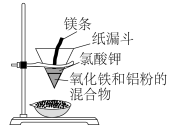
Ⅱ.一些活泼金属也可作还原剂,将相对不活泼的金属从其化合物中置换出来。例如“铝热反应”的原理是: 。其反应装置如下图所示,已知镁条与氯酸钾反应产生高温可引发“铝热反应”。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入装有沙子的蒸发皿中”。由化学手册查阅得有关物质的熔、沸点数据如下表。
。其反应装置如下图所示,已知镁条与氯酸钾反应产生高温可引发“铝热反应”。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入装有沙子的蒸发皿中”。由化学手册查阅得有关物质的熔、沸点数据如下表。
(2)该同学推测,铝热反应所得到的熔融物可能是铁铝合金。理由是该反应放出的热量使铁熔化,而铝的熔点比铁的低,此时液态的铁和铝熔合成铁铝合金,设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是_____ (填化学式),该试剂与金属铝反应的离子方程式为_______ 。
(3)另一同学推测铝热反应得到的熔融物中还含有 ,他设计了如下方案来验证熔融物是否有
,他设计了如下方案来验证熔融物是否有 剩余:取一块该熔融物冷却后投入到稍过量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察到溶液颜色未变红,证明该熔融物中不含有
剩余:取一块该熔融物冷却后投入到稍过量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察到溶液颜色未变红,证明该熔融物中不含有 。则物质甲是
。则物质甲是_______ (填化学式)。该同学的实验方案是否合理?______ (填“合理”或“不合理”)。理由:_______ (用离子方程式说明)。
(1)钠着火不能用二氧化碳来灭火,已知钠在足量二氧化碳中燃烧生成炭黑和一种白色固体。根据实验现象写出方程式:
Ⅱ.一些活泼金属也可作还原剂,将相对不活泼的金属从其化合物中置换出来。例如“铝热反应”的原理是:
 。其反应装置如下图所示,已知镁条与氯酸钾反应产生高温可引发“铝热反应”。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入装有沙子的蒸发皿中”。由化学手册查阅得有关物质的熔、沸点数据如下表。
。其反应装置如下图所示,已知镁条与氯酸钾反应产生高温可引发“铝热反应”。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入装有沙子的蒸发皿中”。由化学手册查阅得有关物质的熔、沸点数据如下表。
| 物质 | Al |  | Fe |  |
| 熔点/℃ | 660 | 2054 | 1535 | 1460 |
| 沸点/℃ | 2467 | 2980 | 2750 |
(2)该同学推测,铝热反应所得到的熔融物可能是铁铝合金。理由是该反应放出的热量使铁熔化,而铝的熔点比铁的低,此时液态的铁和铝熔合成铁铝合金,设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是
(3)另一同学推测铝热反应得到的熔融物中还含有
 ,他设计了如下方案来验证熔融物是否有
,他设计了如下方案来验证熔融物是否有 剩余:取一块该熔融物冷却后投入到稍过量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察到溶液颜色未变红,证明该熔融物中不含有
剩余:取一块该熔融物冷却后投入到稍过量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察到溶液颜色未变红,证明该熔融物中不含有 。则物质甲是
。则物质甲是
您最近一年使用:0次
2024-01-14更新
|
172次组卷
|
2卷引用:辽宁省部分高中2023-2024学年高一上学期期末考试高化学试题



