解题方法
1 . 富脂食品密封保存往往需要在包装袋内装一小包脱氧剂(有效成分是还原铁粉),某小组为探究脱氧剂中铁粉是否变质,取少量样品溶于稀盐酸,再进行下列实验,下列有关实验现象和结论的说法错误的是
| A.若加盐酸时有气体产生,不能证明脱氧剂未变质 |
| B.若滴加KSCN溶液,无明显变化,再滴加氯水显血红色,则证明脱氧剂未变质 |
| C.若滴加KSCN溶液,溶液显血红色,则证明脱氧剂已变质 |
| D.若加入铜粉充分反应后,溶液呈蓝色,则证明脱氧剂已变质 |
您最近一年使用:0次
2 . Ⅰ.钠、铝、铁是三种重要的金属,它们的单质及其化合物在生活生产中有重要的作用。请回答下列问题:
(1)钠着火不能用二氧化碳来灭火,已知钠在足量二氧化碳中燃烧生成炭黑和一种白色固体。根据实验现象写出方程式:_______ ,该反应中氧化剂和还原剂的物质的量之比为______ 。
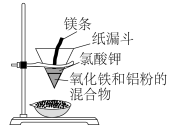
Ⅱ.一些活泼金属也可作还原剂,将相对不活泼的金属从其化合物中置换出来。例如“铝热反应”的原理是: 。其反应装置如下图所示,已知镁条与氯酸钾反应产生高温可引发“铝热反应”。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入装有沙子的蒸发皿中”。由化学手册查阅得有关物质的熔、沸点数据如下表。
。其反应装置如下图所示,已知镁条与氯酸钾反应产生高温可引发“铝热反应”。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入装有沙子的蒸发皿中”。由化学手册查阅得有关物质的熔、沸点数据如下表。
(2)该同学推测,铝热反应所得到的熔融物可能是铁铝合金。理由是该反应放出的热量使铁熔化,而铝的熔点比铁的低,此时液态的铁和铝熔合成铁铝合金,设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是_____ (填化学式),该试剂与金属铝反应的离子方程式为_______ 。
(3)另一同学推测铝热反应得到的熔融物中还含有 ,他设计了如下方案来验证熔融物是否有
,他设计了如下方案来验证熔融物是否有 剩余:取一块该熔融物冷却后投入到稍过量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察到溶液颜色未变红,证明该熔融物中不含有
剩余:取一块该熔融物冷却后投入到稍过量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察到溶液颜色未变红,证明该熔融物中不含有 。则物质甲是
。则物质甲是_______ (填化学式)。该同学的实验方案是否合理?______ (填“合理”或“不合理”)。理由:_______ (用离子方程式说明)。
(1)钠着火不能用二氧化碳来灭火,已知钠在足量二氧化碳中燃烧生成炭黑和一种白色固体。根据实验现象写出方程式:
Ⅱ.一些活泼金属也可作还原剂,将相对不活泼的金属从其化合物中置换出来。例如“铝热反应”的原理是:
 。其反应装置如下图所示,已知镁条与氯酸钾反应产生高温可引发“铝热反应”。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入装有沙子的蒸发皿中”。由化学手册查阅得有关物质的熔、沸点数据如下表。
。其反应装置如下图所示,已知镁条与氯酸钾反应产生高温可引发“铝热反应”。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入装有沙子的蒸发皿中”。由化学手册查阅得有关物质的熔、沸点数据如下表。
| 物质 | Al |  | Fe |  |
| 熔点/℃ | 660 | 2054 | 1535 | 1460 |
| 沸点/℃ | 2467 | 2980 | 2750 |
(2)该同学推测,铝热反应所得到的熔融物可能是铁铝合金。理由是该反应放出的热量使铁熔化,而铝的熔点比铁的低,此时液态的铁和铝熔合成铁铝合金,设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是
(3)另一同学推测铝热反应得到的熔融物中还含有
 ,他设计了如下方案来验证熔融物是否有
,他设计了如下方案来验证熔融物是否有 剩余:取一块该熔融物冷却后投入到稍过量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察到溶液颜色未变红,证明该熔融物中不含有
剩余:取一块该熔融物冷却后投入到稍过量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察到溶液颜色未变红,证明该熔融物中不含有 。则物质甲是
。则物质甲是
您最近一年使用:0次
2024-01-14更新
|
168次组卷
|
2卷引用:辽宁省部分高中2023-2024学年高一上学期期末考试高化学试题
名校
3 . 某化学兴趣小组利用废铁屑(含少量 )制备还原性铁粉,从而达到资源回收利用的目的,制备流程如图所示。
)制备还原性铁粉,从而达到资源回收利用的目的,制备流程如图所示。

请回答下列问题:
(1)“酸溶”时,搅拌的目的是_______ 。
(2)“操作Y”为_______ (填操作名称),经过“操作Y”得到了滤渣 ,则物质X可用于除去过量的稀硫酸和防止
,则物质X可用于除去过量的稀硫酸和防止 被氧化,可选择
被氧化,可选择_______ (填试剂名称),“转化2”发生反应的离子方程式为_______ 。
(3)“洗涤”时,能证明滤渣洗涤干净的操作及现象为_______ 。
(4)麦片中常添加微量还原性铁粉,用于补充入体所需的铁元素,这些铁粉在胃酸(主要成分为盐酸)的作用下发生反应变成人体容易吸收的铁元素,发生反应的化学方程式为_______ ;人体补铁时,同时服用维生素C能促进亚铁离子被吸收,说明维生素C具有_______ (填“氧化性”或“还原性”)。
 )制备还原性铁粉,从而达到资源回收利用的目的,制备流程如图所示。
)制备还原性铁粉,从而达到资源回收利用的目的,制备流程如图所示。
请回答下列问题:
(1)“酸溶”时,搅拌的目的是
(2)“操作Y”为
 ,则物质X可用于除去过量的稀硫酸和防止
,则物质X可用于除去过量的稀硫酸和防止 被氧化,可选择
被氧化,可选择(3)“洗涤”时,能证明滤渣洗涤干净的操作及现象为
(4)麦片中常添加微量还原性铁粉,用于补充入体所需的铁元素,这些铁粉在胃酸(主要成分为盐酸)的作用下发生反应变成人体容易吸收的铁元素,发生反应的化学方程式为
您最近一年使用:0次
2022-12-07更新
|
228次组卷
|
4卷引用:云南省楚雄彝族自治州2022-2023学年高一上学期期末教育学业质量监测化学试题
云南省楚雄彝族自治州2022-2023学年高一上学期期末教育学业质量监测化学试题四川省成都市四校2022-2023学年高一上学期12月联考化学试题四川省眉山市彭山区第一中学2022-2023学年高一上学期第二次模拟选科调考化学试题(已下线)第13讲 铁和铁的氧化物-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)
名校
解题方法
4 . 为不断满足人民群众对美好生活的需要,水资源保护已经成为我国生态建设的重要领域。水处理技术的目的在于使废水经过技术处理后达到再次使用或者排放的水质要求,被广泛应用于工业、农业、环保、餐饮等各个行业,与人们的日常生活密切相关。经检测,某工厂的酸性废水中所含离子及其浓度如下表所示:
回答下列问题:
Ⅰ.
(1)该工业废水中
___________  。
。
Ⅱ.为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾( )。
)。
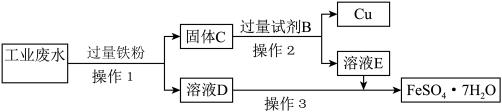
(2)在实验室完成操作1,需用到的玻璃仪器除烧杯、玻璃棒外,还有___________ 。
(3)工业废水中加入铁粉后,反应的离子方程式为 、
、___________ 、___________ 。
(4)试剂B是___________ 。
(5)操作3是蒸发浓缩、___________ 、过滤,最后用少量冷水洗涤晶体,在低温下干燥。
(6)证明溶液E中只含有 而不含
而不含 的实验方法:取少量溶液E于试管中,
的实验方法:取少量溶液E于试管中,___________ (填字母)。
a.先加氯水,再加KSCN溶液后显红色
b.先加KSCN溶液,不显红色,再加氯水后显红色
c.滴加NaOH溶液,只产生白色沉淀,且白色沉淀迅速变为灰绿色,最后呈红褐色
| 离子 |  |  |  |  |  |
浓度/( ) ) |  | 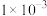 | 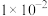 |  |
Ⅰ.
(1)该工业废水中

 。
。Ⅱ.为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾(
 )。
)。
(2)在实验室完成操作1,需用到的玻璃仪器除烧杯、玻璃棒外,还有
(3)工业废水中加入铁粉后,反应的离子方程式为
 、
、(4)试剂B是
(5)操作3是蒸发浓缩、
(6)证明溶液E中只含有
 而不含
而不含 的实验方法:取少量溶液E于试管中,
的实验方法:取少量溶液E于试管中,a.先加氯水,再加KSCN溶液后显红色
b.先加KSCN溶液,不显红色,再加氯水后显红色
c.滴加NaOH溶液,只产生白色沉淀,且白色沉淀迅速变为灰绿色,最后呈红褐色
您最近一年使用:0次
2023-04-23更新
|
257次组卷
|
2卷引用:贵州省铜仁市2022-2023学年高一上学期期末考试化学试题
名校
解题方法
5 . 高铁酸钠(Na2FeO4)是一种多功能绿色水处理剂,杀菌消毒的同时可生成氢氧化铁胶体。某工厂利用废金属屑(主要成分为Fe和Cu,含有少量Fe2O3)制取Na2FeO4并回收金属Cu,工艺流程如下:
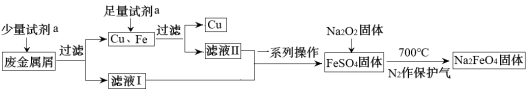
(1)试剂a为___________ (填化学式)。
(2)证明滤液I中无Fe3+的实验方法是___________ ;用离子方程式解释滤液I不含有Fe3+可能的原因___________ 。
(3)流程中Na2O2不可暴露在空气中时间过长,原因是___________ (用化学方程式表示)。
(4)制备Na2FeO4的原理:2FeSO4+6Na2O2 2Na2FeO4+2Na2O+2Na2SO4+O2↑。反应中
2Na2FeO4+2Na2O+2Na2SO4+O2↑。反应中___________ 作还原剂;每生成1mol Na2FeO4转移的电子数为___________ 。
(5)Na2FeO4净水过程中所发生的化学反应主要为:▢Na2FeO4+▢H2O→▢Fe(OH)3(胶体)+▢NaOH+▢X↑,请推测X的化学式为____________ ,配平该化学方程式,化学计量数从左至右分别为___________ 。
(6)用Na2FeO4代替Cl2处理饮用水的优点是___________ (只答一条即可)。

(1)试剂a为
(2)证明滤液I中无Fe3+的实验方法是
(3)流程中Na2O2不可暴露在空气中时间过长,原因是
(4)制备Na2FeO4的原理:2FeSO4+6Na2O2
 2Na2FeO4+2Na2O+2Na2SO4+O2↑。反应中
2Na2FeO4+2Na2O+2Na2SO4+O2↑。反应中(5)Na2FeO4净水过程中所发生的化学反应主要为:▢Na2FeO4+▢H2O→▢Fe(OH)3(胶体)+▢NaOH+▢X↑,请推测X的化学式为
(6)用Na2FeO4代替Cl2处理饮用水的优点是
您最近一年使用:0次
名校
6 . 下列实验内容可以达到预期实验目的的是
| 选项 | 实验内容 | 实验目的 |
| A | 将1 mol 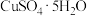 溶解在1 L水中 溶解在1 L水中 | 配制1  的 的 溶液 溶液 |
| B | 将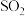 通入酸性 通入酸性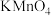 溶液中 溶液中 | 证明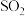 具有漂白性 具有漂白性 |
| C | 加入足量铁屑,充分反应后,过滤 | 除去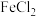 溶液中的少量 溶液中的少量 |
| D | 将木炭与浓硫酸共热,得到的气体通入澄清石灰水 | 检验木炭的氧化产物是 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-16更新
|
239次组卷
|
2卷引用:山东省青岛第二中学2023届高三上学期1月期末考试化学试题
7 . (1)利用原电池装置可以验证Fe3+与Cu2+氧化性相对强弱,如图所示。写出该氧化还原反应的离子方程式:___________ 。该装置中的负极材料是___________ (填化学式),正极反应式是___________ 。

(2)某研究性学习小组为证明 为可逆反应,设计如下两种方案(已知:酸性溶液中Fe2+易被空气氧化为Fe3+)。
为可逆反应,设计如下两种方案(已知:酸性溶液中Fe2+易被空气氧化为Fe3+)。
方案一:取5mL0.1mol/LKI溶液,滴加2mL0.1mol/L的FeCl3溶液,滴入5滴稀盐酸,再继续加入2mLCCl4,充分振荡、静置、分层,取上层清液,滴加KSCN溶液,现象是___________ ,即可证明该反应为可逆反应。你认为此方案___________ (“不严密”或“严密”),理由是___________ (用离子方程式表示)。
方案二:设计如图原电池装置,接通灵敏电流计,指针向右偏转,随着反应时间进行;电流计读数逐渐变小,最后读数变为零。当指针读数变零后,在右边的池了中加入1mol/L FeCl2溶液,灵敏电流计指针向左偏转,即可证明该反应为可逆反应。你认为灵敏电流计“读数变为零”的原因是___________ 。


(2)某研究性学习小组为证明
 为可逆反应,设计如下两种方案(已知:酸性溶液中Fe2+易被空气氧化为Fe3+)。
为可逆反应,设计如下两种方案(已知:酸性溶液中Fe2+易被空气氧化为Fe3+)。方案一:取5mL0.1mol/LKI溶液,滴加2mL0.1mol/L的FeCl3溶液,滴入5滴稀盐酸,再继续加入2mLCCl4,充分振荡、静置、分层,取上层清液,滴加KSCN溶液,现象是
方案二:设计如图原电池装置,接通灵敏电流计,指针向右偏转,随着反应时间进行;电流计读数逐渐变小,最后读数变为零。当指针读数变零后,在右边的池了中加入1mol/L FeCl2溶液,灵敏电流计指针向左偏转,即可证明该反应为可逆反应。你认为灵敏电流计“读数变为零”的原因是

您最近一年使用:0次
解题方法
8 . 某工厂废水中含大量 和少量的
和少量的 、
、 、
、 ,为减少污染变废为宝,实验小组设计了如图方案(其中每步加入试剂均过量):
,为减少污染变废为宝,实验小组设计了如图方案(其中每步加入试剂均过量):

(1)“试剂Ⅱ”为_______ ,与“试剂Ⅰ”反应的离子有_______
(2)“红褐色沉淀”为_______ ,“ ”的作用是
”的作用是_______
(3)“试剂Ⅲ”是沉淀“溶液B”中 ,证明“溶液B”中
,证明“溶液B”中 已经完全沉淀的试剂为
已经完全沉淀的试剂为_______ 。
(4)“溶液B”中残留 与“试剂Ⅲ”反应的化学方程式为
与“试剂Ⅲ”反应的化学方程式为_______ 。
(5)“溶液C”在空气中晾晒一段时间后,加盐酸调成弱酸性,蒸发可得工业食盐,但加盐酸时有少量气泡逸出,经检验为 ,则“溶液C”中碳酸盐形成的可能离子反应为(写出一个即可)
,则“溶液C”中碳酸盐形成的可能离子反应为(写出一个即可)_______
 和少量的
和少量的 、
、 、
、 ,为减少污染变废为宝,实验小组设计了如图方案(其中每步加入试剂均过量):
,为减少污染变废为宝,实验小组设计了如图方案(其中每步加入试剂均过量):
(1)“试剂Ⅱ”为
(2)“红褐色沉淀”为
 ”的作用是
”的作用是(3)“试剂Ⅲ”是沉淀“溶液B”中
 ,证明“溶液B”中
,证明“溶液B”中 已经完全沉淀的试剂为
已经完全沉淀的试剂为(4)“溶液B”中残留
 与“试剂Ⅲ”反应的化学方程式为
与“试剂Ⅲ”反应的化学方程式为(5)“溶液C”在空气中晾晒一段时间后,加盐酸调成弱酸性,蒸发可得工业食盐,但加盐酸时有少量气泡逸出,经检验为
 ,则“溶液C”中碳酸盐形成的可能离子反应为(写出一个即可)
,则“溶液C”中碳酸盐形成的可能离子反应为(写出一个即可)
您最近一年使用:0次
2022-01-17更新
|
688次组卷
|
2卷引用:四川省达州市2021-2022学年高一上学期期末监测化学试题
解题方法
9 . 电子工业常用FeCl3溶液腐蚀印刷电路板上的铜箔。某研究小组设计以下流程从腐蚀废液中回收铜,并重新获得FeCl3溶液。

(1)FeCl3溶液腐蚀铜箔的离子方程式为___ 。
(2)试剂①为___ (写化学式),试剂②需过量的原因是___ 。
(3)证明“滤液”中不含Fe3+的方法为___ 。
(4)“反应”步骤中的离子方程式为___ 。
(5)向沸水中加入1mol•L-1FeCl3溶液至液体呈透明的红褐色,该分散系具有的独特性质是___ (写出一条)。

(1)FeCl3溶液腐蚀铜箔的离子方程式为
(2)试剂①为
(3)证明“滤液”中不含Fe3+的方法为
(4)“反应”步骤中的离子方程式为
(5)向沸水中加入1mol•L-1FeCl3溶液至液体呈透明的红褐色,该分散系具有的独特性质是
您最近一年使用:0次
2021-01-28更新
|
190次组卷
|
2卷引用:河南省郑州市2020-2021学年高一上学期期末考试化学试题
11-12高三上·黑龙江牡丹江·期末
10 . 某同学欲在实验室中完成Fe与水蒸气反应的实验,装置如图甲、乙两种。
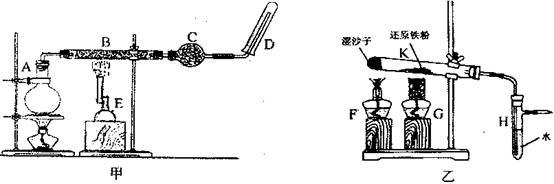
已知B中放入的是铁与石棉绒的混合物,C中放的是干燥剂,E为酒精喷灯,G为带有铁丝网罩的酒精灯。
Ⅰ.对比两装置,回答下列问题:
(1)如何检查乙装置的气密性?_____________________________________ 。
(2)乙装置中湿沙子的作用是________________________________________ 。
(3)B处发生反应的化学方程式:__________________________________________ 。
(4)该同学认为欲在乙装置的尖嘴导管处点燃反应产生的气体,装置H必不可少,H的作用是__________________ 。
(5)对比甲、乙两装置的B和K,B的优点是______________________________ 。
Ⅱ.某同学为了研究一定时间内铁粉的转化率,用上图中的甲装置设计了如下实验:准确称量一定质量的铁粉进行反应,收集并测量反应后生成的气体体积,计算铁粉的转化率。
①用排水法收集并测量气体体积可选下图中的_________________ 装置。
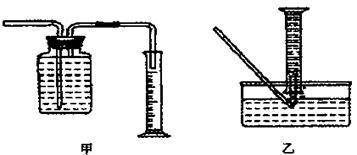
②称取mg铁粉与适量石棉绒混合,然后加热至无气体放出。若收集的气体体积换算为标准状况为VL,铁粉的转化率为(列出计算式即可)________________________ 。
③为了证明反应后的固体混合物中含有+3价的Fe,该同学取出少量混合物于试管中,加入足量的盐酸,溶解后过滤,立即向溶液中滴加KSCN溶液,结果观察到溶液的颜色没变化。经过思考,该同学认为此现象不能说明反应后的固体混合物中不含有+3价Fe。他的理由是:______________ 。

已知B中放入的是铁与石棉绒的混合物,C中放的是干燥剂,E为酒精喷灯,G为带有铁丝网罩的酒精灯。
Ⅰ.对比两装置,回答下列问题:
(1)如何检查乙装置的气密性?
(2)乙装置中湿沙子的作用是
(3)B处发生反应的化学方程式:
(4)该同学认为欲在乙装置的尖嘴导管处点燃反应产生的气体,装置H必不可少,H的作用是
(5)对比甲、乙两装置的B和K,B的优点是
Ⅱ.某同学为了研究一定时间内铁粉的转化率,用上图中的甲装置设计了如下实验:准确称量一定质量的铁粉进行反应,收集并测量反应后生成的气体体积,计算铁粉的转化率。
①用排水法收集并测量气体体积可选下图中的

②称取mg铁粉与适量石棉绒混合,然后加热至无气体放出。若收集的气体体积换算为标准状况为VL,铁粉的转化率为(列出计算式即可)
③为了证明反应后的固体混合物中含有+3价的Fe,该同学取出少量混合物于试管中,加入足量的盐酸,溶解后过滤,立即向溶液中滴加KSCN溶液,结果观察到溶液的颜色没变化。经过思考,该同学认为此现象不能说明反应后的固体混合物中不含有+3价Fe。他的理由是:
您最近一年使用:0次



