1 . 完成下列问题。
(1)某化学研究性学习小组用NH4Cl、KCl、(NH4)2SO4配制含有 、Cl-、K+、
、Cl-、K+、 的溶液,且要求该溶液中,c(Cl-)=c(K+)=c(
的溶液,且要求该溶液中,c(Cl-)=c(K+)=c( )=0.4mol/L,则
)=0.4mol/L,则 的物质的量浓度为
的物质的量浓度为___________ 。
(2)向含有2molHNO3和0.6molH2SO4的混合稀溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。

①a表示的是___________ 的变化曲线。
②n1=___________ ,n3=___________ 。
③向P点溶液中加入铜粉,最多可溶解铜粉的质量是___________ g。
(1)某化学研究性学习小组用NH4Cl、KCl、(NH4)2SO4配制含有
 、Cl-、K+、
、Cl-、K+、 的溶液,且要求该溶液中,c(Cl-)=c(K+)=c(
的溶液,且要求该溶液中,c(Cl-)=c(K+)=c( )=0.4mol/L,则
)=0.4mol/L,则 的物质的量浓度为
的物质的量浓度为(2)向含有2molHNO3和0.6molH2SO4的混合稀溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。

①a表示的是
②n1=
③向P点溶液中加入铜粉,最多可溶解铜粉的质量是
您最近一年使用:0次
名校
2 . 下列解释事实的方程式或离子方程式正确的是
A.铁与稀盐酸反应: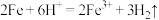 |
B.碳酸钙与稀盐酸反应: |
C.常温下,新切开的钠表面很快变暗: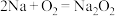 |
D.黄色FeCl3溶液加入铁粉溶液变成浅绿色: |
您最近一年使用:0次
名校
解题方法
3 . 已知 某溶液(该溶液称为
某溶液(该溶液称为 )中仅含有两种溶质
)中仅含有两种溶质 和
和 ,且物质的量浓度依次为
,且物质的量浓度依次为 和
和 ,向该溶液中投入
,向该溶液中投入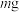 铁粉恰好完全反应,释放出的气体体积为
铁粉恰好完全反应,释放出的气体体积为 。下列叙述正确的是
。下列叙述正确的是
 某溶液(该溶液称为
某溶液(该溶液称为 )中仅含有两种溶质
)中仅含有两种溶质 和
和 ,且物质的量浓度依次为
,且物质的量浓度依次为 和
和 ,向该溶液中投入
,向该溶液中投入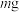 铁粉恰好完全反应,释放出的气体体积为
铁粉恰好完全反应,释放出的气体体积为 。下列叙述正确的是
。下列叙述正确的是A. 中 中 的物质的量为 的物质的量为 |
B.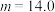 |
C.反应后所得溶液中氧化产物与还原产物的物质的量之比为 |
D.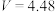 |
您最近一年使用:0次
名校
解题方法
4 . 工业上用赤铁矿(主要含Fe2O3、FeO,还含有少量的Al2O3、CuO等杂质 制备绿矾(FeSO4∙7H2O)的流程如下:
制备绿矾(FeSO4∙7H2O)的流程如下:
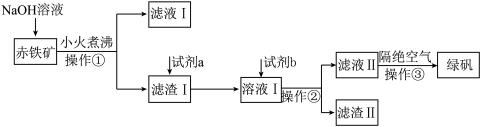
(1)NaOH溶液加入赤铁矿中发生反应的离子方程式为___________ 。
(2)滤液I通过一系列操作可得到Al2O3,该过程涉及化学反应的流程可表示为___________ 。(示例:滤液I B……)。
B……)。
(3)试剂a为___________ (填化学式),试剂 为
为___________ (填化学式),“溶液I”中氧化性最强的阳离子为___________ (填化学式)。
(4)操作③需要隔绝空气的主要原因是___________ 。
(5)8.34gFeSO4∙7H2O(M=278g∙mol-1)样品受热分解过程中样品质量随温度变化的曲线如图所示:
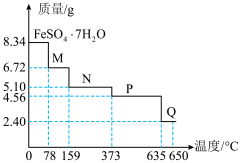
请回答下列问题
①温度为78℃时,固体物质M的化学式为___________ 。
②取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种常见含硫氧化物生成,则Q的化学式为___________ 。
 制备绿矾(FeSO4∙7H2O)的流程如下:
制备绿矾(FeSO4∙7H2O)的流程如下:
(1)NaOH溶液加入赤铁矿中发生反应的离子方程式为
(2)滤液I通过一系列操作可得到Al2O3,该过程涉及化学反应的流程可表示为
 B……)。
B……)。(3)试剂a为
 为
为(4)操作③需要隔绝空气的主要原因是
(5)8.34gFeSO4∙7H2O(M=278g∙mol-1)样品受热分解过程中样品质量随温度变化的曲线如图所示:

请回答下列问题
①温度为78℃时,固体物质M的化学式为
②取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种常见含硫氧化物生成,则Q的化学式为
您最近一年使用:0次
名校
5 . 除去下列物质中的杂质,所用试剂和方法错误的是
| 物质 | 杂质 | 除杂质所用试剂和方法 | |
| A | 铁粉 | 铝粉 | NaOH溶液,过滤、洗涤、干燥 |
| B | 氯化亚铁 | 氯化铁 | 铁粉,过滤 |
| C | 碳酸钠固体 | 碳酸氢钠固体 | 加热 |
| D | 氧化铝 | 氧化钠 | 水,过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 下列不属于化合反应的是
| A.Fe+2Fe3+=3Fe2+ | B.Fe3++3OH-=Fe(OH)3↓ |
| C.4Fe(OH)2+O2+2H2O=4Fe(OH)3 | D.3Fe+2O2 Fe3O4 Fe3O4 |
您最近一年使用:0次
解题方法
7 . 下列离子方程式正确的是
A.化工生产中漂白粉的制备: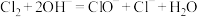 |
B.过氧化钠溶于水: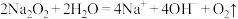 |
C.铁与氯化铁溶液的反应: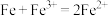 |
D.用小苏打治疗胃酸过多: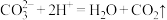 |
您最近一年使用:0次
8 . 铁及其化合物在日常生产生活中有着广泛应用。
I.在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。现设计如下装置完成高温下“Fe与水蒸气反应”的实验,并检验其产物(已知:Fe3O4中Fe的化合价为+2价、+3价)。
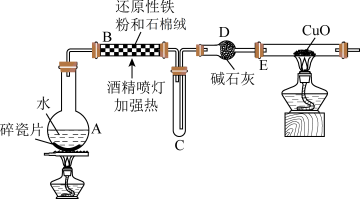
(1)装置B中发生反应的化学方程式为___________ 。
(2)装置C中导管“短进长出”的原因___________ 。
(3)取反应后得到的黑色粉末放入一试管中,加入稀硫酸将固体溶解,再滴加几滴KSCN溶液,振荡,溶液没有出现红色,原因是___________ (用离子方程式表示)。
II.某学生设计了如图装置制备白色Fe(OH)2固体。
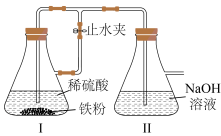
(4)开始实验时,先打开止水夹,待装置中空气已排尽,再关闭止水夹。
①关闭止水夹前,如何证明装置中空气已排尽:___________ 。
②装置II中发生反应的主要化学方程式为___________ 。
③若未排净装置中的空气,则装置II中观察到的实验现象为___________ 。
I.在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。现设计如下装置完成高温下“Fe与水蒸气反应”的实验,并检验其产物(已知:Fe3O4中Fe的化合价为+2价、+3价)。

(1)装置B中发生反应的化学方程式为
(2)装置C中导管“短进长出”的原因
(3)取反应后得到的黑色粉末放入一试管中,加入稀硫酸将固体溶解,再滴加几滴KSCN溶液,振荡,溶液没有出现红色,原因是
II.某学生设计了如图装置制备白色Fe(OH)2固体。

(4)开始实验时,先打开止水夹,待装置中空气已排尽,再关闭止水夹。
①关闭止水夹前,如何证明装置中空气已排尽:
②装置II中发生反应的主要化学方程式为
③若未排净装置中的空气,则装置II中观察到的实验现象为
您最近一年使用:0次
名校
解题方法
9 . 如图为铁元素的“价—类”二维图,请回答下列问题。

(1)图中“ ”代表的物质类别为
”代表的物质类别为_______ 。图中物质只具有还原性的是_______ (填化学式)。
(2)在烧制砖瓦时,用黏土做成的坯经过烘烧后,铁的化合物转化成___________ (填字母,下同)而制得红色砖瓦;若烘烧后期从窑顶向下慢慢浇水,窑内会产生大量 、
、 气体,它们把该红色物质还原成黑色的
气体,它们把该红色物质还原成黑色的___________ ,同时还有未燃烧的碳的颗粒,而制得了青色砖瓦。
A. B.
B. C.
C. D.
D.
(3)根据上述“价—类”二维图判断 中
中 元素的价态,写出
元素的价态,写出 与稀盐酸反应的离子方程式
与稀盐酸反应的离子方程式___________ 。
(4)用坩埚钳夹住一束铁丝,灼烧后立即放入充满氯气的集气瓶中,观察到的现象是铁丝剧烈燃烧,___________ 。
(5)以绿矾(主要成分 ,部分
,部分 已被氧化为
已被氧化为 )为原料,生产铁红
)为原料,生产铁红 的工艺流程如图:
的工艺流程如图:
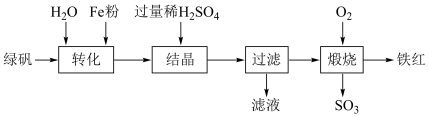
①“转化”过程中,加入过量 粉时发生反应的离子方程式为
粉时发生反应的离子方程式为___________ 。
②“结晶”时,加入过量稀硫酸的目的是___________ 。
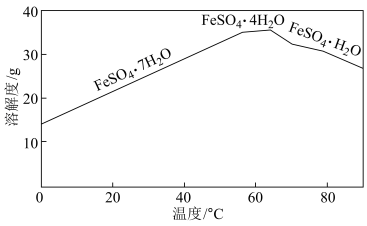
③“结晶”时,控制温度在75℃左右进行(相关物质的溶解度见图),从溶液中析出的晶体是___________ (填化学式)。
④“煅烧”时生成铁红的化学方程式为___________ 。

(1)图中“
 ”代表的物质类别为
”代表的物质类别为(2)在烧制砖瓦时,用黏土做成的坯经过烘烧后,铁的化合物转化成
 、
、 气体,它们把该红色物质还原成黑色的
气体,它们把该红色物质还原成黑色的A.
 B.
B. C.
C. D.
D.
(3)根据上述“价—类”二维图判断
 中
中 元素的价态,写出
元素的价态,写出 与稀盐酸反应的离子方程式
与稀盐酸反应的离子方程式(4)用坩埚钳夹住一束铁丝,灼烧后立即放入充满氯气的集气瓶中,观察到的现象是铁丝剧烈燃烧,
(5)以绿矾(主要成分
 ,部分
,部分 已被氧化为
已被氧化为 )为原料,生产铁红
)为原料,生产铁红 的工艺流程如图:
的工艺流程如图:
①“转化”过程中,加入过量
 粉时发生反应的离子方程式为
粉时发生反应的离子方程式为②“结晶”时,加入过量稀硫酸的目的是
③“结晶”时,控制温度在75℃左右进行(相关物质的溶解度见图),从溶液中析出的晶体是

④“煅烧”时生成铁红的化学方程式为
您最近一年使用:0次
10 . 铁、铜等金属及其化合物在日常生产生活中有非常广泛的用途。
I.化学实验室产生的废液中含有大量会污染环境的物质,为了保护环境,这些废液必须经处理后才能排放。某化学实验室产生的废液中含有两种金属离子: 、
、 ,化学小组设计了如图所示的方案对废液进行处理,以回收金属,保护环境。
,化学小组设计了如图所示的方案对废液进行处理,以回收金属,保护环境。

(1)操作①的名称是___________ 。加入铁屑先发生的离子反应为:___________ 。
(2)沉淀A中含有的金属单质有___________ 。
(3)操作②中观察到的实验现象是___________ 。
(4)操作③中发生反应的离子方程式为___________ 。
II.某化学实验小组通过实验来探究一包黑色粉是否含有 、CuO,探究过程如下:
、CuO,探究过程如下:
提出假设:
假设1.黑色粉末是CuO;
假设2.黑色粉末是 ;
;
假设3.黑色粉末是CuO和 的混合物。
的混合物。
设计探究实验:取少量粉末放入足量稀硫酸中,得溶液X,取一定量X于试管中,向其中滴加KSCN溶液。
(5)若假设1成立,则实验现象是___________ 。
(6)若假设2成立,则实验现象是___________ 。如何检验溶液X中含 离子?
离子?___________ 。
(7)若假设3成立,需继续向X溶液加入足量铁粉,则实验现象是___________ 。
I.化学实验室产生的废液中含有大量会污染环境的物质,为了保护环境,这些废液必须经处理后才能排放。某化学实验室产生的废液中含有两种金属离子:
 、
、 ,化学小组设计了如图所示的方案对废液进行处理,以回收金属,保护环境。
,化学小组设计了如图所示的方案对废液进行处理,以回收金属,保护环境。
(1)操作①的名称是
(2)沉淀A中含有的金属单质有
(3)操作②中观察到的实验现象是
(4)操作③中发生反应的离子方程式为
II.某化学实验小组通过实验来探究一包黑色粉是否含有
 、CuO,探究过程如下:
、CuO,探究过程如下:提出假设:
假设1.黑色粉末是CuO;
假设2.黑色粉末是
 ;
;假设3.黑色粉末是CuO和
 的混合物。
的混合物。设计探究实验:取少量粉末放入足量稀硫酸中,得溶液X,取一定量X于试管中,向其中滴加KSCN溶液。
(5)若假设1成立,则实验现象是
(6)若假设2成立,则实验现象是
 离子?
离子?(7)若假设3成立,需继续向X溶液加入足量铁粉,则实验现象是
您最近一年使用:0次



