10-11高三上·江苏泰州·阶段练习
名校
解题方法
1 . 向一定量的Fe、FeO、Fe2O3的混合物中加入100mL1mol/L的盐酸,恰好使混合物完全溶解,放出224mL(标准状况下)的气体。所得溶液中加入KSCN溶液无红色出现,混合物中铁元素的质量分数为
| A.81.4% | B.77.8% | C.68.6% | D.无法计算 |
您最近一年使用:0次
2023-01-06更新
|
893次组卷
|
11卷引用:2017届河北省冀州中学高三(高复班)上学期一轮检测(二)化学试卷
2017届河北省冀州中学高三(高复班)上学期一轮检测(二)化学试卷2016届湖南省益阳市箴言中学高三上学期第三次模拟化学试卷(已下线)2010年江苏省泰兴市重点中学高三上学期第一次检测化学试题2016-2017学年湖北省武钢三中高一12月月考化学试卷江苏省启东中学2017-2018学年高一(创新2班)上学期期中考试化学试题天津市耀华中学2022-2023学年高一上学期期末考试化学试题天津市耀华中学2022-2023学年高一上学期期末考试化学试题 山东省淄博实验中学2022-2023学年高一上学期期末考试化学试题(已下线)期末测试卷02-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册) 2023-2024学年高一上学期化学人教版(2019)必修第一册 期末综合测试题(一)河南省南阳市邓州市第一高级中学校2023-2024学年高一上学期期末考试化学试题
名校
解题方法
2 . 下列实验操作现象与结论对应关系正确的是
| 实验操作、现象 | 结论 | |
| A | 加热NaI固体和浓磷酸的混合物,有气体产生 | 浓磷酸的酸性大于氢碘酸 |
| B | 分别在20℃、30℃下,取 溶液,向其中先加入 溶液,向其中先加入 的硫酸,再加入淀粉溶液,发生反应 的硫酸,再加入淀粉溶液,发生反应 | 探究反应速率与温度的关系 |
| C | 将SO2通入Ca(ClO)2溶液,出现白色沉淀 | SO2是酸性氧化物 |
| D | 探究氧化铁和乙醇反应得到黑色固体成分,该黑色固体能被磁铁吸引且加入足量稀盐酸,振荡,固体全部溶解,未观察到有气体生成 | 不能确定是否含有0价铁 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 工业上用铁泥(主要成分为Fe2O3、FeO和少量Fe)制备纳米Fe3O4的流程图如图:

下列叙述正确的是

下列叙述正确的是
| A.为提高步骤①的反应速率,所加稀盐酸的量越多越好 |
| B.步骤②中,主要反应的离子方程式为2Fe3++Fe=3Fe2+ |
| C.步骤④中,反应完成后剩余的H2O2无需除去 |
| D.步骤⑥中,“分离”包含的操作有过滤、洗涤 |
您最近一年使用:0次
名校
4 . 下列有关铁及其化合物的说法中正确的是( )
| A.铁的氧化物都难溶于水,且不与水反应 |
| B.铁与水蒸气在高温下反应的产物为Fe2O3和H2 |
| C.Fe3O4常用作油漆、涂料、油墨和橡胶的红色颜料 |
| D.FeO是一种黑色粉末,不稳定,在空气中受热,迅速被氧化成Fe2O3 |
您最近一年使用:0次
2021-01-31更新
|
150次组卷
|
2卷引用:河北省石家庄市第二中学西校区2020-2021学年高一上学期假期考试化学试题
解题方法
5 . 硫酸亚铁在空气中易被氧化,与硫酸铵反应生成硫酸亚铁铵[化学式为FeSO4·(NH4)2SO4·6H2O]后就不易被氧化。模拟工业制备硫酸亚铁铵晶体的实验装置如下图所示。请回答下列问题:
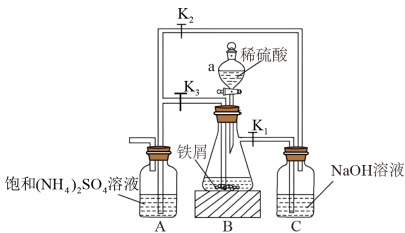
(1)仪器a的名称是______________________ 。
(2)铁屑中常含有Fe2O3、FeS等杂质,则装置C的作用是___________ ,装置B中发生反应的离子方程式可能是___________ (填序号)。
A. Fe+2H+=Fe2++H2↑
B.Fe2O3+6H+=2Fe3++3H2O
C.2Fe3++S2-=2Fe2++S↓
D.2Fe3++Fe=2Fe2+
(3)按上图连接好装置,经检验气密性良好后加入相应的药品,打开K1、K2,关闭K3,装置B中有气体产生,该气体的作用是___________ 。反应一段时间后,打开K3,关闭K1和K2。装置B中的溶液会流入装置A,其原因是______________________ 。
(4)按上图所示装置制备硫酸亚铁铵晶体的安全隐患是______________________ 。
(5)根据相关物质的溶解度判断,从装置A中分离出硫酸亚铁铵晶体,需采用的操作有___________ 、___________ 、洗涤、干燥。
三种盐的溶解度(单位为g/100gH2O)

(1)仪器a的名称是
(2)铁屑中常含有Fe2O3、FeS等杂质,则装置C的作用是
A. Fe+2H+=Fe2++H2↑
B.Fe2O3+6H+=2Fe3++3H2O
C.2Fe3++S2-=2Fe2++S↓
D.2Fe3++Fe=2Fe2+
(3)按上图连接好装置,经检验气密性良好后加入相应的药品,打开K1、K2,关闭K3,装置B中有气体产生,该气体的作用是
(4)按上图所示装置制备硫酸亚铁铵晶体的安全隐患是
(5)根据相关物质的溶解度判断,从装置A中分离出硫酸亚铁铵晶体,需采用的操作有
三种盐的溶解度(单位为g/100gH2O)
温度 | FeSO4 | (NH4)2SO4 | 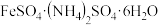 |
| 10 | 20.0 | 73 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78 | 28.1 |
您最近一年使用:0次
2018·河北·一模
6 . 实验室测定氧化物X(FexOy)的组成实验如下:

下列有关说法正确的是

下列有关说法正确的是
| A.步骤Ⅰ、Ⅱ中氯元素均被还原 |
| B.溶液Y中c(Fe2+)︰c(Fe3+)=1︰2 |
| C.溶液Z中的离子只有Fe3+和Cl- |
| D.步骤Ⅰ中消耗HCl的物质的量为0.28mol |
您最近一年使用:0次
名校
解题方法
7 . 黄铜矿(CuFeS2)是冶炼铜及制备铁的氧化物的重要矿藏,常含有微量的金、银等。如图是以黄铜矿为主要原料生产铜、铁红(氧化铁)颜料的工艺流程图:

(1)反应Ⅰ的离子方程式为_________________________________________ 。
(2)CuCl难溶于水,但可与过量的Cl-反应生成溶于水的[CuCl2]-。该反应的离子方程式为_________________________________________________ 。
(3)有大量Cl-存在时,Na2SO3可将CuCl2还原成[CuCl2]-。 Na2SO3要缓慢滴加到溶液中的原因是_________________________________________________ 。
(4)反应Ⅰ〜Ⅴ五个反应中属于非氧化还原反应的是反应____________ 。
(5)已知Cu+在反应Ⅴ中发生自身氧化还原反应,歧化为Cu2+和Cu,由此可推知溶液A中的溶质为_______________ (填化学式)。
(6)含AsO43-的废水对环境造成严重污染,常用新制的氢氧化铁沉淀与之作用形成FeAsO4沉淀而除去,相同温度下溶解度:Fe(OH)3__________ (填“<”“ >”或“=”)FeAsO4。
(7)在酸性、有氧条件下,一种叫Thibacillus ferroxidans的细菌能将黄铜矿转化成硫酸盐,该过程中发生反应的离子方程式为________________________________ 。
(8)将一定量的铁红溶于160 mL 5 mol • L-1盐酸中,再加入足量铁粉,待反应结束后共收集到气体2.24 L (标准状况),经检测,溶液中无 Fe3+,则参加反应的铁粉的质量为_____________ 。

(1)反应Ⅰ的离子方程式为
(2)CuCl难溶于水,但可与过量的Cl-反应生成溶于水的[CuCl2]-。该反应的离子方程式为
(3)有大量Cl-存在时,Na2SO3可将CuCl2还原成[CuCl2]-。 Na2SO3要缓慢滴加到溶液中的原因是
(4)反应Ⅰ〜Ⅴ五个反应中属于非氧化还原反应的是反应
(5)已知Cu+在反应Ⅴ中发生自身氧化还原反应,歧化为Cu2+和Cu,由此可推知溶液A中的溶质为
(6)含AsO43-的废水对环境造成严重污染,常用新制的氢氧化铁沉淀与之作用形成FeAsO4沉淀而除去,相同温度下溶解度:Fe(OH)3
(7)在酸性、有氧条件下,一种叫Thibacillus ferroxidans的细菌能将黄铜矿转化成硫酸盐,该过程中发生反应的离子方程式为
(8)将一定量的铁红溶于160 mL 5 mol • L-1盐酸中,再加入足量铁粉,待反应结束后共收集到气体2.24 L (标准状况),经检测,溶液中无 Fe3+,则参加反应的铁粉的质量为
您最近一年使用:0次
2011·河北邢台·一模
解题方法
8 . 以黄铜矿(CuFeS2)为原料冶炼铜的反应为:
8CuFeS2+21O2 8Cu+4FeO3+2Fe2O3+16SO2
8Cu+4FeO3+2Fe2O3+16SO2
(1)若Cu为+2价,则反应中每生成1molCu需要转移_____________ mol电子。
(2)为综合利用炉气中的大量SO2,下列方案合理的是___________ 。
a.用浓硫酸吸收 b.用于制备硫酸
c.高空排放 d.用纯碱液吸收制亚硫酸钠
(3)为检验所得矿渣是中是否含有FeO、Fe2O3、CuO、A12O3、SiO2等氧化物,进行了以下实验;
①取一定量矿渣粉末,加入适量浓硫酸后加热,固体全部溶解,得溶液A;将产生的气体通入品红溶液中,溶液褪色。由此判断矿渣中一定含有_________ ,一定没有______ 。
②将溶液A稀释后分成两份,取其中一份,加入过量NaOH溶液,有沉淀产生,静置后取上层清液,通入过量的CO2溶液变浑浊。由此判断出矿渣中含有_________ ,写出通入过量的CO2所发生反应的离子方程式:______________ 。
③取另一份溶液A加入过量的铁粉充分反应后过滤,得到的固体中有红色物质,由此判断矿渣中有_____________ ,写出此步操作中得到红色物质所发生反应的离子方程式____________ 。
8CuFeS2+21O2
 8Cu+4FeO3+2Fe2O3+16SO2
8Cu+4FeO3+2Fe2O3+16SO2(1)若Cu为+2价,则反应中每生成1molCu需要转移
(2)为综合利用炉气中的大量SO2,下列方案合理的是
a.用浓硫酸吸收 b.用于制备硫酸
c.高空排放 d.用纯碱液吸收制亚硫酸钠
(3)为检验所得矿渣是中是否含有FeO、Fe2O3、CuO、A12O3、SiO2等氧化物,进行了以下实验;
①取一定量矿渣粉末,加入适量浓硫酸后加热,固体全部溶解,得溶液A;将产生的气体通入品红溶液中,溶液褪色。由此判断矿渣中一定含有
②将溶液A稀释后分成两份,取其中一份,加入过量NaOH溶液,有沉淀产生,静置后取上层清液,通入过量的CO2溶液变浑浊。由此判断出矿渣中含有
③取另一份溶液A加入过量的铁粉充分反应后过滤,得到的固体中有红色物质,由此判断矿渣中有
您最近一年使用:0次



