名校
1 . 炼铁厂的废渣铁矾渣主要含有K2Fe6(SO4)4(OH)12、ZnO Fe2O3及少量的CaO、MgO、SiO2 ,等等。可利用废渣铁矾渣制备复合镍锌铁氧体 (NiZnFe4O8.具体制备流程如下图所示:
Fe2O3及少量的CaO、MgO、SiO2 ,等等。可利用废渣铁矾渣制备复合镍锌铁氧体 (NiZnFe4O8.具体制备流程如下图所示:
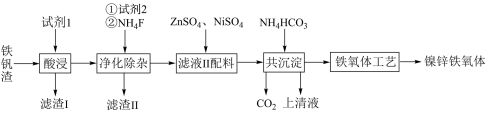
(1)试剂1是过量的______ 。
(2)试剂2为过量的铁粉,加入后可以观察的现象有______________________ 。
(3)NH4F溶液不能放入玻璃器皿中保存,理由是_____________________________ (用离子方程式表示)。已知:25 °C时,Ksp(CaF2)=2.7×10-11、,Ksp(MgF2)=6.4×10-19。加入NH4F溶液沉淀后,c(Mg2+) = 1. 6×10-10mol • L-1,此时Ca2+是否也完全沉淀?写出具体的分析过程:______ (若溶液中某离子浓度小于1.0×10-5mol • L-1时,说明该离子已沉淀完全)。
(4)在Fe2+、Ni2+、Zn2+共沉淀过程中,若以Me代表Fe、Ni、Zn元素,则生成MeCO3•2Me(OH)2•H2O沉淀的化学方程式为________________________________ .
(5)按照上述流程,一座10万吨规模的炼铁厂每年产生铁矾渣约5万吨,Fe3+含量为44.8%,理论上每年至少可制备复合镍锌铁氧体(NiZnFe4O8,M=476 g • mol -1)__________ 万吨。
(6)滤液Ⅱ中加入的ZnSO4溶液,低温烘干后可得到皓矾(ZnSO4• 7H2O) 取28.70 g皓矾加热至不同温度,剩余固体的质量变化如图所示:

①100 °C时所得固体的化学式__________ 。
②680 °C时所得固体的化学式为____
 Fe2O3及少量的CaO、MgO、SiO2 ,等等。可利用废渣铁矾渣制备复合镍锌铁氧体 (NiZnFe4O8.具体制备流程如下图所示:
Fe2O3及少量的CaO、MgO、SiO2 ,等等。可利用废渣铁矾渣制备复合镍锌铁氧体 (NiZnFe4O8.具体制备流程如下图所示:
(1)试剂1是过量的
(2)试剂2为过量的铁粉,加入后可以观察的现象有
(3)NH4F溶液不能放入玻璃器皿中保存,理由是
(4)在Fe2+、Ni2+、Zn2+共沉淀过程中,若以Me代表Fe、Ni、Zn元素,则生成MeCO3•2Me(OH)2•H2O沉淀的化学方程式为
(5)按照上述流程,一座10万吨规模的炼铁厂每年产生铁矾渣约5万吨,Fe3+含量为44.8%,理论上每年至少可制备复合镍锌铁氧体(NiZnFe4O8,M=476 g • mol -1)
(6)滤液Ⅱ中加入的ZnSO4溶液,低温烘干后可得到皓矾(ZnSO4• 7H2O) 取28.70 g皓矾加热至不同温度,剩余固体的质量变化如图所示:

①100 °C时所得固体的化学式
②680 °C时所得固体的化学式为
您最近一年使用:0次
名校
解题方法
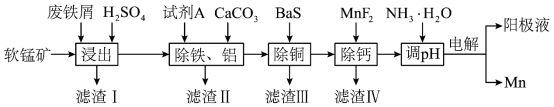
2 . 以废铁屑、低品位软锰矿[主要成分有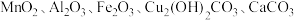 、
、 等]为原料,制备硫酸锰,进一步电解制备金属锰,工艺流程如图所示:
等]为原料,制备硫酸锰,进一步电解制备金属锰,工艺流程如图所示:
已知:I.部分金属阳离子以氢氧化物沉淀时的 如表:
如表:
Ⅱ.几种化合物的溶解性或溶度积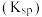 如表:
如表:
(1)基态 的价层电子排布式为
的价层电子排布式为__________ 。
(2)为去除废铁屑表面的油污可采用的方法为__________ ;“浸出”后浸出液中的 价金属阳离子有
价金属阳离子有 、
、__________ 。
(3)锰的浸出率结果如图所示。

由图可知,影响锰浸出率的因素有__________ 。
(4)“除铁、铝”过程中,浸出液需要先用试剂 处理,然后加入
处理,然后加入 ,反应后溶液的
,反应后溶液的 。试剂
。试剂 的作用是
的作用是__________ 。
(5)“除铜”过程中,当铜离子恰好完全沉淀(当离子浓度小于或等于 时视为完全沉淀)时,溶液中
时视为完全沉淀)时,溶液中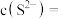
__________  。
。
(6)用惰性电极电解中性 溶液可以制得金属
溶液可以制得金属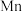 。装置如图所示。
。装置如图所示。
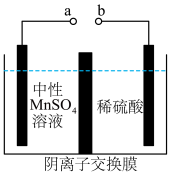
若生成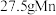 ,右室溶液中最终
,右室溶液中最终 的变化为
的变化为__________ (填“增加”或“减少”) 。
。
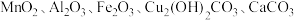 、
、 等]为原料,制备硫酸锰,进一步电解制备金属锰,工艺流程如图所示:
等]为原料,制备硫酸锰,进一步电解制备金属锰,工艺流程如图所示:
已知:I.部分金属阳离子以氢氧化物沉淀时的
 如表:
如表:| 金属阳离子 |  |  |  |  |  |
开始沉淀的 | 6.8 | 1.8 | 3.7 | 8.6 | 5.2 |
沉淀完全的 | 8.3 | 2.8 | 4.7 | 10.1 | 6.7 |
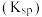 如表:
如表:| 化合物 |  |  |  |  |  |
溶解性或溶度积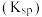 | 溶于水 | 溶于水 | 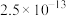 |  |  |
(1)基态
 的价层电子排布式为
的价层电子排布式为(2)为去除废铁屑表面的油污可采用的方法为
 价金属阳离子有
价金属阳离子有 、
、(3)锰的浸出率结果如图所示。

由图可知,影响锰浸出率的因素有
(4)“除铁、铝”过程中,浸出液需要先用试剂
 处理,然后加入
处理,然后加入 ,反应后溶液的
,反应后溶液的 。试剂
。试剂 的作用是
的作用是(5)“除铜”过程中,当铜离子恰好完全沉淀(当离子浓度小于或等于
 时视为完全沉淀)时,溶液中
时视为完全沉淀)时,溶液中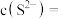
 。
。(6)用惰性电极电解中性
 溶液可以制得金属
溶液可以制得金属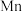 。装置如图所示。
。装置如图所示。
若生成
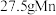 ,右室溶液中最终
,右室溶液中最终 的变化为
的变化为 。
。
您最近一年使用:0次
解题方法
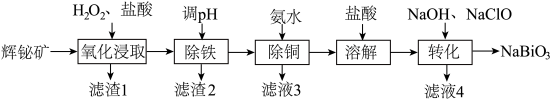
3 . 铋(Bi)的化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为 ,含
,含 、CuO、
、CuO、 等杂质)制备
等杂质)制备 的工艺流程如下:
的工艺流程如下:
已知:
i. 易水解。
易水解。 难溶于冷水。
难溶于冷水。
ii.“氧化浸取”时,铋元素转化为 ,硫元素转化为硫单质。
,硫元素转化为硫单质。
iii.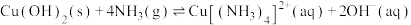
 。
。
回答下列问题:
(1)为提高“浸取”速率,采取的措施有:升高温度、___________ (写出一条)。辉铋矿浸取率随温度的变化曲线如图,高于40℃时浸取率快速下降,其可能的原因是___________ 。
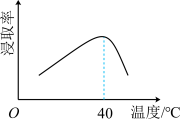
(2)“氧化浸取”时, 和
和 发生反应的物质的量之比为
发生反应的物质的量之比为___________ 。
(3)“除铜”时发生反应: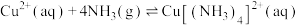
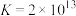 ,则
,则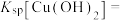
___________ 。
(4)“转化”时,生成 的离子方程式为
的离子方程式为___________ 。
(5)已知酸性环境下, 可以将
可以将 氧化成
氧化成 (
( 被还原成
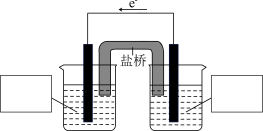
被还原成 )。请设计一个原电池装置来证明这一点,在下图中的两个方框内标出两烧杯溶液中溶质的化学式
)。请设计一个原电池装置来证明这一点,在下图中的两个方框内标出两烧杯溶液中溶质的化学式___________ ,并写出正极的电极反应式:___________ 。
(6)取 产品w g,加入足量稀硫酸和
产品w g,加入足量稀硫酸和 稀溶液使其完全反应,再用a mol·L
稀溶液使其完全反应,再用a mol·L
 标准溶液滴定生成的
标准溶液滴定生成的 ,当溶液紫红色恰好褪去时,消耗b mL标准溶液。该产品的纯度为
,当溶液紫红色恰好褪去时,消耗b mL标准溶液。该产品的纯度为___________ (用含w、a、b的代数式表示)。
 ,含
,含 、CuO、
、CuO、 等杂质)制备
等杂质)制备 的工艺流程如下:
的工艺流程如下:
已知:
i.
 易水解。
易水解。 难溶于冷水。
难溶于冷水。ii.“氧化浸取”时,铋元素转化为
 ,硫元素转化为硫单质。
,硫元素转化为硫单质。iii.
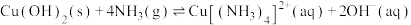
 。
。回答下列问题:
(1)为提高“浸取”速率,采取的措施有:升高温度、

(2)“氧化浸取”时,
 和
和 发生反应的物质的量之比为
发生反应的物质的量之比为(3)“除铜”时发生反应:
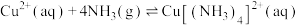
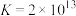 ,则
,则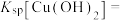
(4)“转化”时,生成
 的离子方程式为
的离子方程式为(5)已知酸性环境下,
 可以将
可以将 氧化成
氧化成 (
( 被还原成
被还原成 )。请设计一个原电池装置来证明这一点,在下图中的两个方框内标出两烧杯溶液中溶质的化学式
)。请设计一个原电池装置来证明这一点,在下图中的两个方框内标出两烧杯溶液中溶质的化学式
(6)取
 产品w g,加入足量稀硫酸和
产品w g,加入足量稀硫酸和 稀溶液使其完全反应,再用a mol·L
稀溶液使其完全反应,再用a mol·L
 标准溶液滴定生成的
标准溶液滴定生成的 ,当溶液紫红色恰好褪去时,消耗b mL标准溶液。该产品的纯度为
,当溶液紫红色恰好褪去时,消耗b mL标准溶液。该产品的纯度为
您最近一年使用:0次
4 . 工业上以铬铁矿(FeCr2O4,含Al、Si氧化物等杂质)为主要原料制备红矾钠(Na2Cr2O7•2H2O)的工艺流程如图。回答下列问题:___ ;冷却结晶所得母液中,除Na2Cr2O7外,可在上述流程中循环利用的物质还有____ 。
(4)利用膜电解技术(装置如图所示),以Na2CrO4为主要原料制备Na2Cr2O7的总反应方程式为:4Na2CrO4+4H2O 2Na2Cr2O7+4NaOH+2H2↑+O2↑。则Na2Cr2O7在
2Na2Cr2O7+4NaOH+2H2↑+O2↑。则Na2Cr2O7在___ (填“阴”或“阳”)极室制得,电解时通过膜的离子主要为___ 。

(1)焙烧的目的是将FeCr2O4转化为Na2CrO4并将Al、Si氧化物转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是
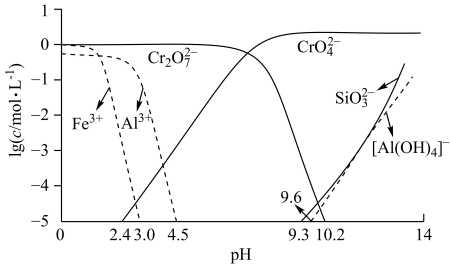
中和时pH的理论范围为
(4)利用膜电解技术(装置如图所示),以Na2CrO4为主要原料制备Na2Cr2O7的总反应方程式为:4Na2CrO4+4H2O
 2Na2Cr2O7+4NaOH+2H2↑+O2↑。则Na2Cr2O7在
2Na2Cr2O7+4NaOH+2H2↑+O2↑。则Na2Cr2O7在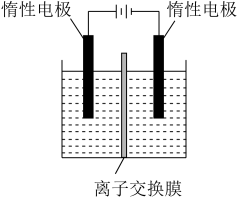
您最近一年使用:0次
2021-06-29更新
|
14390次组卷
|
22卷引用:湖南省邵阳市邵东市创新高级中学2023-2024学年高三上学期第四次月考化学试题
湖南省邵阳市邵东市创新高级中学2023-2024学年高三上学期第四次月考化学试题2021年新高考山东化学高考真题(已下线)微专题32 化学工艺流程题——核心反应与条件控制-备战2022年高考化学考点微专题(已下线)专题16 工艺流程综合题-备战2022年高考化学真题及地市好题专项集训【山东专用】(已下线)专题讲座(六)化工流程的解题策略(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)2021年山东高考化学试题变式题11-20(已下线)解密11 化学实验基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密11 化学实验(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题27 无机化工流程-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)押新高考卷14题 工艺流程综合题-备战2022年高考化学临考题号押题(新高考通版)(已下线)回归教材重难点08 化学工艺流程分析-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)微专题17 热点金属及其化合物制备流程(V、Cr、Mn、Co、Ni)-备战2023年高考化学一轮复习考点微专题(已下线)微专题25 化学工艺流程题-----原料的预处理-备战2023年高考化学一轮复习考点微专题(已下线)微专题27 化学工艺流程题-----物质的分离与提纯-备战2023年高考化学一轮复习考点微专题山东省济宁市邹城市孟子湖中学2021-2022学年高三下学期开学考试化学试题第二部分 热点专项突破——解题能力稳提升 专项3 结合理论的综合类工艺流程(已下线)题型39 其他过渡金属及其化合物的转化流程(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)江苏省华罗庚中学2023-2024学年高三上学期12月阶段检测化学试卷
5 . 工业上以黄铜矿(主要成分CuFeS2)为原料制备CuS04.5H2O的主要流程如下:

(1)下列装置不能用于吸收气体X的是___________ 。(填代号)。

(2)熔渣Y的成分为Fe203和Fe0,选用提供的试剂,设计实验验证熔渣中含有FeO。
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMn04溶液、NaOH溶液、氯水。
①从上述提供的试剂中选择实验验证所需药品____________________ 。
②写出验证过程中所发生的氧化还原反应的离子方程式____________________ 。
(3)向粗铜中加入硫酸和硝酸的混酸溶液制取硫酸铜时(杂质不参加反应),混酸中HNO3与H2S04的最佳物质的量之比为__________ 。

(1)下列装置不能用于吸收气体X的是

(2)熔渣Y的成分为Fe203和Fe0,选用提供的试剂,设计实验验证熔渣中含有FeO。
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMn04溶液、NaOH溶液、氯水。
①从上述提供的试剂中选择实验验证所需药品
②写出验证过程中所发生的氧化还原反应的离子方程式
(3)向粗铜中加入硫酸和硝酸的混酸溶液制取硫酸铜时(杂质不参加反应),混酸中HNO3与H2S04的最佳物质的量之比为
您最近一年使用:0次



