名校
解题方法
1 . 用氧化焙烧-软锰矿浆吸收工艺处理砷华废渣,吸收液经净化除杂、浓缩结晶等工序可制备工业产品硫酸锰。

已知:a.砷华废渣中硫主要以FeS、FeS2、FeAsS、单质硫、硫酸盐等形态存在;铁主要以Fe2O3、FeAsS、FeS形态存在;砷主要以FeAsS、Fe3(AsO4)2等形态存在。
b.软锰矿吸收的过程中,除锰浸出外,还伴随着杂质Fe、Al、Ca、Pb和Si等的同时浸出。
c.SDD为二乙胺硫代甲酸钠。
d.溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
回答下列问题:
(1)砷华废渣预先粉碎的目的是___ ;写出焙烧时FeAsS被氧气氧化成+3价金属氧化物和SO2的方程式:___ 。
(2)砷华废渣焙烧温度与Mn的浸出率的关系图如图:
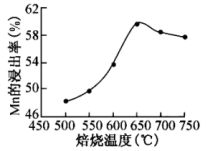
①焙烧的适宜温度为___ 。
②Mn的浸出率随着焙烧的温度升高而升高,温度高于650℃后,Mn的浸出率降低的可能原因是___ 。
(3)软锰矿浆(MnO2)吸收焙烧放出的SO2的化学方程式为___ 。
(4)加入MnO2粉末的目的是氧化Fe2+,其发生反应的离子方程式为___ 。
(5)根据实验目的调节pH的范围是___ 。
(6)称量产品MnSO4·H2O17.21g,溶于水,滴加足量的BaCl2溶液,生成的沉淀,经过过滤、洗涤、干燥后得固体,称量固体的质量为23.30g,则产品中MnSO4·H2O的质量分数为___ %(保留1位小数)。

已知:a.砷华废渣中硫主要以FeS、FeS2、FeAsS、单质硫、硫酸盐等形态存在;铁主要以Fe2O3、FeAsS、FeS形态存在;砷主要以FeAsS、Fe3(AsO4)2等形态存在。
b.软锰矿吸收的过程中,除锰浸出外,还伴随着杂质Fe、Al、Ca、Pb和Si等的同时浸出。
c.SDD为二乙胺硫代甲酸钠。
d.溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
| 金属离子 | Fe2+ | Fe3+ | Al3+ | Pb2+ | Mn2+ |
| 开始沉淀时pH | 7.0 | 1.9 | 3.7 | 7.1 | 8.1 |
| 完全沉淀时pH | 9.0 | 3.2 | 4.7 | 9.1 | 10.1 |
(1)砷华废渣预先粉碎的目的是
(2)砷华废渣焙烧温度与Mn的浸出率的关系图如图:

①焙烧的适宜温度为
②Mn的浸出率随着焙烧的温度升高而升高,温度高于650℃后,Mn的浸出率降低的可能原因是
(3)软锰矿浆(MnO2)吸收焙烧放出的SO2的化学方程式为
(4)加入MnO2粉末的目的是氧化Fe2+,其发生反应的离子方程式为
(5)根据实验目的调节pH的范围是
(6)称量产品MnSO4·H2O17.21g,溶于水,滴加足量的BaCl2溶液,生成的沉淀,经过过滤、洗涤、干燥后得固体,称量固体的质量为23.30g,则产品中MnSO4·H2O的质量分数为
您最近一年使用:0次
2021-09-10更新
|
252次组卷
|
3卷引用:湖南省常德市汉寿县第一中学2023-2024学年高三下学期开学化学试题
名校
解题方法
2 . 氧化铁红颜料跟某些油料混合,可以制成防锈油漆.以黄铁矿为原料制硫酸产生的硫酸渣中含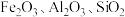 (难溶于稀硫酸),用硫酸渣制备铁红
(难溶于稀硫酸),用硫酸渣制备铁红 的过程如图:
的过程如图:

(1)“酸溶”过程中,加入过量稀硫酸充分反应后的溶液中含有的阳离子除了 ,还有
,还有____________ (填离子符号),写出 与稀硫酸反应的离子方程式:
与稀硫酸反应的离子方程式:____________ .
(2)实验室中过滤需要用到的玻璃仪器有____________ .
(3)滤渣A的主要成分是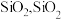 是一种常见的酸性氧化物,与
是一种常见的酸性氧化物,与 类似,可与强碱反应,写出
类似,可与强碱反应,写出 与
与 溶液反应的化学方程式:
溶液反应的化学方程式:____________ .
(4)“氧化”时,可观察到的现象为____________ .若加入的 溶液过量,则滤液B中的溶质除了
溶液过量,则滤液B中的溶质除了 外,还有
外,还有____________ (填化学式,下同);若加入的 溶液不够,则制得的铁红中可能含有的杂质为
溶液不够,则制得的铁红中可能含有的杂质为____________ .
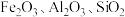 (难溶于稀硫酸),用硫酸渣制备铁红
(难溶于稀硫酸),用硫酸渣制备铁红 的过程如图:
的过程如图:
(1)“酸溶”过程中,加入过量稀硫酸充分反应后的溶液中含有的阳离子除了
 ,还有
,还有 与稀硫酸反应的离子方程式:
与稀硫酸反应的离子方程式:(2)实验室中过滤需要用到的玻璃仪器有
(3)滤渣A的主要成分是
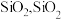 是一种常见的酸性氧化物,与
是一种常见的酸性氧化物,与 类似,可与强碱反应,写出
类似,可与强碱反应,写出 与
与 溶液反应的化学方程式:
溶液反应的化学方程式:(4)“氧化”时,可观察到的现象为
 溶液过量,则滤液B中的溶质除了
溶液过量,则滤液B中的溶质除了 外,还有
外,还有 溶液不够,则制得的铁红中可能含有的杂质为
溶液不够,则制得的铁红中可能含有的杂质为
您最近一年使用:0次
2024-02-03更新
|
83次组卷
|
2卷引用:湖南省岳阳市 岳阳县第一中学2023-2024学年高一下学期开学化学试题
名校
解题方法
3 . 以废铁屑、低品位软锰矿[主要成分有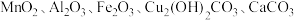 、
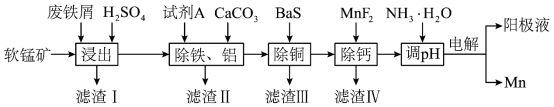
、 等]为原料,制备硫酸锰,进一步电解制备金属锰,工艺流程如图所示:
等]为原料,制备硫酸锰,进一步电解制备金属锰,工艺流程如图所示:
已知:I.部分金属阳离子以氢氧化物沉淀时的 如表:
如表:
Ⅱ.几种化合物的溶解性或溶度积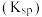 如表:
如表:
(1)基态 的价层电子排布式为
的价层电子排布式为__________ 。
(2)为去除废铁屑表面的油污可采用的方法为__________ ;“浸出”后浸出液中的 价金属阳离子有
价金属阳离子有 、
、__________ 。
(3)锰的浸出率结果如图所示。

由图可知,影响锰浸出率的因素有__________ 。
(4)“除铁、铝”过程中,浸出液需要先用试剂 处理,然后加入
处理,然后加入 ,反应后溶液的
,反应后溶液的 。试剂
。试剂 的作用是
的作用是__________ 。
(5)“除铜”过程中,当铜离子恰好完全沉淀(当离子浓度小于或等于 时视为完全沉淀)时,溶液中
时视为完全沉淀)时,溶液中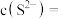
__________  。
。
(6)用惰性电极电解中性 溶液可以制得金属
溶液可以制得金属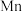 。装置如图所示。
。装置如图所示。
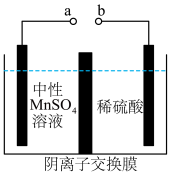
若生成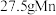 ,右室溶液中最终
,右室溶液中最终 的变化为
的变化为__________ (填“增加”或“减少”) 。
。
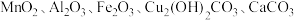 、
、 等]为原料,制备硫酸锰,进一步电解制备金属锰,工艺流程如图所示:
等]为原料,制备硫酸锰,进一步电解制备金属锰,工艺流程如图所示:
已知:I.部分金属阳离子以氢氧化物沉淀时的
 如表:
如表:| 金属阳离子 |  |  |  |  |  |
开始沉淀的 | 6.8 | 1.8 | 3.7 | 8.6 | 5.2 |
沉淀完全的 | 8.3 | 2.8 | 4.7 | 10.1 | 6.7 |
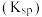 如表:
如表:| 化合物 |  |  |  |  |  |
溶解性或溶度积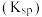 | 溶于水 | 溶于水 | 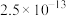 |  |  |
(1)基态
 的价层电子排布式为
的价层电子排布式为(2)为去除废铁屑表面的油污可采用的方法为
 价金属阳离子有
价金属阳离子有 、
、(3)锰的浸出率结果如图所示。

由图可知,影响锰浸出率的因素有
(4)“除铁、铝”过程中,浸出液需要先用试剂
 处理,然后加入
处理,然后加入 ,反应后溶液的
,反应后溶液的 。试剂
。试剂 的作用是
的作用是(5)“除铜”过程中,当铜离子恰好完全沉淀(当离子浓度小于或等于
 时视为完全沉淀)时,溶液中
时视为完全沉淀)时,溶液中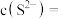
 。
。(6)用惰性电极电解中性
 溶液可以制得金属
溶液可以制得金属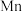 。装置如图所示。
。装置如图所示。
若生成
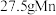 ,右室溶液中最终
,右室溶液中最终 的变化为
的变化为 。
。
您最近一年使用:0次
名校
解题方法
4 . 实验室以锈蚀程度很大的废铁屑为原料制备无水 的流程可简要表示如图:
的流程可简要表示如图: ;
;
② ;
;
③在水溶液中 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀 。
。
试回答下列问题:
(1)“酸溶”过程中发生主要反应有:① ;②
;② ;③
;③___________ (用离子方程式表示)
(2)“酸溶”需控制温度在40℃左右,最佳的加热方式是___________ 。
(3)“过滤”需要的玻璃仪器除烧杯外还有___________ 。
(4) 和
和 反应生成
反应生成 的化学方程式为
的化学方程式为___________ 。
(5)“氧化”过程可在如图所示装置中进行。 与浓盐酸反应生成
与浓盐酸反应生成 和
和 ,其离子方程式为
,其离子方程式为___________
②装置C的作用是___________ 。
③证明装置B溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是___________ 。
 的流程可简要表示如图:
的流程可简要表示如图:
 ;
;②
 ;
;③在水溶液中
 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀 。
。试回答下列问题:
(1)“酸溶”过程中发生主要反应有:①
 ;②
;② ;③
;③(2)“酸溶”需控制温度在40℃左右,最佳的加热方式是
(3)“过滤”需要的玻璃仪器除烧杯外还有
(4)
 和
和 反应生成
反应生成 的化学方程式为
的化学方程式为(5)“氧化”过程可在如图所示装置中进行。

 与浓盐酸反应生成
与浓盐酸反应生成 和
和 ,其离子方程式为
,其离子方程式为②装置C的作用是
③证明装置B溶液中
 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是
您最近一年使用:0次
2024-04-01更新
|
203次组卷
|
2卷引用:湖南省长沙市实验中学2023-2024学年高一下学期期中考试化学试题



