解题方法
1 . 下列化学或离子方程式对实验现象解释错误的是
A.氢氧化镁固体溶于饱和氯化铵溶液:Mg(OH)2+2NH =Mg2++2NH3·H2O =Mg2++2NH3·H2O |
| B.氢氧化亚铁在水中由白色沉淀迅速转化为灰绿色,最终变成红褐色沉淀:4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
C.二氧化氮通入水中红棕色消失:3NO2+H2O=2H++2NO +NO +NO |
D.电解硫酸铜溶液阳极出现无色气泡:CuSO4+H2O Cu+O2↑+H2SO4 Cu+O2↑+H2SO4 |
您最近一年使用:0次
2 . 构建知识网络是一种有效的学习方法,化学学习中的“价一类”二维图就是其中一种,如图所示是铁及其化合物的“价一类”二维图,下列有关叙述或化学方程式书写错误的是
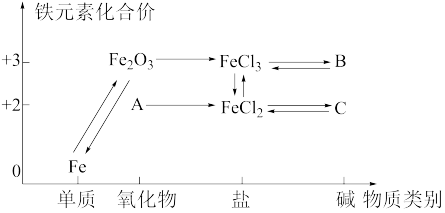
| A.物质A是氧化亚铁 |
B.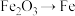 可能是 可能是 |
C. 在空气中的现象是白色沉淀迅速变成灰绿色,最终变成红褐色 在空气中的现象是白色沉淀迅速变成灰绿色,最终变成红褐色 |
D. 的反应类型只能是复分解反应 的反应类型只能是复分解反应 |
您最近一年使用:0次
2022-08-03更新
|
1556次组卷
|
7卷引用:河南省郑州市巩义,中牟,登封等六县2021-2022学年高一上学期期末联考化学试题
河南省郑州市巩义,中牟,登封等六县2021-2022学年高一上学期期末联考化学试题(已下线)第三章 铁 金属材料(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)四川省成都市第七中学2022-2023学年高一上学期期末考试化学试题(已下线)【知识图鉴】单元讲练测必修第一册第三单元01讲核心(已下线)考点巩固卷03 金属及其化合物(4大考点48题)-2024年高考化学一轮复习考点通关卷(新高考通用)新疆石河子第一中学2023-2024学年高一上学期11月月考化学试题江西省南昌市第十九中学2022-2023学年高一上学期12月第二次月考化学试卷
3 . MgO与SiO2/CuO是重要的化工材料,利用石棉尾矿(主要含有SiO2、MgO、Fe2O3、FeO、Al2O3等)可同时制备以上两种物质,其流程如图,下列叙述错误的是


| A.滤渣l的主要成分为SiO2 |
| B.滤渣2中可能含有Fe(OH)2、Fe(OH)3、Al(OH)3 |
| C.可向滤液2中加入BaCl2溶液检验杂质离子是否除尽 |
D.焙烧发生的反应方程式为:MgCO3 MgO+CO2↑ MgO+CO2↑ |
您最近一年使用:0次
2022-08-18更新
|
1281次组卷
|
5卷引用:河南省济源高级中学2023-2024学年高二上学期开学考试 化学试题
名校
解题方法
4 . 下列反应,其产物的颜色按红色、红褐色、淡黄色、蓝色顺序排列的是
①金属钠在纯氧中燃烧
②FeSO4溶液中滴入NaOH溶液,并在空气中放置一段时间
③FeCl3溶液中滴入KSCN溶液
④无水硫酸铜放入医用酒精中
①金属钠在纯氧中燃烧
②FeSO4溶液中滴入NaOH溶液,并在空气中放置一段时间
③FeCl3溶液中滴入KSCN溶液
④无水硫酸铜放入医用酒精中
| A.②③①④ | B.③②①④ | C.③①②④ | D.①②③④ |
您最近一年使用:0次
2022-01-13更新
|
1238次组卷
|
83卷引用:2016-2017学年河南省南阳一中高一上月考二化学卷
2016-2017学年河南省南阳一中高一上月考二化学卷2016-2017学年河南省南阳一中高一月考二化学卷河南省封丘县一中2018-2019学年高一上学期12月月考化学试题河南省信阳市第六高级中学2018-2019学年高一上学期第三次(1月)月考化学试题河南省洛阳市第一高级中学2021届高三上学期10月月考化学试题(已下线)2010年广东省湛江二中高二第二学期期中考试化学(文)试题(已下线)2010年湖南省浏阳一中高一上学期第三次阶段性测试化学卷(已下线)2010—2011学年湖北省沙市中学高一上学期期末考试化学试卷(已下线)2011-2012学年黑龙江省庆安三中高一上学期期末考试化学试卷(已下线)2012-2013学年山东省济宁市汶上一中高一3月质量检测化学试卷(已下线)2012-2013学年广东省佛山市佛山一中高一下学期期中考试化学试卷(已下线)2012-2013学年广东省佛山市佛山一中高一下学期期中考试化学试卷(已下线)2012-2013学年山西省晋中市昔阳中学高二下学期期末考试化学试卷(已下线)2012-2013学年辽宁省铁岭市六校第一次联合考试化学试卷(已下线)2013-2014学年江苏省宿迁市高一上学期第二次月考化学试卷(已下线)2015届甘肃省天水市秦安县二中高三上学期期中考试化学试卷2014-2015黑龙江省哈尔滨六中高一12月月考化学试卷2014-2015湖南省浏阳一中等三校高一12月联考化学试卷2014-2015黑龙江省绥化市三校高一上学期期末联考化学试卷14-15内蒙古北方重工业集团三中高一上学期期末化学试卷2014-2015广东省深圳市南山区上学期高一化学期末试卷陕西省咸阳市西藏民族学院附属中学2015-2016学年高一上期末化学卷2015-2016学年广东省肇庆市高一上学期期末考试化学试卷2015-2016学年黑龙江省绥棱一中高二6月月考化学试卷2015-2016学年甘肃省甘谷一中高一上期末化学试卷2017届辽宁省铁岭市高三上学期第一次联考化学试卷2016-2017学年江西省南昌市第二中学高一上学期期末考试化学试卷2016-2017学年黑龙江省鸡西市第十九中学高一上学期期末考试化学试卷辽宁省大石桥市第二高级中学2016-2017学年高二学业水平模拟测试化学试题青海省西宁市第四高级中学2017-2018学年高一上学期第二次月考化学试题1湖北省荆州中学2017-2018学年高一12月月考化学试题湖南省醴陵市第一中学2017-2018学年高一上学期第二次月考(12月)化学试题湖北省宜昌市葛洲坝中学2017-2018学年高一12月月考化学试题湖北省宜昌市长阳县第一高级中学2017-2018学年高一12月月考化学试题安徽省淮南市第二中学2017-2018学年高一上学期第二次月考化学试题新疆昌吉市2017-2018学年高一上学期期末考试化学试题天津市红桥区2017-2018学年高一上学期期末考试化学试题宁夏银川一中2017-2018学年高一上学期期末考试化学试题湖北省宜昌市示范高中协作体2017-2018学年高一上学期期末化学试题湖南省师范大学附属中学2017-2018学年高一上学期期末考试化学试题黑龙江省伊春中学2017-2018学年高一化学上学期期末考试题【全国百强校】青海省平安县第一高级中学2017-2018学年高一下学期期中考试(A卷)化学试题人教版2017-2018学年高一化学必修1:3.2 几种重要的金属化合物 同步测试2【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二(文)上学期10月月考化学试题山西省晋中市平遥县第二中学2018-2019学年高一上学期12月月考化学试题陕西省黄陵中学2018-2019学年高一(普通班)上学期期末考试化学试题宁夏回族自治区青铜峡市高级中学2018-2019学年高一上学期期末考试化学试题新疆石河子第二中学2018-2019学年高一上学期期末考试化学试题内蒙古开来中学2018-2019学年高二下学期期末考试化学试题辽宁省实验中学东戴河分校2020届高三上学期期初摸底考试化学试题黑龙江省佳木斯市汤原高级中学2018-2019学年高二下学期期末考试化学试题江西省赣州市会昌中学2019-2020学年高一上学期第二次月考化学试题河北省安平中学2019-2020学年高一上学期第四次月考化学试题山西省晋中市平遥县第二中学2019-2020学年高一12月月考化学试题北京市昌平区新学道临川学校2019-2020学年高一上学期期末考试化学试题福建省泉州第五中学苏教版高中化学必修1专题3 单元综合练习云南省大理市下关第一中学2019-2020学年高一上学期期末考试化学试题安徽省六安市第一中学2019-2020学年高一下学期疫情防控延期开学期间辅导测试(二)化学试题四川省南充市阆中中学2020届高三化学选择题专项训练(15)江西省上饶市2019-2020学年高一上学期期末考试 化学(自招班)试题天津市西青区2019-2020学年高一上学期期末考试化学试题(已下线)专题3.2 铁及其化合物 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》陕西省咸阳市实验中学2019-2020学年高一上学期第三次月考化学试题河北省衡水市桃城区第十四中学2019-2020学年高一下学期第六次综合测试化学试题人教版(2019)高一必修第一册 第三章 铁 金属材料 第一节 铁及其化合物黑龙江省鸡东县第二中学2020-2021学年高一上学期中考试化学试卷宁夏石嘴山市平罗中学2020-2021学年高一上学期第三次月考化学试题天津市东丽区2020-2021学年高一上学期期末考试化学试题吉林省长春市第二十中学2020-2021学年高一上学期第三次考试化学试题广西南宁市英华学校2020-2021学年高一上学期期末考试化学试题(已下线)专题3.1.3 铁盐与亚铁盐(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)吉林省长春市农安县2021-2022学年高一上学期期末考试化学试题新疆哈密市第八中学2021-2022学年高一上学期期末考试化学试题陕西省西安市阎良区关山中学2021-2022学年高一上学期第三次质量检测化学(理科)试题安徽省宿州市北方中学2021-2022学年高一上学期期末测试化学试题2023年广东省普通高中学业水平合格性考试化学科模拟测试卷(四)2023年广东省普通高中学业水平合格性考试化学科模拟仿真卷(一)天津市新华中学2022-2023学年高一上学期期末考试化学试题 云南省玉溪第一中学2022-2023学年高一下学期期中考试化学试题(已下线)专题九 铁及其化合物(已下线)合格考真题汇编8金属元素及其化合物二云南省大理白族自治州实验中学2020-2021学年高一上学期12月月考化学试题天津北京师范大学静海附属学校2023-2024学年高一上学期第三次月考化学试题
2023·北京顺义·一模
解题方法
5 . 下列方程式与所给事实不相符 的是
A.用碳酸钠溶液处理锅炉水垢: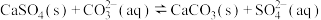 |
B. 通入水中制氯水: 通入水中制氯水: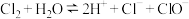 |
C.氢氧化亚铁暴露于空气中变色: |
D.常温下 氨水的pH约为11: 氨水的pH约为11: |
您最近一年使用:0次
2023-01-09更新
|
533次组卷
|
4卷引用:河南省湘豫名校联考2022-2023学年高三上学期12月期末摸底考试变式汇编(9-16)
(已下线)河南省湘豫名校联考2022-2023学年高三上学期12月期末摸底考试变式汇编(9-16)北京市顺义区2023届高三第一次统练化学试题(已下线)专题04 离子反应北京市顺义区2022-2023学年高三上学期第一次统练化学试卷
6 . 铁及其化合物在生产生活中有重要用途。某化学兴趣小组同学设计以下实验探究铁及其化合物性质。
I.“铁与水反应”的实验,并检验产物的性质:
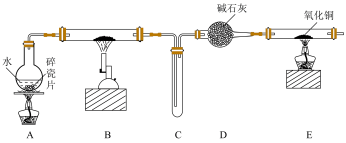
(1)A装置的作用是___________ 。
(2)B中反应的化学方程式为___________ 。
(3)点燃E处酒精灯之前应进行的操作是___________ 。
Ⅱ.制备氢氧化亚铁:设计如下实验能较长时间观察到白色Fe(OH)2沉淀,选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图。
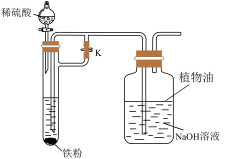
(4)植物油的作用是___________ 。
(5)实验时,先___________ (填“打开”或“关闭”)止水夹K,然后打开分液漏斗的玻璃塞和活塞,使稀硫酸与铁粉反应,一段时间后,___________ (填“打开”或“关闭”)止水夹K,制得白色Fe(OH)2沉淀,且沉淀能持续一段时间不变色。
Ⅲ.制备FeCl3:已知无水FeCl3在空气中遇水易潮解,加热易升华,实验装置如图。
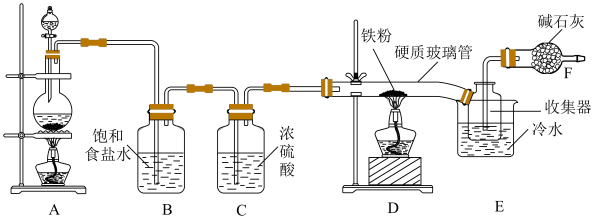
(6)饱和食盐水的作用是___________ 。
(7)装置D发生反应的化学方程式为___________ 。
(8)硬质玻璃管直接接入收集器的优点是___________ 。
(9)F装置的两个作用是___________ 、___________ 。
I.“铁与水反应”的实验,并检验产物的性质:

(1)A装置的作用是
(2)B中反应的化学方程式为
(3)点燃E处酒精灯之前应进行的操作是
Ⅱ.制备氢氧化亚铁:设计如下实验能较长时间观察到白色Fe(OH)2沉淀,选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图。

(4)植物油的作用是
(5)实验时,先
Ⅲ.制备FeCl3:已知无水FeCl3在空气中遇水易潮解,加热易升华,实验装置如图。

(6)饱和食盐水的作用是
(7)装置D发生反应的化学方程式为
(8)硬质玻璃管直接接入收集器的优点是
(9)F装置的两个作用是
您最近一年使用:0次
2023-07-24更新
|
455次组卷
|
3卷引用:河南省信阳市2022-2023学年高一上学期1月期末考试化学试题
名校
解题方法
7 . 铁的价类二维图如图所示。下列说法错误的是
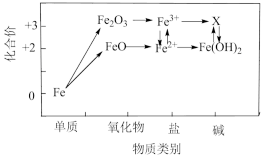

| A.Fe(OH)2→X需要加入氧化剂 | B.Fe3+→X可以加入NaOH溶液 |
| C.Fe与水蒸气在高温下反应生成Fe2O3 | D.用酸除铁锈时,Fe2O3→Fe3+ |
您最近一年使用:0次
2022-01-22更新
|
942次组卷
|
13卷引用:河南省唐河县鸿唐高级中学2023-2024学年高三上学期9月月考化学试题
河南省唐河县鸿唐高级中学2023-2024学年高三上学期9月月考化学试题广东省佛山市2021-2022学年高一上学期期末考试化学试题广东省佛山市2021-2022学年高一上学期高中教学质量检测化学试题湖北省麻城市实验高级中学2021-2022学年高一下学期2月迎春考化学试题广东省深圳市龙华区2022-2023学年高一上学期期末考试化学试题陕西省西安市第六中学2022-2023学年高一上学期期末考试化学试题广东省东莞市七校2022-2023学年高一上学期12月月考化学试题广东省广州市白云中学2022-2023学年高一上学期期末考试化学试题(已下线)第14讲 铁的氢氧化物和铁盐、亚铁盐-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)宁夏石嘴山市平罗中学2022-2023学年高一下学期3月月考化学试题广东省广州市白云区广州空港实验中学2023-2024学年高一上学期12月月考化学试题 广东省深圳市福田区福田中学2023-2024学年高一上学期期末考试化学试卷广东省茂名市信宜市2023-2024学年高一上学期1月期末考试化学试题
名校
解题方法
8 . 铁及其化合物的“价—类”二维图如图。若b,e为氯化物,下列推断不合理的是


A.b溶液中通入 可生成e 可生成e |
| B.a中加入NaOH溶液可制备c |
C.1mol c与足量的 和 和 完全反应转移 完全反应转移 个电子 个电子 |
| D.向沸腾的蒸馏水中逐滴加入饱和e溶液可得到d胶体 |
您最近一年使用:0次
2022-01-22更新
|
559次组卷
|
5卷引用:河南省郑州市部分中学2021-2022学年高一上学期期末考试化学试题
河南省郑州市部分中学2021-2022学年高一上学期期末考试化学试题福建省厦门市2021-2022学年高一上学期期末考试化学试题福建省龙岩第一中学2021-2022学年高一下学期第一次月考化学试题(已下线)3.1.1 铁的单质、氧化物及氢氧化物-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)宁夏银川唐徕回民中学2021-2022学年高一下学期3月月考化学试题
名校
解题方法
9 . 某研究小组欲探究 能否与
能否与 溶液反应。
溶液反应。
【查阅资料】
i. 具有较强的还原性,
具有较强的还原性, 具有较强的氧化性。
具有较强的氧化性。
ii. 遇
遇 可生成
可生成 ,
, 溶液呈血红色,可用于
溶液呈血红色,可用于 的检验。
的检验。
【提出猜想】
(1)小组同学经过讨论后,认为 溶液可以与
溶液可以与 溶液反应,请从化合价的角度加以解释:
溶液反应,请从化合价的角度加以解释:___________ 。
【设计实验】
(2)实验I:在试管中加入 溶液和
溶液和 溶液,再加入
溶液,再加入 溶液,发现溶液
溶液,发现溶液_____ ,小组同学认为 和
和 溶液反应生成了
溶液反应生成了 。
。
(3)甲同学注意到盛放 溶液的试剂瓶中有空气,因此不同意该结论,他的理由是
溶液的试剂瓶中有空气,因此不同意该结论,他的理由是______ 。
重新设计实验:
实验II:在试管中加入 溶液,然后加入
溶液,然后加入 溶液,发现溶液无明显变化,再加入
溶液,发现溶液无明显变化,再加入 溶液,发现溶液变红。
溶液,发现溶液变红。
【获得结论】
(4)过氧化氢___________ (填“能”或者“不能”)氧化 。
。
【发现异常】
乙同学继续向实验II所得溶液中滴加溶液,发现溶液褪色。
小组同学经过重新查阅资料后,发现可以将 氧化为
氧化为 。乙同学设计实验III并证实了该资料中的说法。
。乙同学设计实验III并证实了该资料中的说法。
(5)补全实验III的方案:在试管中加入 溶液,加入
溶液,加入 溶液,再加入
溶液,再加入___________ ,产生___________ 。
【总结反思】
(6)小组同学经过讨论后,提出了 的检验方法:取待测液于试管中,
的检验方法:取待测液于试管中,___________ ,证明待测液含有 。
。
(7)从上述实验中可以得出结论,在物质性质的检验中,应注意___________ (至少写出两条)对实验结果的影响。
 能否与
能否与 溶液反应。
溶液反应。【查阅资料】
i.
 具有较强的还原性,
具有较强的还原性, 具有较强的氧化性。
具有较强的氧化性。ii.
 遇
遇 可生成
可生成 ,
, 溶液呈血红色,可用于
溶液呈血红色,可用于 的检验。
的检验。【提出猜想】
(1)小组同学经过讨论后,认为
 溶液可以与
溶液可以与 溶液反应,请从化合价的角度加以解释:
溶液反应,请从化合价的角度加以解释:【设计实验】
(2)实验I:在试管中加入
 溶液和
溶液和 溶液,再加入
溶液,再加入 溶液,发现溶液
溶液,发现溶液 和
和 溶液反应生成了
溶液反应生成了 。
。(3)甲同学注意到盛放
 溶液的试剂瓶中有空气,因此不同意该结论,他的理由是
溶液的试剂瓶中有空气,因此不同意该结论,他的理由是重新设计实验:
实验II:在试管中加入
 溶液,然后加入
溶液,然后加入 溶液,发现溶液无明显变化,再加入
溶液,发现溶液无明显变化,再加入 溶液,发现溶液变红。
溶液,发现溶液变红。【获得结论】
(4)过氧化氢
 。
。【发现异常】
乙同学继续向实验II所得溶液中滴加溶液,发现溶液褪色。
小组同学经过重新查阅资料后,发现可以将
 氧化为
氧化为 。乙同学设计实验III并证实了该资料中的说法。
。乙同学设计实验III并证实了该资料中的说法。(5)补全实验III的方案:在试管中加入
 溶液,加入
溶液,加入 溶液,再加入
溶液,再加入【总结反思】
(6)小组同学经过讨论后,提出了
 的检验方法:取待测液于试管中,
的检验方法:取待测液于试管中, 。
。(7)从上述实验中可以得出结论,在物质性质的检验中,应注意
您最近一年使用:0次
2021-11-07更新
|
1003次组卷
|
4卷引用:河南省安阳市第一中学2022-2023学年高一上学期12月月考化学试题
10 . 常温下,在pH=1的某溶液中可能有Na+、Fe3+、Fe2+、I−、Cl−、 中的几种,现取100mL该溶液进行如下实验。根据实验结果,下列判断正确的是
中的几种,现取100mL该溶液进行如下实验。根据实验结果,下列判断正确的是

 中的几种,现取100mL该溶液进行如下实验。根据实验结果,下列判断正确的是
中的几种,现取100mL该溶液进行如下实验。根据实验结果,下列判断正确的是
| A.Fe2+、I−、Cl−三种离子一定存在 |
B. 一定不存在,不能确定Na+和Cl−是否存在 一定不存在,不能确定Na+和Cl−是否存在 |
| C.Fe3+与Fe2+至少有一种 |
| D.该溶液中c(Cl−)至少为0.2mol⋅L‑1 |
您最近一年使用:0次
2021-01-04更新
|
871次组卷
|
15卷引用:河南省南阳市第一中学校2020-2021学年高二上学期第三次考试化学试题
河南省南阳市第一中学校2020-2021学年高二上学期第三次考试化学试题河南省信阳市2022届高三第二次质量检测化学试题河南省南阳市第一完全学校2020-2021学年高二上学期第二次月考化学试题黑龙江省哈尔滨师范大学附属中学2017届高三第四次模拟考试理综化学试题内蒙古包头市第九中学2016-2017学年高二下学期期末考试化学试题吉林省长春市实验中学2019-2020学年高二下学期期末考试化学试题黑龙江省牡丹江市第一高级中学2021届高三上学期开学考试化学试题吉林省实验中学2019-2020学年高二下学期期末考试化学试题黑龙江省大庆市铁人中学2021届高三上学期期中考试化学试题福建省福州第一中学2021届高三上学期期中考试化学试题黑龙江省八校2021届高三摸底考试化学试题山东省泰安市新泰第一中学(东校)2020-2021学年高二上学期第二次质量检测化学试题黑龙江省嫩江市高级中学2021届高三上学期期中考试化学试题(已下线)学科网2020年高三11月大联考考后强化卷(新课标Ⅱ卷)天津市静海区第一中学2021-2022学年高三上学期(9月)学生学业能力调研化学试题



