解题方法
1 . 钠、铁及它们的化合物在生产、生活中有着重要的用途。
(1)某汽车安全气囊的产气药剂主要含有 、
、 、
、 、
、 等物质。当汽车发生碰撞时,
等物质。当汽车发生碰撞时, 迅速分解产生
迅速分解产生 和Na,同时放出大量的热,
和Na,同时放出大量的热, 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。
① 是助氧化剂,可处理产生的Na,其中氯元素的化合价是
是助氧化剂,可处理产生的Na,其中氯元素的化合价是___________ 。
② 是主氧化剂,也可处理产生的Na,反应为
是主氧化剂,也可处理产生的Na,反应为 ,反应中
,反应中 是
是___________ (填“还原产物”或“氧化产物”)。
(2)铁及其重要化合物之间的部分转化关系如图所示。___________ (填序号);
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
②实现Fe转化为Fe2+可选用足量的___________ (填序号);
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
③在点燃的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为血红色,证明产物为FeCl3,写出氯气和铁反应的化学方程式为___________ 。
④在FeSO4中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为___________ ,此过程中发生的氧化还原反应为(用化学方程式表达)___________ 。
(1)某汽车安全气囊的产气药剂主要含有
 、
、 、
、 、
、 等物质。当汽车发生碰撞时,
等物质。当汽车发生碰撞时, 迅速分解产生
迅速分解产生 和Na,同时放出大量的热,
和Na,同时放出大量的热, 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。①
 是助氧化剂,可处理产生的Na,其中氯元素的化合价是
是助氧化剂,可处理产生的Na,其中氯元素的化合价是②
 是主氧化剂,也可处理产生的Na,反应为
是主氧化剂,也可处理产生的Na,反应为 ,反应中
,反应中 是
是(2)铁及其重要化合物之间的部分转化关系如图所示。
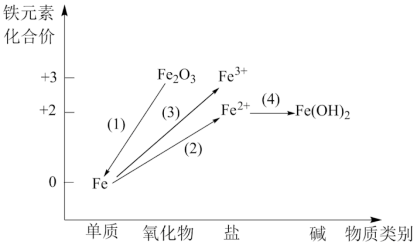
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
②实现Fe转化为Fe2+可选用足量的
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
③在点燃的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为血红色,证明产物为FeCl3,写出氯气和铁反应的化学方程式为
④在FeSO4中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为
您最近一年使用:0次
2 . 已知A为淡黄色固体,T、R为日常生活中两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体M。
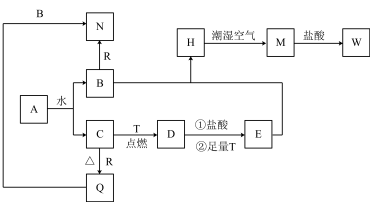
(1)写出下列物质的化学式:A:________ ,D:________ ,W:________ 。
(2)按要求写出下列方程式:
①A和水反应的化学方程式:___________ 。
②D能与HI溶液反应,该反应的离子方程式:___________ 。
③H在潮湿空气中变成M的化学方程式:___________ 。
(3)检验W中阳离子的方法是:___________ 。

(1)写出下列物质的化学式:A:
(2)按要求写出下列方程式:
①A和水反应的化学方程式:
②D能与HI溶液反应,该反应的离子方程式:
③H在潮湿空气中变成M的化学方程式:
(3)检验W中阳离子的方法是:
您最近一年使用:0次
3 . 铁及其化合物在生产生活中有重要用途。某化学兴趣小组同学设计以下实验探究铁及其化合物性质。
I.“铁与水反应”的实验,并检验产物的性质:
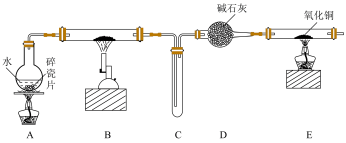
(1)A装置的作用是___________ 。
(2)B中反应的化学方程式为___________ 。
(3)点燃E处酒精灯之前应进行的操作是___________ 。
Ⅱ.制备氢氧化亚铁:设计如下实验能较长时间观察到白色Fe(OH)2沉淀,选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图。
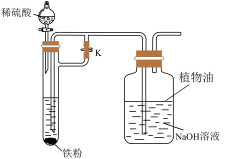
(4)植物油的作用是___________ 。
(5)实验时,先___________ (填“打开”或“关闭”)止水夹K,然后打开分液漏斗的玻璃塞和活塞,使稀硫酸与铁粉反应,一段时间后,___________ (填“打开”或“关闭”)止水夹K,制得白色Fe(OH)2沉淀,且沉淀能持续一段时间不变色。
Ⅲ.制备FeCl3:已知无水FeCl3在空气中遇水易潮解,加热易升华,实验装置如图。
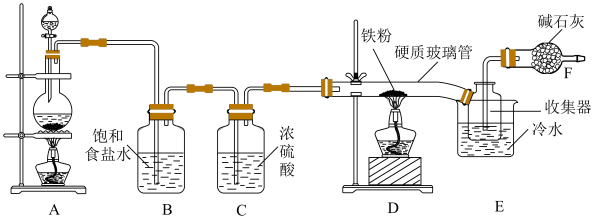
(6)饱和食盐水的作用是___________ 。
(7)装置D发生反应的化学方程式为___________ 。
(8)硬质玻璃管直接接入收集器的优点是___________ 。
(9)F装置的两个作用是___________ 、___________ 。
I.“铁与水反应”的实验,并检验产物的性质:

(1)A装置的作用是
(2)B中反应的化学方程式为
(3)点燃E处酒精灯之前应进行的操作是
Ⅱ.制备氢氧化亚铁:设计如下实验能较长时间观察到白色Fe(OH)2沉淀,选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图。

(4)植物油的作用是
(5)实验时,先
Ⅲ.制备FeCl3:已知无水FeCl3在空气中遇水易潮解,加热易升华,实验装置如图。

(6)饱和食盐水的作用是
(7)装置D发生反应的化学方程式为
(8)硬质玻璃管直接接入收集器的优点是
(9)F装置的两个作用是
您最近一年使用:0次
2023-07-24更新
|
455次组卷
|
3卷引用:河南省信阳市2022-2023学年高一上学期1月期末考试化学试题
名校
4 . 以化合价为纵坐标,物质类别为横坐标的图像称为价类二维图,在地壳中的含量仅次于铝,居第四位的元素价类二维图如图所示,下列说法错误的是
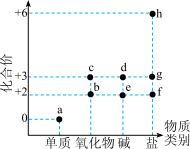

| A.a与水常温下几乎不发生反应,但在高温下可生成c |
| B.e可通过化合反应转化为d |
| C.c的用途之一是做颜料 |
| D.h的某种盐是具备净水和消毒双重功能的水处理剂 |
您最近一年使用:0次
5 . 铁与空气接触时会形成氧化物,如一块低碳钢可以被三种氧化物膜所覆盖与金属接触的一侧是FeO,与空气接触的一侧是 ,而中间则是
,而中间则是 。
。
(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的___________ (填化学式)。
(2) 的一种用途是
的一种用途是___________ 。(填“用作油漆、涂料 ”或“磁电机”);
(3)FeO可作化妆品中的色素,它还能进行一系列转化: 。
。
① 时应加入的试剂是
时应加入的试剂是___________ (填“H2SO4”或“Na2SO4”)。
②“速力菲”(主要有效成分是 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入___________ (填“KSCN”或“K2SO4”),若出现___________ (填“红色”或“浅绿色”)现象,则证明该药物已变质。
③在 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成___________ (填“红褐色”或“黄色”),其中沉淀颜色发生变化的化学方程式为___________ 。
 ,而中间则是
,而中间则是 。
。(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的
(2)
 的一种用途是
的一种用途是(3)FeO可作化妆品中的色素,它还能进行一系列转化:
 。
。①
 时应加入的试剂是
时应加入的试剂是②“速力菲”(主要有效成分是
 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入③在
 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
您最近一年使用:0次
6 . 氯、铁及其化合物在很多领域有重要的用途。
Ⅰ.“84消毒液”能有效杀灭新冠病毒,其有效成分是NaClO。已知某“84消毒液”中NaClO的物质的量浓度为4.00 mol/L。
(1)某化学实验小组用该品牌消毒液配制480 mL0.20 mol/L的NaClO稀溶液,需要此消毒液___________ mL。
(2)完成上述实验必须用到的仪器有玻璃棒、烧杯、胶头滴管、量筒、还有___________ 。
(3)请写出用氢氧化钠溶液和氯气反应制备“84消毒液”的化学方程式:___________ 。
Ⅱ.某工厂的工业废水中含有大量的FeSO4和较多的Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收FeSO4和金属铜。请根据以下流程图,回答下列问题:

(4)操作a的名称为___________ 。
(5)工业上常用绿矾(FeSO4·7H2O)处理工业废水中有毒的重铬酸根离子( )。反应的离子方程式为
)。反应的离子方程式为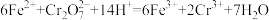 。该反应中
。该反应中___________ 是还原剂;若消耗1 mol Cr2O ,则转移电子的物质的量为
,则转移电子的物质的量为___________ mol。
(6)若取2 mL溶液⑥加入试管中,然后滴加氢氧化钠溶液,产生的现象是___________ 。
Ⅰ.“84消毒液”能有效杀灭新冠病毒,其有效成分是NaClO。已知某“84消毒液”中NaClO的物质的量浓度为4.00 mol/L。
(1)某化学实验小组用该品牌消毒液配制480 mL0.20 mol/L的NaClO稀溶液,需要此消毒液
(2)完成上述实验必须用到的仪器有玻璃棒、烧杯、胶头滴管、量筒、还有
(3)请写出用氢氧化钠溶液和氯气反应制备“84消毒液”的化学方程式:
Ⅱ.某工厂的工业废水中含有大量的FeSO4和较多的Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收FeSO4和金属铜。请根据以下流程图,回答下列问题:

(4)操作a的名称为
(5)工业上常用绿矾(FeSO4·7H2O)处理工业废水中有毒的重铬酸根离子(
 )。反应的离子方程式为
)。反应的离子方程式为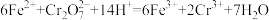 。该反应中
。该反应中 ,则转移电子的物质的量为
,则转移电子的物质的量为(6)若取2 mL溶液⑥加入试管中,然后滴加氢氧化钠溶液,产生的现象是
您最近一年使用:0次
解题方法
7 . 已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体M。
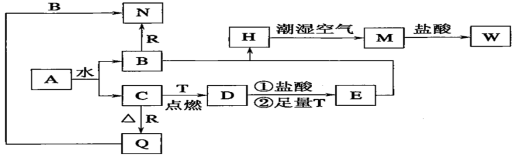
(1)写出下列物质的化学式:A:_______ ,D:_______ ,R:_______ 。
(2)按要求写下列反应方程式:
①H在潮湿空气中变成M的过程中的化学方程式:_______ ;
②B和R反应生成N的离子方程式:_______ ;
③D与盐酸反应的离子方程式:_______ 。

(1)写出下列物质的化学式:A:
(2)按要求写下列反应方程式:
①H在潮湿空气中变成M的过程中的化学方程式:
②B和R反应生成N的离子方程式:
③D与盐酸反应的离子方程式:
您最近一年使用:0次
名校
解题方法
8 . 如图所示为部分物质(或其溶液)间的转化关系(除水外,其他反应物、生成物均已列出)。已知 为紫红色金属单质,
为紫红色金属单质, 为能使带火星的木条复燃的气体,
为能使带火星的木条复燃的气体, 为红褐色沉淀,
为红褐色沉淀, 的焰色试验呈紫色(透过蓝色钴玻璃),回答下列问题。
的焰色试验呈紫色(透过蓝色钴玻璃),回答下列问题。

(1)写出下列物质的化学式:A___________ 、G___________ 。
(2)I加热分解产生的固体产物俗称___________ ,写出其一种用途:___________ 。
(3)F与H作用生成I的化学方程式为___________ ; 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
(4)除去D溶液中混有的J,最好使用的方法是___________ (用离子方程式表示)。
 为紫红色金属单质,
为紫红色金属单质, 为能使带火星的木条复燃的气体,
为能使带火星的木条复燃的气体, 为红褐色沉淀,
为红褐色沉淀, 的焰色试验呈紫色(透过蓝色钴玻璃),回答下列问题。
的焰色试验呈紫色(透过蓝色钴玻璃),回答下列问题。
(1)写出下列物质的化学式:A
(2)I加热分解产生的固体产物俗称
(3)F与H作用生成I的化学方程式为
 与
与 反应的离子方程式为
反应的离子方程式为(4)除去D溶液中混有的J,最好使用的方法是
您最近一年使用:0次
9 . 铁及其化合物在生产生活中有重要用途。某化学兴趣小组同学设计以下实验探究铁及其化合物性质。
Ⅰ.氢氧化亚铁的制备:
两组同学分别设计如下实验探究能较长时间观察到白色Fe(OH)2沉淀的制取方法。
A组实验:用NaOH溶液和FeSO4溶液直接反应。(如图1)
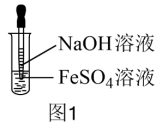
(1) FeSO4可由铁粉还原Fe2(SO4)3制得,反应的离子方程式是:_______ 。
(2)该方法能观察到白色Fe(OH)2沉淀,但沉淀颜色快速发生变化,其颜色变化为_______ 。
B组实验:选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图2。

(3)实验时,先_______ (填“打开”或“关闭”)止水夹K,然后打开分液漏斗的玻璃塞和活塞,使稀硫酸与铁粉反应,一段时间后, _______ (填“打开”或“关闭”)止水夹K,制得白色Fe(OH)2沉淀,且沉淀能持续一段时间不变色。
Ⅱ.“铁与水反应”的实验,并检验产物的性质:

(4)①A装置的作用是_______ B中反应的化学方程式为_______ 。
②D的作用是_______ 。
③点燃E处酒精灯之前应进行的操作是_______ 。
Ⅰ.氢氧化亚铁的制备:
两组同学分别设计如下实验探究能较长时间观察到白色Fe(OH)2沉淀的制取方法。
A组实验:用NaOH溶液和FeSO4溶液直接反应。(如图1)

(1) FeSO4可由铁粉还原Fe2(SO4)3制得,反应的离子方程式是:
(2)该方法能观察到白色Fe(OH)2沉淀,但沉淀颜色快速发生变化,其颜色变化为
B组实验:选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图2。

(3)实验时,先
Ⅱ.“铁与水反应”的实验,并检验产物的性质:

(4)①A装置的作用是
②D的作用是
③点燃E处酒精灯之前应进行的操作是
您最近一年使用:0次
10 . 下图中A~J均为中学化学中常见的物质,它们之间有如下转化关系。其中,A、D为金属单质,A 是地壳中含量最多的金属。(反应过程中生成的水及其它产物已略去),D的合金目前用量最大用途最广。请回答以下问题:
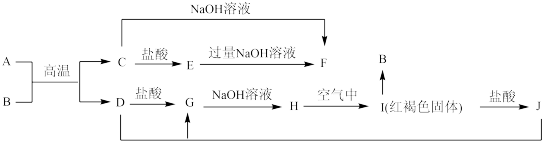
(1)C是_______ ,H是_______ (填化学式)。
(2)写出J与D反应转化为G的离子方程式:_______ 。
(3)A在常温下也可与NaOH溶液反应生成F,写出此反应的化学方程式:_______ 。
(4)写出H在空气中生成I对应方程式_______ 。
(5)写出一种B的用途_______ 。

(1)C是
(2)写出J与D反应转化为G的离子方程式:
(3)A在常温下也可与NaOH溶液反应生成F,写出此反应的化学方程式:
(4)写出H在空气中生成I对应方程式
(5)写出一种B的用途
您最近一年使用:0次



