1 . 为探究铁和铁的化合物的一些化学性质,某学生实验小组设计以下实验。
(1)如下图:
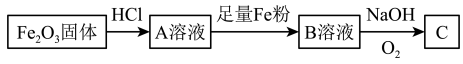
①Fe2O3和HCl的离子方程式是_______ 。
②B→C变化中可看到的现象是_______ 。发生氧化还原反应的化学方程式是_______ 。
(2)某班同学用如下实验探究 、
、 的性质。回答下列问题:
的性质。回答下列问题:
①分别取一定量氯化铁、氯化亚铁固体,均配制成100mL0.1mol/L的溶液。在配制FeCl2溶液时需加入少量铁屑,其目的是_______ 。
②某同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明 可将
可将 氧化。FeCl2溶液与氯水反应的离子方程式为
氧化。FeCl2溶液与氯水反应的离子方程式为_______ 。
(3)某实验小组探究氯水与铁的反应。(实验过程)操作过程及实验现象如图所示。

①实验i中产生少量无色气体,该气体可能是_______ 。
②(2)实验ii中观察到溶液变为红色,可推知上层清液中含有Fe3+,则试剂X是_______ (填字母)。
a.KSCN溶液 b.NaCl溶液
③实验iii中观察到溶液无明显变化,可推知上层清液中不含Fe3+,其原因是_______ (用离子方程式表示)。
(反思评价)
④甲同学认为上层清液中的Fe3+是由Cl2与Fe2+反应生成。乙同学认为还有其他可能性,请写出其中一种:_______ 。
(1)如下图:

①Fe2O3和HCl的离子方程式是
②B→C变化中可看到的现象是
(2)某班同学用如下实验探究
 、
、 的性质。回答下列问题:
的性质。回答下列问题:①分别取一定量氯化铁、氯化亚铁固体,均配制成100mL0.1mol/L的溶液。在配制FeCl2溶液时需加入少量铁屑,其目的是
②某同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明
 可将
可将 氧化。FeCl2溶液与氯水反应的离子方程式为
氧化。FeCl2溶液与氯水反应的离子方程式为(3)某实验小组探究氯水与铁的反应。(实验过程)操作过程及实验现象如图所示。

①实验i中产生少量无色气体,该气体可能是
②(2)实验ii中观察到溶液变为红色,可推知上层清液中含有Fe3+,则试剂X是
a.KSCN溶液 b.NaCl溶液
③实验iii中观察到溶液无明显变化,可推知上层清液中不含Fe3+,其原因是
(反思评价)
④甲同学认为上层清液中的Fe3+是由Cl2与Fe2+反应生成。乙同学认为还有其他可能性,请写出其中一种:
您最近一年使用:0次
2022-01-18更新
|
182次组卷
|
2卷引用:海南省华东师范大学第二附属中学乐东黄流中学2023-2024学年高一下学期开学化学试题
名校
2 . 铁及其重要化合物之间的部分转化关系如图所示。

(1)下列金属矿物中用于冶炼金属铁的是_______ (填序号);
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
(2)实现Fe转化为Fe2+可选用足量的_______ (填序号);
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
(3)在点燃的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为_______ 色,证明产物为FeCl3,写出氯气和铁反应的化学方程式为_______ ;
(4)某同学将FeSO4溶液与NaOH溶液混合,未观察到白色沉淀,分析原因是生成的Fe(OH)2易被空气中的O2氧化,请你设计一个防止Fe(OH)2被O2氧化的实验方案_______

(1)下列金属矿物中用于冶炼金属铁的是
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
(2)实现Fe转化为Fe2+可选用足量的
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
(3)在点燃的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为
(4)某同学将FeSO4溶液与NaOH溶液混合,未观察到白色沉淀,分析原因是生成的Fe(OH)2易被空气中的O2氧化,请你设计一个防止Fe(OH)2被O2氧化的实验方案
您最近一年使用:0次
2021-04-06更新
|
520次组卷
|
3卷引用:海南省儋州市第二中学2020-2021学年高一下学期3月月考化学(合格考)试题
3 . 铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
(1)Fe跟Cl2在一定条件下反应,将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成_______ 色。
b.向另一支试管中滴加NaOH溶液,现象为_______ ,反应的离子方程式是_______ 。
(2)若Fe2+溶液中存在Fe3+,除杂的方法是:_______ ;该反应的离子方程式为:_______ 。
(3)Fe(OH)2悬浊液在空气中被氧化的过程现象为___ ,请写出反应的化学方程式_____
(1)Fe跟Cl2在一定条件下反应,将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.向另一支试管中滴加NaOH溶液,现象为
(2)若Fe2+溶液中存在Fe3+,除杂的方法是:
(3)Fe(OH)2悬浊液在空气中被氧化的过程现象为
您最近一年使用:0次
名校
4 . 为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验。
(1)往A溶液中分别滴入几滴KSCN溶液,溶液的颜色__________ ,
(2)根据上述过程写出有关反应的离子方程式:Fe3O4→A_________________ ,A→B ___________ 。
(3)向B溶液中加入NaOH溶液,可看到的现象是_______________________________________ ,此过程中发生的氧化还原反应化学方程式为__________________________________ 。
(4)将A的饱和溶液滴入沸水中并不断加热,可制得_______________ 胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为___________ 效应。

(1)往A溶液中分别滴入几滴KSCN溶液,溶液的颜色
(2)根据上述过程写出有关反应的离子方程式:Fe3O4→A
(3)向B溶液中加入NaOH溶液,可看到的现象是
(4)将A的饱和溶液滴入沸水中并不断加热,可制得
您最近一年使用:0次



