名校
1 . 铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。小组同学利用化学实验进行菠菜中铁元素的检验和铁元素含量测定。
实验1.菠菜中铁元素的检验

(1)操作1的名称是_______ 。
(2)溶液②为浅红色,说明溶液①中含有_______ (填离子符号)。
(3)溶液③中_______ (填实验现象),证明溶液②中还含有 ,其推理过程是
,其推理过程是_______ 。
实验2.测定菠菜中铁元素的含量
i.沉淀法:向实验1滤液①中加入足量NaOH溶液,过滤、洗涤沉淀、加热烘干、称量。
(4)滤液①中加入足量NaOH溶液后生成的沉淀有_______ 、_______ ;在沉淀生成或后续处理过程中,沉淀转化发生的氧化还原 反应为_______ 。
ii.比色法:利用色度传感器测定其对光的透过率或者吸收率,颜色越深,吸收率越高。
测得不同浓度 的标准液吸收率如下图。
的标准液吸收率如下图。

(5) 菠菜处理后得到溶液(3)
菠菜处理后得到溶液(3) ,色度传感器测得吸收率为上图中a点,则
,色度传感器测得吸收率为上图中a点,则
_______  ,
, 菠菜中含铁
菠菜中含铁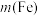 =
=_______ g。
实验1.菠菜中铁元素的检验

(1)操作1的名称是
(2)溶液②为浅红色,说明溶液①中含有
(3)溶液③中
 ,其推理过程是
,其推理过程是实验2.测定菠菜中铁元素的含量
i.沉淀法:向实验1滤液①中加入足量NaOH溶液,过滤、洗涤沉淀、加热烘干、称量。
(4)滤液①中加入足量NaOH溶液后生成的沉淀有
ii.比色法:利用色度传感器测定其对光的透过率或者吸收率,颜色越深,吸收率越高。
测得不同浓度
 的标准液吸收率如下图。
的标准液吸收率如下图。
(5)
 菠菜处理后得到溶液(3)
菠菜处理后得到溶液(3) ,色度传感器测得吸收率为上图中a点,则
,色度传感器测得吸收率为上图中a点,则
 ,
, 菠菜中含铁
菠菜中含铁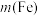 =
=
您最近一年使用:0次
2023-01-05更新
|
244次组卷
|
2卷引用:北京市大兴区2022-2023学年高一上学期期末考试化学试题
2 . 回答下列问题
(1)向少量新制的氯化亚铁溶液中,加入几滴硫氰化钾溶液,溶液_______ 色;再加几滴氯水,溶液呈_______ 色,该实验体现了Fe2+的_______ 性。已知Fe(SCN)3中N为−3价,可推测S元素的化合价为_______ 价。
(2)FeCl2溶液与Cl2反应的化学方程式为_______ ,上述生成Fe(SCN)3反应的离子方程式为_______ 。
(3)除去FeCl2溶液中的少量FeCl3,可采用的试剂是_______ (填写化学式),该反应的离子方程式为_______ 。
(4)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为_______ ,反应的化学方程式为_______ 。
(1)向少量新制的氯化亚铁溶液中,加入几滴硫氰化钾溶液,溶液
(2)FeCl2溶液与Cl2反应的化学方程式为
(3)除去FeCl2溶液中的少量FeCl3,可采用的试剂是
(4)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为
您最近一年使用:0次
解题方法
3 . Ⅰ.碳酸亚铁在空气中灼烧得到铁的氧化物A和一种气体。某学习小组为了探究该氧化物A的组成设计如下实验方案:
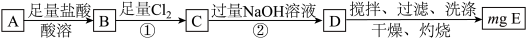
(1)若该方案中①通入 不足量,小组成员认为可以通过在空气中充分搅拌D而最终实现准确测定,他的依据是
不足量,小组成员认为可以通过在空气中充分搅拌D而最终实现准确测定,他的依据是_______ (用化学方程式表示)。
(2)若氧化物A的质量是7.84g,E的质量为8.00g,根据数据计算化合物A的化学式为_______ 。
Ⅱ.高铁酸钾( )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,已知
)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,已知 在
在 催化下会分解,在强碱性条件下稳定。高铁酸钾(
催化下会分解,在强碱性条件下稳定。高铁酸钾( )生产流程如下:
)生产流程如下:
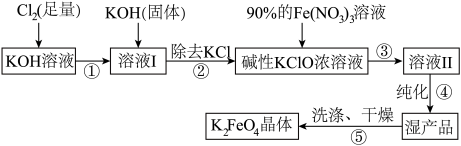
(3)在溶液Ⅰ中加入KOH固体的目的是_______。
(4)写出③反应的离子方程式_______ 。
(5)制备 时,将90%的
时,将90%的 溶液缓缓滴加到碱性的KClO浓溶液中,并且不断搅拌,采用这种混合方式的原因是
溶液缓缓滴加到碱性的KClO浓溶液中,并且不断搅拌,采用这种混合方式的原因是_______ 。
(6) 在酸性或弱碱性条件下能与水反应生成一种胶体和一种氧化性气体单质,该气体单质为
在酸性或弱碱性条件下能与水反应生成一种胶体和一种氧化性气体单质,该气体单质为_______ (写出化学式)。
(7) 净水时能吸附悬浮物的原因是
净水时能吸附悬浮物的原因是_______ 。
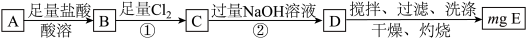
(1)若该方案中①通入
 不足量,小组成员认为可以通过在空气中充分搅拌D而最终实现准确测定,他的依据是
不足量,小组成员认为可以通过在空气中充分搅拌D而最终实现准确测定,他的依据是(2)若氧化物A的质量是7.84g,E的质量为8.00g,根据数据计算化合物A的化学式为
Ⅱ.高铁酸钾(
 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,已知
)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,已知 在
在 催化下会分解,在强碱性条件下稳定。高铁酸钾(
催化下会分解,在强碱性条件下稳定。高铁酸钾( )生产流程如下:
)生产流程如下:
(3)在溶液Ⅰ中加入KOH固体的目的是_______。
A.与溶液Ⅰ中过量的 继续反应,生成更多的KClO 继续反应,生成更多的KClO |
| B.KOH固体溶解时会放出较多的热量,有利于提高KClO产率 |
| C.为下一步反应提供碱性的环境 |
D.使 转化为KClO 转化为KClO |
(5)制备
 时,将90%的
时,将90%的 溶液缓缓滴加到碱性的KClO浓溶液中,并且不断搅拌,采用这种混合方式的原因是
溶液缓缓滴加到碱性的KClO浓溶液中,并且不断搅拌,采用这种混合方式的原因是(6)
 在酸性或弱碱性条件下能与水反应生成一种胶体和一种氧化性气体单质,该气体单质为
在酸性或弱碱性条件下能与水反应生成一种胶体和一种氧化性气体单质,该气体单质为(7)
 净水时能吸附悬浮物的原因是
净水时能吸附悬浮物的原因是
您最近一年使用:0次
2023-01-04更新
|
512次组卷
|
3卷引用:辽宁省重点高中2022-2023学年高一上学期期末联考化学试题
4 . 某小组设计实验探究 是否能与
是否能与 形成络离子。查阅资料:向难溶电解质中加入具有不同离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。实验表明:“盐效应”与离子浓度、离子所带电量有关。分别取等量的纯
形成络离子。查阅资料:向难溶电解质中加入具有不同离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。实验表明:“盐效应”与离子浓度、离子所带电量有关。分别取等量的纯 进行实验,实验结果如图所示:
进行实验,实验结果如图所示:
 是否能与
是否能与 形成络离子。查阅资料:向难溶电解质中加入具有不同离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。实验表明:“盐效应”与离子浓度、离子所带电量有关。分别取等量的纯
形成络离子。查阅资料:向难溶电解质中加入具有不同离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。实验表明:“盐效应”与离子浓度、离子所带电量有关。分别取等量的纯 进行实验,实验结果如图所示:
进行实验,实验结果如图所示: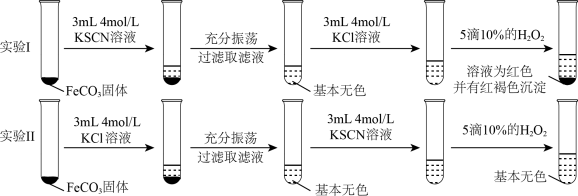
A.实验Ⅱ中,KCl溶液能促进 溶解 溶解 | B.相同浓度下,KSCN溶液盐效应大于KCl溶液 |
| C.滤液中+2价铁离子总浓度:实验Ⅰ=实验Ⅱ | D.实验表明, 和 和 不能形成络离子 不能形成络离子 |
您最近一年使用:0次
2023-01-03更新
|
923次组卷
|
5卷引用:湖南省长沙市长郡中学2022-2023学年高三上学期月考(四)化学试题
湖南省长沙市长郡中学2022-2023学年高三上学期月考(四)化学试题山东省沂水县第一中学2022-2023学年高一上学期期末考试化学试题(已下线)专题11 化学实验基础(练)-2023年高考化学二轮复习讲练测(新高考专用)湖南省醴陵市第一中学2023届高三第六次月考化学试题章末检测卷(三) 物质的性质与转化
名校
5 . Ⅰ.根据铁及其化合物的相关性质,回答下列问题:
(1)Fe(OH)2白色沉淀,在空气中颜色变化为_______ ,反应方程式为_______ ,因此制取Fe(OH)2要用特殊方法。
(2)在FeSO4溶液中滴加入少量KSCN溶液,溶液颜色_______ ,再滴入几滴氯水,溶液颜色_______ ,因为有_______ 生成。
Ⅱ.化学方法除杂选择试剂的原则是:不增、不减、不繁。
(3)现有含少量FeCl2杂质的FeCl3溶液,为了除去Fe2+离子,应该向溶液中滴加适量的_______ (填试剂名称),其反应的离子方程式为_______ 。
(4)现有含少量FeCl3杂质的FeCl2溶液,为了除去Fe3+离子,应该向溶液中加_______ ,其反应的离子方程式为_______ 。证明Fe3+已除干净的方法为_______ 。
(1)Fe(OH)2白色沉淀,在空气中颜色变化为
(2)在FeSO4溶液中滴加入少量KSCN溶液,溶液颜色
Ⅱ.化学方法除杂选择试剂的原则是:不增、不减、不繁。
(3)现有含少量FeCl2杂质的FeCl3溶液,为了除去Fe2+离子,应该向溶液中滴加适量的
(4)现有含少量FeCl3杂质的FeCl2溶液,为了除去Fe3+离子,应该向溶液中加
您最近一年使用:0次
6 . 铁及其化合物在生产和生活中起到重要的作用。请回答下列问题:
(1)人体对Fe2+的吸收效果更好,但人体中时刻进行着Fe2+ Fe3+的转化。服用补铁口服剂时,配合服用维生素C会增强人体对铁的吸收效果,在此过程中维生素C的作用是起
Fe3+的转化。服用补铁口服剂时,配合服用维生素C会增强人体对铁的吸收效果,在此过程中维生素C的作用是起_____ 。
(2)钢铁烤蓝是在钢铁表面形成一层一定厚度和强度的致密氧化膜,古代铁匠常用红热的铁浸入水中形成烤蓝,体现该反应原理的化学方程式为_____ 。
(3)实验室中储存FeSO4溶液时,为了防止其被空气中氧气氧化变质,会在溶液中加入一定量的______ 。
(4)某小组同学欲用废铁屑(主要成分为Fe,还含有少量Fe2O3)制备Fe2O3。操作过程如下:
i.用稀盐酸溶解废铁屑。
ii.在所得溶液中先加入过量氧化剂H2O2,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
①步骤ii中加入过量氧化剂H2O2的目的是______ 。
②设计实验验证操作i所得溶液中不含Fe3+,简述实验操作及现象:______ 。
③该小组同学认为即使操作i所得溶液中不含Fe3+,也不需要加入H2O2,若直接加入NaOH溶液可观察到的实验现象为_____ 。
(1)人体对Fe2+的吸收效果更好,但人体中时刻进行着Fe2+
 Fe3+的转化。服用补铁口服剂时,配合服用维生素C会增强人体对铁的吸收效果,在此过程中维生素C的作用是起
Fe3+的转化。服用补铁口服剂时,配合服用维生素C会增强人体对铁的吸收效果,在此过程中维生素C的作用是起(2)钢铁烤蓝是在钢铁表面形成一层一定厚度和强度的致密氧化膜,古代铁匠常用红热的铁浸入水中形成烤蓝,体现该反应原理的化学方程式为
(3)实验室中储存FeSO4溶液时,为了防止其被空气中氧气氧化变质,会在溶液中加入一定量的
(4)某小组同学欲用废铁屑(主要成分为Fe,还含有少量Fe2O3)制备Fe2O3。操作过程如下:
i.用稀盐酸溶解废铁屑。
ii.在所得溶液中先加入过量氧化剂H2O2,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
①步骤ii中加入过量氧化剂H2O2的目的是
②设计实验验证操作i所得溶液中不含Fe3+,简述实验操作及现象:
③该小组同学认为即使操作i所得溶液中不含Fe3+,也不需要加入H2O2,若直接加入NaOH溶液可观察到的实验现象为
您最近一年使用:0次
解题方法
7 . 电子工业中,人们常用 溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板。
溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板。
(1)制造印刷线路板过程中发生反应的化学方程式为___________ 。
(2)为了从腐蚀废液中回收铜,并制得可用做补铁剂的绿矾(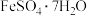 ),可以采用下列步骤:
),可以采用下列步骤:
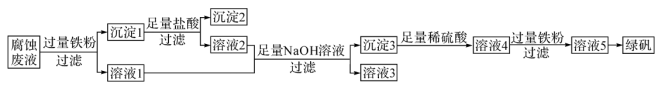
①加入过量铁粉时溶液中发生的反应有:___________ ,___________ 。
②合并溶液1和溶液2,向合并后的溶液中加入足量NaOH溶液后可观察到的现象是___________ 。其中沉淀发生转化的化学反应方程式为___________ 。
③从溶液5中获得绿矾晶体的实验操作为___________ 、过滤、洗涤、干燥。
 溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板。
溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板。(1)制造印刷线路板过程中发生反应的化学方程式为
(2)为了从腐蚀废液中回收铜,并制得可用做补铁剂的绿矾(
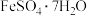 ),可以采用下列步骤:
),可以采用下列步骤:
①加入过量铁粉时溶液中发生的反应有:
②合并溶液1和溶液2,向合并后的溶液中加入足量NaOH溶液后可观察到的现象是
③从溶液5中获得绿矾晶体的实验操作为
您最近一年使用:0次
8 . 部分含铁物质的物质类别与相应化合价的关系如图所示,下列相关说法错误的是
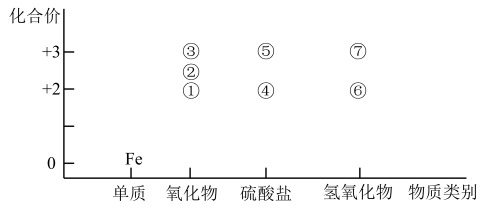

| A.Fe高温下可与水蒸气反应生成② |
| B.③用于生产红色涂料,可长久不变色 |
| C.在空气中加热⑥,不易得到纯净的FeO,易生成红棕色的Fe2O3 |
| D.向盛有少量酸性KMnO4溶液的试管中加入足量④溶液,紫色褪去,说明④溶液未变质 |
您最近一年使用:0次
解题方法
9 . 21世纪化学的最新定义为“化学是一门创造新物质的科学”。下列有关说法不正确的是
| A.开发利用太阳能、生物质能等清洁能源,有利于节约资源 |
| B.为增强治疗缺铁性贫血效果,可在口服硫酸亚铁片时同服维生素C |
| C.铝合金的大量使用归功于人们能使用焦炭从氧化铝中获得铝 |
| D.葡萄中含有的花青素在碱性环境下显蓝色,可用苏打粉检验假葡萄酒 |
您最近一年使用:0次
名校
解题方法
10 . 填空或写出下列反应的离子方程式:
(1)碘-131是元素碘(元素周期表中第53号元素)的一种放射性同位素,符号为 。在核医学中,以
。在核医学中,以 以NaI溶液的形式直接用于甲状腺功能检查和甲状腺疾病。
以NaI溶液的形式直接用于甲状腺功能检查和甲状腺疾病。 和
和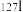 互为同位素,这两种原子的中子数差值为
互为同位素,这两种原子的中子数差值为_________ 。碘元素在元素中位于第__________ 周期第__________ 族。
(2)向明矾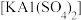 溶液中滴加Ba(OH)2、溶液
溶液中滴加Ba(OH)2、溶液 恰好沉淀,离子方程式是:
恰好沉淀,离子方程式是:________________ 。
(3)实验室常利用氨水制取Al(OH)3,而不用NaOH的溶液的原因是(用离子方程式说明)______ 。
(4)实验室用FeCl2溶液和NaOH溶液制取Fe(OH)2时观察到的现象是________________ 。
(5)将0.2mol钠、镁、铝分别投入10mL1mol/L的盐酸中,在标准状况下产生氢气体积的大小顺序是________________ 。
(1)碘-131是元素碘(元素周期表中第53号元素)的一种放射性同位素,符号为
 。在核医学中,以
。在核医学中,以 以NaI溶液的形式直接用于甲状腺功能检查和甲状腺疾病。
以NaI溶液的形式直接用于甲状腺功能检查和甲状腺疾病。 和
和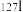 互为同位素,这两种原子的中子数差值为
互为同位素,这两种原子的中子数差值为(2)向明矾
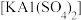 溶液中滴加Ba(OH)2、溶液
溶液中滴加Ba(OH)2、溶液 恰好沉淀,离子方程式是:
恰好沉淀,离子方程式是:(3)实验室常利用氨水制取Al(OH)3,而不用NaOH的溶液的原因是(用离子方程式说明)
(4)实验室用FeCl2溶液和NaOH溶液制取Fe(OH)2时观察到的现象是
(5)将0.2mol钠、镁、铝分别投入10mL1mol/L的盐酸中,在标准状况下产生氢气体积的大小顺序是
您最近一年使用:0次



