1 . 下列关于铁及其化合物的说法中正确的是

| A.自然界中不存在游离态的铁 |
B.红热的Fe能与水蒸气发生反应,生成 和 和 |
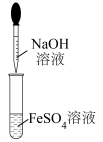
| C.图中的实验现象:生成的白色絮状沉淀迅速变成灰绿色,过一段时间后还会有红褐色物质生成 |
D. 受热分解生成的 受热分解生成的 ,俗称磁性氧化铁 ,俗称磁性氧化铁 |
您最近一年使用:0次
2 . 实验是检验真理的唯一标准。下列叙述正确的是
A. 溶液中滴加 溶液中滴加 溶液,立刻生成红褐色沉淀 溶液,立刻生成红褐色沉淀 |
| B.自由移动离子数目多的溶液导电性一定比数目少的溶液强 |
| C.分别向装有干燥的和潮湿的有色纸条的集气瓶中通入干燥的氯气,有色布条均褪色 |
| D.若容量瓶中有少量蒸馏水,配制一定物质的量浓度的溶液时,对实验无影响 |
您最近一年使用:0次
名校
解题方法
3 . 设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.14g聚乙烯与聚丙烯的混合物,含C—H键的数目为2 |
B. 和 和 均能通过化合反应制取 均能通过化合反应制取 |
| C.实验室观察气体燃烧时火焰的颜色所用的尖嘴玻璃管材质为石英玻璃 |
D.碘化银与硫化氢反应的化学方程式: |
您最近一年使用:0次
2023-02-03更新
|
287次组卷
|
4卷引用:江苏省扬州中学2022-2023学年高三下学期开学摸底考试化学试题
名校
4 . 有一固体含 、
、 、
、 中的一种或几种。现进行如下实验:
中的一种或几种。现进行如下实验:
①向固体混合物中加水并不断搅拌,固体完全溶解;
②向溶液中加入过量铁粉,充分反应后铁粉变少,同时有红色物质析出,过滤;
③向所得滤液中加入NaOH溶液至过量,开始时有白色沉淀生成,沉淀很快变为灰绿色,最终变为红褐色。
下列说法正确的是
 、
、 、
、 中的一种或几种。现进行如下实验:
中的一种或几种。现进行如下实验:①向固体混合物中加水并不断搅拌,固体完全溶解;
②向溶液中加入过量铁粉,充分反应后铁粉变少,同时有红色物质析出,过滤;
③向所得滤液中加入NaOH溶液至过量,开始时有白色沉淀生成,沉淀很快变为灰绿色,最终变为红褐色。
下列说法正确的是
A.原固体中一定有 | B.原固体中一定有 |
C.原固体中可能有 | D.实验③中既有复分解反应,也有化合反应 |
您最近一年使用:0次
5 . MgO与SiO2/CuO是重要的化工材料,利用石棉尾矿(主要含有SiO2、MgO、Fe2O3、FeO、Al2O3等)可同时制备以上两种物质,其流程如图,下列叙述错误的是


| A.滤渣l的主要成分为SiO2 |
| B.滤渣2中可能含有Fe(OH)2、Fe(OH)3、Al(OH)3 |
| C.可向滤液2中加入BaCl2溶液检验杂质离子是否除尽 |
D.焙烧发生的反应方程式为:MgCO3 MgO+CO2↑ MgO+CO2↑ |
您最近一年使用:0次
2022-08-18更新
|
1280次组卷
|
5卷引用:江苏省南通市通州区金沙中学2021-2022学年高二下学期5月线上教学质量检测考试化学试题
解题方法
6 . 实验室以硫酸亚铁晶体(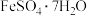 )为主要原料制取废水处理催化剂γ-FeOOH,其实验流程如图:
)为主要原料制取废水处理催化剂γ-FeOOH,其实验流程如图:

(1)称取一定量的硫酸亚铁晶体,酸溶后定容至250mL,再加入如图所示的装置中。定容所需的玻璃仪器有烧杯、玻璃棒、_______ 。

(2)沉淀时装置内需保证无氧条件,可采取的措施为_______ 。
(3)检验滤渣已洗净的操作为_______ 。
(4)已知:γ-FeOOH在水中会有部分 溶出,原子吸收仪可测定水样中
溶出,原子吸收仪可测定水样中 的浓度;在氧气的作用下,废水中的
的浓度;在氧气的作用下,废水中的 可以在γ-FeOOH表面催化结晶除去。为定量考察产品对水中
可以在γ-FeOOH表面催化结晶除去。为定量考察产品对水中 的去除效果(去除率),设计实验方案:取1g制备的γ-FeOOH,置于250mL蒸馏水中,边通空气边搅拌,一段时间后取上层清液测定
的去除效果(去除率),设计实验方案:取1g制备的γ-FeOOH,置于250mL蒸馏水中,边通空气边搅拌,一段时间后取上层清液测定 的浓度;
的浓度;_______ (实验中必须使用的物质: 溶液、空气、γ-FeOOH)。
溶液、空气、γ-FeOOH)。
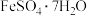 )为主要原料制取废水处理催化剂γ-FeOOH,其实验流程如图:
)为主要原料制取废水处理催化剂γ-FeOOH,其实验流程如图:
(1)称取一定量的硫酸亚铁晶体,酸溶后定容至250mL,再加入如图所示的装置中。定容所需的玻璃仪器有烧杯、玻璃棒、

(2)沉淀时装置内需保证无氧条件,可采取的措施为
(3)检验滤渣已洗净的操作为
(4)已知:γ-FeOOH在水中会有部分
 溶出,原子吸收仪可测定水样中
溶出,原子吸收仪可测定水样中 的浓度;在氧气的作用下,废水中的
的浓度;在氧气的作用下,废水中的 可以在γ-FeOOH表面催化结晶除去。为定量考察产品对水中
可以在γ-FeOOH表面催化结晶除去。为定量考察产品对水中 的去除效果(去除率),设计实验方案:取1g制备的γ-FeOOH,置于250mL蒸馏水中,边通空气边搅拌,一段时间后取上层清液测定
的去除效果(去除率),设计实验方案:取1g制备的γ-FeOOH,置于250mL蒸馏水中,边通空气边搅拌,一段时间后取上层清液测定 的浓度;
的浓度; 溶液、空气、γ-FeOOH)。
溶液、空气、γ-FeOOH)。
您最近一年使用:0次
名校
7 . 草酸亚铁晶体(FeC2O4·2H2O)可作为制备电池正极材料磷酸铁锂的原料。以FeSO4溶液制备电池级草酸亚铁晶体的实验流程如图:

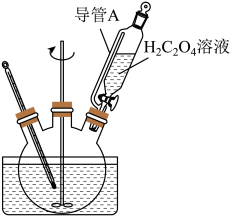
(1)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是___ 。
(2)“转化”在右图所示的装置中进行。导管A的作用是___ 。
(3)检验“洗涤”完全的实验操作是__ 。
(4)以废渣(主要含Fe2O3、Al2O3、SiO2等)为原料制备实验所需的FeSO4溶液,请补充实验方案:向废渣中分批加入稀硫酸,边加边搅拌,当固体不再溶解时,过滤;___ 。[实验中须使用的试剂:稀硫酸、铁粉、NaOH溶液、KSCN溶液、蒸馏水]
(5)测定草酸亚铁样品纯度的方法如下:准确称取0.2500g样品,加入适量水、浓H2SO4、磷酸,用0.04500mol·L-1KMnO4标准溶液滴定至终点(草酸亚铁转化为Fe3+和CO2),消耗KMnO4标准溶液18.00mL。计算样品中FeC2O4·2H2O的纯度___ (写出计算过程)。


(1)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是
(2)“转化”在右图所示的装置中进行。导管A的作用是
(3)检验“洗涤”完全的实验操作是
(4)以废渣(主要含Fe2O3、Al2O3、SiO2等)为原料制备实验所需的FeSO4溶液,请补充实验方案:向废渣中分批加入稀硫酸,边加边搅拌,当固体不再溶解时,过滤;
(5)测定草酸亚铁样品纯度的方法如下:准确称取0.2500g样品,加入适量水、浓H2SO4、磷酸,用0.04500mol·L-1KMnO4标准溶液滴定至终点(草酸亚铁转化为Fe3+和CO2),消耗KMnO4标准溶液18.00mL。计算样品中FeC2O4·2H2O的纯度
您最近一年使用:0次
2021-09-22更新
|
282次组卷
|
6卷引用:江苏省南京市2022届高三上学期9月学情调研化学试题



